|
Fa quatre dies el món sencer estava alerta per una nova variant de la grip porcina, la grip A, causada pel virus H1N1. L’11 de juny del 2009, l’Organització Mundial de la Salut (OMS) va classificar aquesta nova grip com a pandèmia. Les autoritats sanitàries de tot el planeta van posar en marxa protocols d’emergència per por que aquesta nova soca viral provoqués més baixes de les esperades. La directora general de l’OMS, Margaret Chan, advertia el següent: «pot ser que en un mes aquest virus desaparegui, pot ser que quedi com està o pot ser que s’agreugi la situació actual». La taxa de mortalitat de la malaltia, que en un principi va ser elevada, va passar a ser molt baixa després d’iniciar els tractaments amb antivirals. Gairebé cent anys abans, la grip espanyola, també coneguda com «l’epidèmia de grip de 1918», va causar la mort d’entre 25 i 40 milions de persones en tot el món. Aquesta grip va ser vehiculada per un virus de la mateixa soca que la grip del 2009, un virus gripal del tipus H1N1. El càncer, una malaltia sense cura Una malaltia infecciosa com la grip és una manifestació clínica conseqüència d’una infecció provocada per un microorganisme o per prions. Si coneixem quin és el microorganisme que causa la malaltia, en la majoria dels casos, som capaços de combatre’l i, com es va viure amb la grip de 2009, pot passar d’ocupar primeres planes dels diaris a desaparèixer de les nostres ments en qüestió de poc temps. Tots nosaltres tenim, però, algun amic, conegut o fins i tot hem patit la proximitat d’un familiar afectat per una malaltia que ha passat a formar part de la nostra societat i que malauradament encara avui dia no es pot curar: el càncer. Què és el càncer? Per què sembla que tothom deixa aquest món per causa d’aquesta malaltia? Per què, en un món on la tecnologia i els avenços científics estan a l’ordre del dia, no som capaços de trobar què és allò que fa que la gent mori, a vegades sense adonar-se’n? El càncer és la segona causa de mort a Catalunya. Segons l’OMS, el nombre de morts per càncer no para d’augmentar a nivell mundial. D’aquí al 2030 es calcula que el nombre de morts anualment s’haurà pràcticament doblat i haurà passat de quasi 8 milions de persones el 2007 a 11 milions i mig el 2030. El càncer és un tipus de malaltia en què un grup de cèl·lules adquireix un fenotip que els permet créixer de manera descontrolada i dividir-se més enllà del normal, donant lloc al que anomenem tumors malignes. Alhora, aquestes cèl·lules són capaces d’envair cèl·lules veïnes o teixits adjacents, i fins i tot d’arribar a altres punts de l’organisme mitjançant el sistema limfàtic o la circulació sanguínia per crear nous nuclis tumorals que anomenem metàstasi. La majoria dels càncers són provocats per anomalies en el material genètic de les cèl·lules canceroses. Les anomalies genètiques poden ser causades per carcinògens externs, els quals es poden adquirir de manera aleatòria, per errors en els sistemes de reparació del material genètic, o bé poden heretar-se, i per tant, estan presents en totes les cèl·lules des del naixement de l’individu. El diagnòstic definitiu d’aquesta malaltia acostuma a realitzar-se mitjançant l’anàlisi histològica del teixit afectat, el qual s’obté mitjançant una biòpsia. Alhora, existeixen un seguit de marcadors de cribatge (screening) en sèrum, que ajuden el metge en la decisió de realitzar o no aquesta biòpsia. La majoria de casos, quan són detectats en estadis inicials, és a dir, quan aquest està localitzat dintre de l’òrgan i encara no ha envaït teixits adjacents, es poden tractar eliminant el focus tumoral. Però si el tumor es detecta en estadis ja avançats, en la majoria dels casos no es coneix encara cap teràpia curativa. Generalment, el tractament es basa en una combinació de cirurgia, quimioteràpia (administració de tòxics químics) i radioteràpia (radiacions ionitzants). Tots ells ataquen d’una manera més o menys directa les cèl·lules canceroses. |
Per a il·lustrar aquest article, Mètode ha comptat amb la col·laboració de l’artista valencià Miquel Navarro (Mislata, 1945), autor de conegudes escultures en gran format i un dels artistes valencians de major projecció internacional. Miquel Navarro va rebre el Premi Nacional d’Arts Plàstiques el 1986 i actualment és acadèmic de la Reial Acadèmia de Belles Arts de San Fernando. A dalt, Miquel Navarro. Fal·lus en repòs, 2011. Terracota, dimensions variables. «El càncer és un tipus de malaltia en què un grup de cèl·lules adquireix un fenotip que els permet créixer de manera descontrolada i dividir-se més enllà del normal, donant lloc al que anomenem tumors malignes» |
|
 © National Cancer Institute, USA. |
||
|
El dilema diagnòstic del càncer de pròstata El càncer de pròstata és el càncer diagnosticat amb més freqüència i la segona causa de mort per malaltia oncològica en els homes del món occidental. S’estima que un de cada sis homes desenvoluparà un càncer d’aquest tipus al llarg de la seva vida. A Catalunya el càncer de pròstata és el càncer més freqüent abans que el càncer de pulmó i el càncer colorectal i és la tercera causa de mort oncològica que afecta la població masculina. Dades recollides per l’IARC (International Agency for Research on Cancer) a 2007 demostren que el de pròstata és el tipus de càncer més freqüent. El càncer de pròstata afecta, com el seu nom indica, la pròstata. La pròstata és un òrgan glandular de l’aparell genital-urinari masculí. Té la mida d’una nou i es localitza sota la bufeta, envoltant la uretra i davant del recte. La seva funció és secretar productes que s’afegiran al líquid seminal amb la finalitat de nodrir i protegir els espermatozous. El diagnòstic actual del càncer de pròstata es basa en una tríada diagnòstica que consta de l’anàlisi dels nivells de PSA (antigen prostàtic específic en les seues sigles en anglès) en sèrum, el tacte rectal i finalment la biòpsia prostàtica. L’antigen prostàtic específic o PSA és una proteïna secretada exclusivament per les glàndules prostàtiques, que participa en la liquació del semen ejaculat. Avui dia, encara no es coneix si aquesta proteïna representa un paper important en el desenvolupament del càncer de pròstata, però, si més no, el seu ús com a marcador de screening és conegut i utilitzat mundialment. Des que es va introduir a finals dels anys vuitanta, el diagnòstic del càncer de pròstata ha millorat significativament. Però tot i que la mortalitat deguda a aquest tipus de càncer ha disminuït, continua essent una de les formes canceroses més mortíferes que ataquen la nostra societat. Quan els nivells de PSA en sèrum se situen per sobre de 4 ng/ml, l’uròleg pot estimar quina és la probabilitat que el pacient estigui afectat per un càncer. A més a més, juntament amb la palpació de la pròstata a través del tacte rectal, es decideix la necessitat de practicar o no una biòpsia prostàtica, que permetrà establir el diagnòstic definitiu. El principal problema del PSA com a marcador de screening és que aquest presenta un nivell d’especificitat baix, un 33%, i alhora, un valor predictiu negatiu baix. L’especificitat d’una prova es defineix com la probabilitat que un individu sa tingui un resultat negatiu, i el valor predictiu negatiu, com la probabilitat que la malaltia no estigui present quan la prova resulta negativa. Exemplificat de manera numèrica, això implicaria que, de cada cent pacients que se sotmetin a un test de PSA i tinguin valors superiors a 4 ng/ml, mitjançant la biòpsia es diagnosticaran aproximadament 66 pacients negatius i només 33 pacients positius per càncer de pròstata. Per tal de detectar aquesta malaltia de manera precoç, s’aconsella que els homes a partir dels cinquanta anys es facin regularment una anàlisi dels nivells de PSA en sèrum i, quan els nivells del marcador superin els 4 ng/ml o bé quan el pacient tingui antecedents de la malaltia, es realitzarà un tacte rectal per tal de determinar la necessitat de realitzar una biòpsia. El problema és que, així com les dones se sotmeten regularment a exàmens ginecològics exploratoris, entre els homes existeix un rebuig cap a aquest tipus d’exploracions. És per tot això que el càncer de pròstata es beneficiaria de l’existència de nous marcadors de screening més específics i alhora d’un diagnòstic menys invasiu. Per altra banda, una millora en el diagnòstic evitaria un gran nombre de biòpsies innecessàries i conseqüentment un important estalvi econòmic en el cost sanitari actual. La recerca de nous marcadors en el càncer de pròstata representa un camp de treball important en la detecció precoç d’aquest tipus de càncer. Donada la situació de la pròstata a l’organisme, sota la bufeta i envoltant la uretra, les secrecions i fins i tot les mateixes cèl·lules prostàtiques, ja siguin normals o malignes, poden trobar-se presents en l’orina. És per això que considerem l’orina com una font important d’informació, a través de la qual es podria arribar a determinar quina situació es dóna a l’òrgan en qüestió. Altres estudis evidencien l’existència de potencials biomarcadors en l’orina, que podrien ajudar en la millora del diagnòstic del càncer de pròstata. A nosaltres ens ocupa l’estudi d’aquelles molècules proteiques que es troben a l’orina, ja siguin secretades per les cèl·lules prostàtiques o bé de les mateixes cèl·lules que, per descamació, van a parar a l’orina. Suposem, doncs, que un massatge prostàtic enriqueix la mostra d’orina de tot tipus de molècules proteiques. Així doncs, la nostra hipòtesi de treball abona que l’orina, després d’un massatge prostàtic, pot ser el fluid ideal per a la recerca de nous biomarcadors capaços de discriminar entre pacients amb càncer de pròstata o sense. |
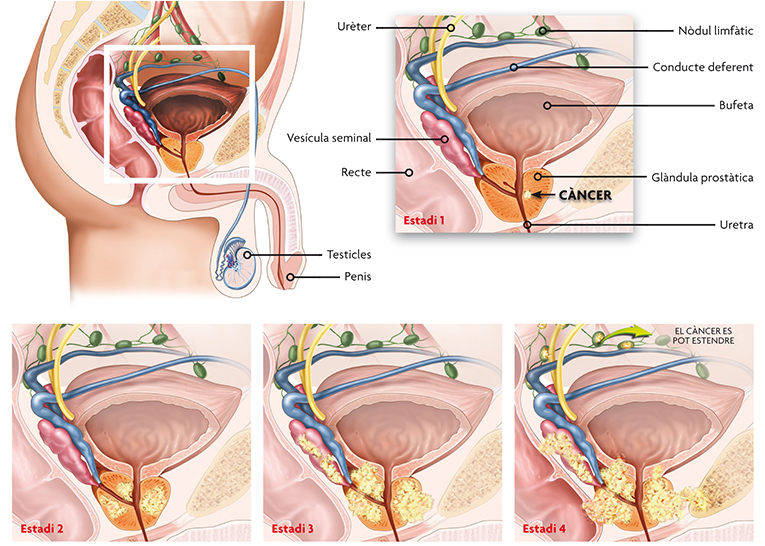
Esquema de l’evolució del càncer de pròstata. Inicialment el càncer es troba localitzat dins de l’òrgan però a mesura que aquest va progressant és capaç de sortir de l’òrgan i envair teixits adjacents. Donada la localització de la pròstata, envoltant la uretra, és possible pensar que productes derivats de la pròstata es poden trobar a l’orina, i d’aquesta manera detectar el càncer de pròstata.
«El càncer de pròstata és el càncer diagnosticat amb més freqüència i la segona causa de mort per malaltia oncològica en els homes del món occidental. S’estima que un de cada sis homes desenvoluparà un càncer d’aquest tipus al llarg de la seva vida» |
|
 |
||
|
La clau, en les proteïnes Al segle xxi ens trobem en plena era de les «òmiques». El terme òmic es refereix a l’anàlisi global dels sistemes biològics. Dins un sistema biològic el «tot» guanya importància sobre les «parts». El proteoma és la imatge dinàmica de totes les proteïnes expressades per un organisme, en un moment donat i sota determinades condicions de temps i ambient. La proteòmica es defineix com l’anàlisi del proteoma. Les proteïnes són compostos orgànics formats d’aminoàcids arranjats en una cadena lineal i units per enllaços peptídics. La seqüència d’aminoàcids que forma una proteïna és definida per l’ADN, seqüència de nucleòtids del gen que la codifica. Poc després, o fins i tot durant la síntesi, els residus d’una proteïna, sovint són modificats químicament per modificacions posttraduccionals, que alteren les propietats físiques i químiques, el plegament, l’estabilitat, l’activitat i la funció de la proteïna. El dogma general de la biologia, fins fa poc temps, establia que un gen (ADN) es transcriu a un RNA missatger (mRNA) i posteriorment es tradueix per donar lloc a una proteïna. Avui dia se sap que, a causa del processament alternatiu (splicing), un mateix gen pot donar lloc a diferents proteïnes. Per tant, si el genoma humà consta d’uns 30.000 gens, el nombre de proteïnes és exponencialment major. És per això que avui dia l’estudi del proteoma, i per tant l’anàlisi proteòmica d’elevat rendiment (High Throughput Analysis), està adquirint molta importància en el camp de la recerca. Els estudis proteòmics es basen principalment en la tècnica de l’espectrometria de masses amb combinació de mètodes de fraccionament i separació de proteïnes i pèptids (fragments proteics), com l’electroforesi bidimensional (gels de 2D) o la cromatografia líquida d’elevada resolució (HPLC). L’espectrometria de masses és una tècnica experimental que permet la mesura de ions derivats de molècules (proteïnes i pèptids). Mitjançant aquesta metodologia es poden realitzar anàlisis qualitatives i comparatives, però també quantitatives, de tot tipus de mostres proteiques. Engeguem el nostre projecte a l’Hospital de la Vall d’Hebron, que ens abasteix de totes les mostres que necessitem, clínics dedicats i gent amb moltes ganes de treballar. L’objectiu principal és arribar a determinar un perfil proteòmic a l’orina capaç de diferenciar entre pacients amb càncer de pròstata i controls sans. En primer lloc l’estudi requereix d’una recerca exhaustiva d’un grup de pacients, tots ells ben caracteritzats: homes d’edat avançada, que se sotmeten a un diagnòstic ràpid de càncer de pròstata, amb nivells de PSA per sobre de 4 ng/ml i per tant amb una certa probabilitat d’amagar un càncer de pròstata. Classifiquem els pacients en dos grups: els problemes, o dit d’una altra manera, aquells que pateixen la malaltia (ja sigui en estadis inicials o avançats), i, no menys importants, els controls, aquells qui no presenten cap anomalia considerable, en resum, controls sans. De tots ells s’obté una mostra d’orina després de la realització d’un massatge prostàtic. La mostra d’orina es processa d’acord amb el protocol estandarditzat per tal d’extreure la fracció proteica que en forma part. Tots els pacients seleccionats per l’estudi se sotmetran posteriorment a una biòpsia prostàtica, de manera que coneixerem amb certesa quin és el seu diagnòstic definitiu. La metodologia escollida per dur a terme l’anàlisi comparativa es basa en l’electroforesi bidimensional (2D). Aquesta tècnica permet separar les proteïnes pel seu pes molecular i per la seva càrrega (punt isoelèctric), situant-les en un gel de 2D. Alhora, marquem les proteïnes de cada grup (control i problema) de mostres amb un fluorocrom diferent, el qual ens permetrà visualitzar les diferents mostres en un mateix gel, i per tant, comparar-les entre si. Aquesta metodologia és coneguda amb el nom de differential in gel electrophoresis (DIGE). En total, comparem 15 mostres control amb 15 mostres problema. De l’anàlisi comparativa n’extraiem la informació necessària per tal d’establir quines són les proteïnes (punts situats al gel de 2D) que més difereixen entre ambdós tipus de mostres. Determinats els punts més rellevants, els retallem del gel i, mitjançant espectometria de masses, n’identifiquem el contingut, és a dir, quina proteïna hi correspon. Tenim una llista de vint-i-quatre proteïnes a destacar, però quina és la més important? No som capaços d’assenyalar-la amb el dit, ja que podríem errar, potser no n’és una, potser en són unes quantes plegades o potser cap. Arribats a aquest punt, l’estudi s’endinsa en un experiment de validació. Una validació experimental implica l’obtenció del mateix resultat mitjançant un altre mètode experimental. En aquest cas és important que el mètode seleccionat ens permeti avaluar els nivells de les proteïnes identificades en un gran nombre de pacients. Ha de ser, doncs, un mètode altament reproduïble i molt sensible, capaç de detectar les proteïnes a baixa concentració. Partirem d’un nombre elevat de mostres d’orina, per tal de donar certesa als resultats. Les mostres s’obtenen i es processen de la mateixa manera que anteriorment, però en aquest cas la població no se selecciona sinó que s’agafa a l’atzar. D’aquesta manera podem saber quin és el comportament d’aquestes proteïnes en la població real. Els resultats que s’obtinguin d’aquest experiment podran ser, doncs, concloents, no concloents i requerir d’una anàlisi encara més minuciosa o, fins i tot, no satisfactoris. Però això no ho sabem de moment. Els resultats preliminars assenyalen que no només serà una proteïna sola sinó un conjunt de proteïnes que a través de l’orina potser podran, algun dia, ajudar el facultatiu a prendre una decisió. Això sí, creiem que sense deixar de banda l’actual marcador diagnòstic, el PSA. Pot ser que el nostre estudi ajudi en el diagnòstic, pot ser que finalment no en traiem res i per tant que quedi com està, però en aquest cas la situació no s’agreujarà, ja que som molts els qui estem lluitant contra aquesta malaltia, ja sigui patint-la o combatent-la. Aquest article ha estat guanyador del Premi de Comunicació Científica Joan Lluís Vives 2010 (modalitat ciències bàsiques, ciències de la salut, enginyeries i arquitectures), convocat per la Xarxa Vives d’Universitats. Marina Rigau Resina. Institut de Recerca Hospital Universitari de la Vall d’Hebron (Barcelona). |
A dalt, Miquel Navarro. Nèctar, 2011. Aquarel·la, 44 x 33 cm. «Així com les dones se sotmeten regularment a exàmens ginecològics exploratoris, entre els homes existeix un rebuig cap a aquest tipus d’exploracions»
«La nostra hipòtesi de treball abona que l’orina, després d’un massatge prostàtic, pot ser el fluid ideal per a la recerca de nous biomarcadors capaços de discriminar entre pacients amb càncer de pròstata o sense»
|
|
Un dilema diagnòstic
Un dilema diagnóstico