La investigació amb cucs de seda
La seda com a biomaterial en medicina regenerativa

«Aquesta extremada versatilitat i la combinació única de resistència i biocompatibilitat no la presenta cap altre biomaterial conegut»
La seda és encara a hores d’ara un recurs econòmic important a escala mundial. El seu principal valor és, òbviament, com a fibra tèxtil de qualitat. Però aquesta no és l’única aplicació que té. Després de mil·lennis d’activitat de cria, als països asiàtics hi ha tota una cultura d’aprofitament dels bioproductes del cuc de seda i la morera, que van de l’alimentació a la medicina tradicional. En aquest sentit, és àmpliament conegut l’efecte beneficiós de les proteïnes de la seda per a la cura de la pell, la qual cosa ha portat a incorporar-les en productes cosmètics d’alta gamma. Però a més, la investigació biològica recent ha posat de manifest noves vies d’aprofitament econòmic del cuc de seda.
«La investigació biològica recent ha posat de manifest noves vies d’aprofitament econòmic del cuc de seda»
D’aquestes noves aplicacions, n’hi ha dues de destacables. Una, és l’ús del cuc de seda com a bioreactor per a produir proteïnes d’interès terapèutic i vacunes. La tècnica consisteix a inocular la larva o la pupa amb un virus del cuc (baculovirus), prèviament modificat per la substitució d’un dels seus gens amb el gen de la proteïna que es desitja expressar.
Una altra aplicació, més difosa, i que descriurem en les línies que segueixen, és l’ús de la proteïna de la seda en la fabricació de carcasses per al creixement de cèl·lules mare en la regeneració de teixits.

Alexandre
BatallerDesprés de mil·lennis d’activitat de cria, als països asiàtics hi ha tota una cultura d’aprofitament dels bioproductes del cuc de seda i la morera, que van de l’alimentació a la medicina tradicional. Però a més, la investigació biològica recent ha posat de manifest noves vies d’aprofitament econòmic del cuc de seda.
Com se sap, a partir de l’any 2000 es va descriure la potencialitat d’aquest tipus especial de cèl·lules, que són capaces de diferenciar-se a qualsevol tipus cel·lular una vegada sotmeses als estímuls adequats. Això obre un camí d’enormes possibilitats, perquè es fa factible cultivar aquestes cèl·lules autòlogues per formar teixits que poden substituir els perduts o danyats, sense cap risc de rebuig. Aquest paradigma ha donat origen a tot el camp de la medicina regenerativa i a l’enginyeria tissular, d’enorme transcendència en l’actualitat. No obstant això, en la reconstrucció de teixits hi ha un component essencial que necessiten les cèl·lules per formar-los i és una carcassa tridimensional (scaffold) sobre la qual créixer amb la forma adequada. La recerca de biomaterials i configuracions apropiades per a aquestes aplicacions és molt intensa, i se’n disposa d’una gamma molt àmplia d’aquests materials, com ara ceràmiques, biovidres, polímers, etc. No obstant això, a partir de la passada dècada van començar a aparèixer en les revistes especialitzades nombrosos treballs que descrivien les excel·lents qualitats com a biomaterial de la seda.
A hores d’ara, el desenvolupament d’aplicacions de la seda en la fabricació de carcasses per a enginyeria tissular creix de manera exponencial, i atrau nombrosos laboratoris d’arreu el món i també del nostre país.

David Pons Chaigneau
La producció de seda a Espanya va estar afectada durant segles d’un nivell tecnològic molt baix, fins que el 1892, i arran de la devastació de la indústria de la producció de seda que va representar l’aparició del patogen del cuc Nosema bombycis (causa de la «pebrina»), el Ministeri de Foment va instaurar l’estació Sericícola de Múrcia, destinada al foment de la indústria amb tecnologia apresa a Itàlia. Aquesta institució va ser la primera i única a Espanya dedicada al desenvolupament i foment de l’activitat sericícola, i va funcionar com a tal fins a 1976, quan va cessar definitivament la cria professional de cuc de seda al país. En aquesta situació, no és estrany que l’Institut Murcià d’Investigació i Desenvolupament Agrari i Alimentari (IMIDA), que n’és la continuïtat administrativa i ocupa l’espai físic de l’antiga estació Sericícola de Múrcia, aprofitara l’oportunitat de rescatar la seua tradició de 84 anys d’activitat sericícola, en un context diferent però de gran potencialitat científica i econòmica. Per fer-ho, el 2006 es va posar en marxa en aquest centre un pla d’investigació sobre biomaterials de seda, en estreta col·laboració amb diversos grups de teràpia cel·lular de tot Espanya, que ja s’ha consolidat i ha començat a produir els primers resultats.

David Pons Chaigneau
Estructura química de la seda
El capoll que forma el cuc de seda per tancar-se a l’interior i realitzar la pupació està constituït per un únic fil continu de seda compost per dues proteïnes de naturalesa molt diferent. La més important és la fibroïna, que és d’estructura polimèrica i fibrosa i constitueix la fibra (70 %) del fil de seda. La fibroïna presenta dominis peptídics repetits, formats per repeticions dels aminoàcids glicina-alanina que s’organitzen en una conformació de làmina beta típica. Aquests dominis són, per tant, hidròfobs i cristal·lins, cosa que confereix a la fibroïna una alta resistència mecànica. Al seu torn, aquests dominis estan separats per d’altres de formats per aminoàcids amb cadenes laterals llargues, que s’organitzen en hèlix alfa o plecs a l’atzar i que confereixen a la fibroïna la gran flexibilitat que la caracteritza. Aquesta estructura molecular, amb diverses variacions, és singular en la naturalesa i comuna amb la seda de les aranyes.
El fil de seda es compon també d’una segona proteïna, la sericina, d’estructura molecular globular. La seua funció és la d’actuar com a adhesiu de les fibres de fibroïna per formar l’estructura tridimensional, tancada i mecànicament resistent que constitueix el capoll.

Fotografia al microscopi electrònic de rastreig d’un fil de seda en què s’aprecia part de la coberta de sericina que revesteix la fibra de fibroïna.
Propietats de la seda com a biomateria
Quines són les propietats de la fibroïna que la fan tan apta com a biomaterial? Una propietat molt important és la biocompatibilitat. La implantació de fibroïna en els teixits no provoca rebuig ni inflamació. Això explica l’ús de la seda com a sutura quirúrgica des de fa segles fins a l’actualitat. La fibroïna en els teixits es va descomponent lentament en pèptids i aminoàcids per l’acció de les proteases. Però, a diferència d’altres biomaterials, en què els productes de descomposició poden produir una elevació local de l’acidesa, els pèptids derivats de la fibroïna tenen fins i tot un efecte bioactiu favorable. Se sap que aquests pèptids són antiinflamatoris i tenen també un efecte cicatritzant en viu.
«Una altra possibilitat que ofereix la fibroïna és la fabricació de nanopartícules que poden unir-se a fàrmacs de moltes classes»
Una altra important qualitat és que els aminoàcids que constitueixen la fibroïna presenten nombrosos grups actius (amina i carboxil) en la superfície del material. Això permet unir a la fibroïna, mitjançant enllaç covalent, una gran diversitat de lligants com ara pèptids d’adhesió cel·lular (RGD), factors de creixement cel·lular de caràcter proteic (BMP-2, bFGF…), anticossos, etc. Aquesta propietat és fonamental per a l’èxit d’un biomaterial, atès que aquests lligants actuen en l’activació de cascades de senyalització en les cèl·lules que en promouen la diferenciació cap a tipus cel·lulars específics, o n’afavoreixen l’adhesió i proliferació. Aquest diàleg bioquímic entre les cèl·lules i el biomaterial de suport és un element clau en l’enginyeria tissular.
«La implantació de fibroïna (proteïna de la seda) en els teixits no provoca rebuig ni inflamació»
Cal mencionar també com un gran avantatge de la fibroïna l’alta resistència mecànica que presenta. Encara que la resistència a tracció és menor que la de la seda d’aranya, la seda de Bombyx mori és un dels biomaterials orgànics més resistents que es coneixen. Això la fa molt adequada per a aplicacions en què la resistència mecànica és un factor rellevant, com ara la fabricació de carcasses per a teixit ossi, cartílag i lligaments.
A més, la taxa de reabsorció de la fibroïna és modulable en funció dels paràmetres de fabricació de les carcasses, i en tot cas, més lenta que la dels biomaterials orgànics habituals. Això permet que les cèl·lules sembrades tinguen temps a diferenciar-se i organitzar-se en teixits abans que la carcassa es reabsorbesca i desaparega. Finalment cal mencionar un altre avantatge molt considerable: la seda es produeix de manera molt senzilla, barata i escalable. Quasi tot el processament es realitza al medi aquós sense utilitzar reactius ni dissolvents tòxics.
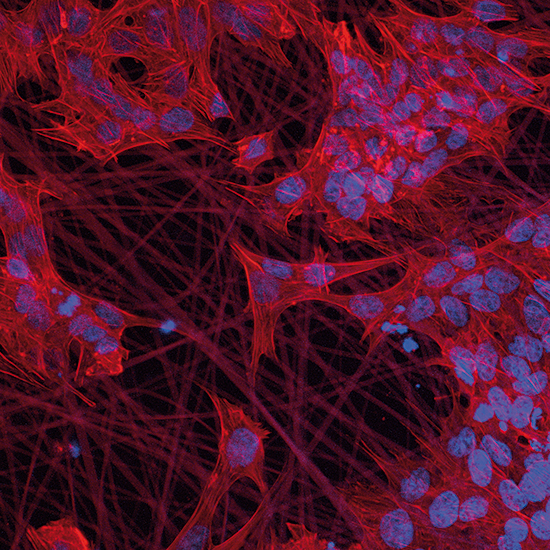
Francisco José Nicolás (Hospital Universitari Virgen de la Arrixaca, Múrcia)
Fotografia al microscopi electrònic confocal en què s’aprecien cèl·lules de pell creixent sobre una malla de nanofibres electrofilades de fibroïna de seda. En blau, el nuclis cel·lulars. En roig, els filaments de citosquelet.
Presentacions de biomaterials de fibroïna de seda
La fibroïna admet una enorme diversitat de configuracions i formats d’ús: films, gels, esponges tridimensionals, malles electrofilades, nanopartícules i fibres. Cada un d’aquests formats obre el camí a aplicacions molt diverses. La fabricació de biomaterials de seda comença pel buidatge de la crisàlide del capoll i el llavatge d’aquest amb una solució de carbonat sòdic per eliminar la sericina. Després d’aquest procés, obtenim una massa fibrosa i cotonosa de fibroïna pura, que és dissolta mitjançant una sal de gran força iònica, com el bromur de liti. Aquesta solució es dialitza per eliminar la sal, amb la qual cosa s’obté una solució aquosa de fibroïna que és el punt de partida de la fabricació
de tots els formats de biomaterials.
El material de fibroïna més senzill de fabricar és un film. Es fa abocant la quantitat adequada de fibroïna líquida en una superfície plana i deixant evaporar l’aigua. S’obté així una làmina transparent, amb la consistència i l’aspecte de la cel·lofana. Sobre aquesta làmina, submergida en un medi de cultiu adequat, poden sembrar-se cèl·lules de diversos tipus que al cap de diversos dies acaben confluint i formant monocapes equivalents a un epiteli cel·lular. Es pot millorar el creixement de les cèl·lules si el film es funcionalitza amb el pèptid RGD (arginina-glicina-àcid aspàrtic) que afavoreix l’adhesió cel·lular a través de la seua unió a les integrines de les cèl·lules. Aquest material s’investiga en l’actualitat per al desenvolupament de còrnies en reconstrucció ocular. Com que la còrnia té una estructura multilaminar de 200 a 250 làmines de col·lagen en què creixen els queratòcits, la superposició i premsatge de làmines de fibroïna ultrafines (2 microns) sembrades amb aquestes cèl·lules pot imitar l’estructura nativa.
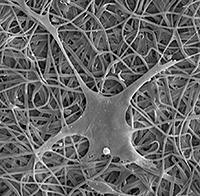
Salvador Aznar Cervantes (IMIDA)
Fotografia al microscopi electrònic de rastreig que mostra una cèl·lula mesenquimàtica de medul·la òssia creixent sobre una malla de nanofibres de fibroïna electrofilada. Les fibres tenen un diàmetre de 400 nanòmetres.
Un segon material que es pot fabricar són les esponges tridimensionals. En aquesta modalitat, es mescla la solució de fibroïna amb un porogen, típicament, clorur sòdic d’una granulometria de 800 microns. La solució s’aboca en un motle, es deixa assecar, s’insolubilitza la fibroïna immergint-la en metanol, i es llava la sal. D’aquesta manera s’obté una estructura sòlida de fibroïna pura, amb la textura d’una esponja. Els porus, connectats entre si, permeten un bon desenvolupament de les cèl·lules, amb un flux adequat de nutrients. Aquestes estructures són especialment adequades per a reparació de teixit ossi. En models animals s’han implantat aquestes esponges, prèviament premineralitzades amb hidroxiapatita, i sembrades amb cèl·lules mesenquimàtiques de la medul·la òssia. Les cèl·lules es diferencien a osteoblasts, i a mesura que aquests creixen i generen teixit ossi, la fibroïna de l’esponja es va reabsorbint. Els resultats obtinguts al cap d’un any són equivalents als obtinguts amb l’empelt d’os autòleg.
En tercer lloc podem descriure l’elaboració de la fibroïna en forma de malles obtingudes mitjançant electrofilatura (electrospinning). Aquesta tècnica consisteix en la projecció d’un doll de polímer, en aquest cas la fibroïna, en un camp elèctric de desenes de quilovolts. L’intens camp elèctric exerceix una força de tracció sobre el doll de polímer i això l’aprima fins a produir filaments de centenars de nanòmetres (milionèsimes de mil·límetre) de grossària que s’agreguen i arrepleguen com un feltre amb l’aspecte d’un full de paper en una placa col·lectora situada davall l’injector.
Aquesta estructura és molt semblant a la que presenta la matriu extracel·lular del teixit connectiu, que serveix com a suport per a la fixació i el creixement de les cèl·lules i es compon de diversos tipus de col·lagen.
A causa d’aquesta similitud amb la matriu extracel·lular, les cèl·lules de diversos tipus sembrades en aquesta estructura troben un medi molt favorable per a diferenciar-se i proliferar. Aquest tipus de carcassa, per la seua configuració bidimensional, s’està investigant àmpliament per a la reparació de pell en casos d’úlceres i cremades mitjançant sembra i conreu en aquest medi de queratinocits de la pell.
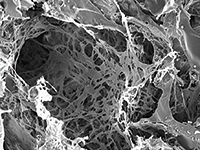
Salvador Aznar Cervantes (IMIDA)
Aquesta fotografia al microscopi electrònic de rastreig mostra la microestructura d’una esponja de fibroïna de seda preparada per a la sembra amb cèl·lules mesenquimàtiques per a creixement de teixit ossi.
Una altra possibilitat que ofereix la fibroïna és la fabricació de nanopartícules. Aquestes partícules poden unir-se a fàrmacs de moltes classes, i també a lligants i anticossos que permeten adreçar les partícules amb la seua càrrega a teixits específics. D’aquesta manera s’aconsegueix una aplicació de fàrmacs molt més localitzada i controlada, i es redueixen els efectes secundaris d’una aplicació sistèmica. La fibroïna es presta especialment bé a la fabricació de nanopartícules, a causa de les peculiaritats de la seua estructura molecular. En presència de certs dissolvents, la cadena d’aminoàcids es plega espontàniament. Així s’obtenen unes partícules de 100 nanòmetres de diàmetre que poden carregar-se amb diversos fàrmacs i proteïnes de manera covalent i que posteriorment permeten alliberar-les lentament. Amb aquesta tècnica s’han fabricat partícules conjugades amb insulina que multipliquen per 2,5 vegades la vida mitjana de l’enzim en la sang.
Cal mencionar també l’ús de fibres de fibroïna per a la formació de carcasses destinades a treballar en condicions de tensió mecànica. Un exemple molt clar el constitueix la fabricació d’estructures per a formar lligaments i tendons. En aquest cas, es realitza un trenat amb fibres de fibroïna natives, no dissoltes, i aquest trenat se sembra amb fibroblasts que al cap del temps creixen i reabsorbeixen la fibroïna per formar un substitut de lligaments.
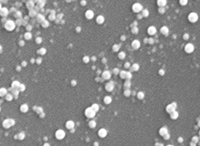
Salvador Aznar Cervantes (IMIDA)
Fotografia al microscopi electrònic de rastreig que mostra nanopartícules de fibroïna de seda, d’un diàmetre mitjà de 100 nanòmetres, utilitzables per a l’alliberament controlat de fàrmacs.
Com es dedueix d’aquesta exposició, la fibroïna de la seda ofereix una versatilitat extraordinària en la fabricació de diverses estructures destinades a sostenir el procés de formació de teixits a partir de la sembra amb cèl·lules. Però a més, la fibroïna presenta el gran avantatge de ser un material biològic, una proteïna. Això ens permet la utilització de tot el conjunt d’eines biotecnològiques per modificar-ne les propietats en funció dels diferents usos que siguen necessaris. Com que el gen de la fibroïna està identificat i clonat, és possible produir fibroïna recombinant en un sistema d’expressió fermentatiu, i també produir fibroïna quimèrica, en què es combina amb altres proteïnes, per exemple, l’elastina. Atesa aquesta possibilitat de dissenyar i expressar proteïnes de fusió amb fibroïna, la possibilitat de produir materials amb noves funcions i propietats és il·limitada. Aquesta extremada versatilitat i la combinació única de resistència i biocompatibilitat no la presenta cap altre biomaterial conegut, la qual cosa permet imaginar un enorme desenvolupament de futures aplicacions dels biomaterials de seda en el camp de la medicina regenerativa.
Referències
Altman, G. H. et al., 2003. «Silk Based Biomaterials». Biomaterials, 24: 401-416.
Kim, K. H. et al., 2005. «Biological Efficacy of Silk Fibroin Nanofiber Membranes for Guided Bone Regeneration». Journal of Biotechnology, 120: 327-339.
Lawrence, B. D.; Marchant, J. K.; Pindrus, M.; Omenetto, F. G. i D. L. Kaplan, 2009. «Silk Film Biomaterials for Cornea Tissue Engineering». Biomaterials, 30(7): 1299-1308.
Sugihara, A. et al., 2000. «Promotive Effects of a Silk Film on Epidermal Recovery from Full Thickness Skin Wounds». Proceedings of the Society for Experimental Biology and Medicine, 225: 58-64.
Wang, Y.; Kim, H-J.; Vunjak-Novakovic, G. i D. Kaplan, 2006. «Stem Cell-Based Tissue Engineering with Silk Biomaterials». Biomaterials, 27: 6064-6082.
Yan, H-B.; Zhang, Y-Q.; Ma, Y-L. i L-X. Zhou, 2008. «Biosynthesis of Insulin-Silk Fibroin Nanoparticles Conjugates and In Vitro Evaluation of a Drug Delivery System». Journal of Nanoparticle Research, 11(8): 1937-1946.
Zhao, J. et al., 2009. «Apatite-coated Silk Fibroin Scaffolds to Healing Mandibular Border Defects in Canines». Bone, 45(3): 517-527.




