Un ecosistema malalt
La lluita contra la resistència a antibiòtics des d'una perspectiva global

La producció antropogènica d’antibiòtics ha provocat una malaltia dels ecosistemes microbians de dimensió planetària, la repercussió més immediata de la qual per a l’home és la intractabilitat de les infeccions. La comprensió del fenomen i les possibilitats d’intervenció requereixen nous mètodes conceptuals, analítics i tecnològics.
Paraules clau: estratègies eco-evo, medicina planetària, resistència a antibiòtics, sistemes multijeràrquics.
Per a prevenir i remeiar la salut humana, la salut pública requereix informació de caràcter epidemiològic que descriga la dimensió (incidència i prevalença) del fenomen sota estudi i permeta induir les possibles associacions causals. És cada vegada més patent que la salut humana depèn de la salut global, és a dir, de la salut de tot el medi ambient en què l’home està inserit. En aquest sentit, els esforços per a controlar les causes que poden afectar negativament la salut de les persones han de comprendre l’anàlisi de les malalties humanes, però també de tots els altres animals (one-health perspective), les malalties dels vegetals i de la nostra extensíssima microbiosfera, el conjunt de microbis que cobreixen el nostre planeta sense conèixer fronteres, i de l’existència i equilibri del qual depèn l’existència dels éssers que, sense molta objectivitat, anomenem superiors.
Una medicina planetària
La salut humana depèn de la que posseesca el nostre planeta. Per descomptat, l’èxit biològic d’Homo sapiens ha modificat profundament la Terra, de tal manera que es pot concebre que l’home ha determinat una nova època geològica, l’Antropocè, en què la naturalesa ha resultat estressada i modificada per l’acció de l’home. Aquesta activitat antropogènica determinarà el futur de l’evolució biològica del nostre planeta. El problema que ací ens ocupa, el de la resistència bacteriana als antibiòtics, és un bon exemple per a il·lustrar els efectes deleteris per a l’espècie humana de la modificació antropogènica del medi ambient.
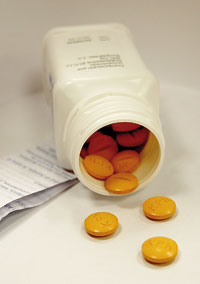
La producció industrial dels antibiòtics ha creat una vertadera «pol·lució antibiòtica planetària». Una de les malalties del planeta és deguda a aquest efecte de la producció massiva d’antibiòtics i a l’alliberament d’aquests en el medi ambient. / Agencia SINC
Probablement necessitarem l’establiment d’una vertadera «medicina planetària». La idea és que el planeta sencer ha de ser considerat com un «subjecte» que requereix atenció mèdica. La refinada metodologia mèdica destinada al malalt individual ha d’escalar-se a la dimensió del planeta, començant per definir els signes i símptomes de les malalties planetàries, estudiant-ne la patogènesi i patofisiologia, tractant d’avaluar les possibilitats de disseminació de la malaltia al conjunt del planeta, establint mètodes per a diagnosticar-la, des de tecnologies d’imatge a tecnologies avançades d’identificació molecular, i amb tot això intentar realitzar prediccions ecològiques i evolutives. Això se seguiria de l’aplicació d’intervencions específiques, sense excloure’n la cirurgia; desenvolupament de tractaments, com els futurs fàrmacs eco-evo1 (Baquero et al., 2011), mètodes de contenció i aïllament, o fins i tot aplicació de vigilància intensiva i mesures preventives. Com dèiem, el problema de la resistència als antibiòtics és un problema-model per a la futura medicina planetària; sens dubte el planeta està «malalt de resistència als antibiòtics», i aquesta malaltia, que afecta la microbiosfera, fa que molts humans estiguen colonitzats per comunitats bacterianes anormals, sovint microorganismes resistents als antibiòtics.
El diagnòstic precís de les malalties de la microbiosfera del planeta requereix millorar la sensibilitat dels nostres criteris i mètodes per a mesurar la diversitat microbiana. Els canvis en la diversitat han de constituir una de les anàlisis-clau per a detectar els símptomes i evolució de la malaltia. Sens dubte aquest objectiu requereix en primer lloc una reconsideració de les unitats biològiques bacterianes. No podem continuar utilitzant la vella classificació linneana de les «espècies microbianes». Per descomptat no podem mantenir seriosament que hi ha 20.000 espècies bacterianes «ben definides», si hem identificat 300.000 espècies de plantes o 10 milions d’artròpodes. Hauria d’haver-hi almenys uns mil milions d’espècies bacterianes, segons algunes estimacions basades en extrapolació matemàtica a partir d’estudis metagenòmics. Per descomptat hem de millorar les nostres tècniques de cultiu; la recent proposta de la «culturòmica» (inoculació de mostres naturals en múltiples medis) probablement millorarà la nostra capacitat analítica. I, per descomptat, hem de redefinir el concepte d’espècie bacteriana.
La pol·lució antibiòtica
L’home ha desenvolupat la capacitat de produir substàncies antimicrobianes per defensar-se de les malalties infeccioses, que en forma individual o sota l’espant de les grans epidèmies han assolat la nostra espècie. Davall el «paraigua protector» dels antibiòtics s’ha desenvolupat tota la medicina moderna. Sense antibiòtics una enorme proporció de les nostres persones grans i dels nostres nadons (amb defenses disminuïdes davant de la infecció) moririen d’infeccions. Sense antibiòtics serien inconcebibles les unitats de vigilància intensiva, la teràpia del càncer, l’atenció als nens prematurs, les cirurgies complexes o els trasplantaments d’òrgans. El problema és que la producció industrial dels antibiòtics ha creat una vertadera «pol·lució antibiòtica planetària». Una de les malalties del planeta és deguda a aquest efecte de la producció massiva d’antibiòtics i a l’alliberament que se’n fa en el medi ambient.
La producció industrial d’antibiòtics és un exemple paradigmàtic del tipus de substàncies antropogèniques que exerceixen un poderós efecte en la microbiosfera. Amb la producció anual de fàrmacs antibiòtics es podria cobrir la superfície de la Terra d’una capa capaç d’eliminar bacteris. No sols els antibiòtics acaben inespecíficament amb trilions de bacteris, sinó que aquesta eliminació va associada a la selecció de microorganismes resistents. La importància de la pol·lució antibiòtica del planeta no és tant la selecció de bacteris resistents potencialment patògens per als humans (i per tant causants d’infeccions intractables), sinó sobretot els efectes de caràcter «ecològic» que podrien resultar de l’eliminació de poblacions naturals i la seua substitució per d’altres. Incrementant les forces selectives i estimulant la capacitat de variació dels microorganismes (mutació, recombinació, transposició, modularització, transferència genètica) (Galán et al., 2013) els antibiòtics d’origen industrial estan modificant l’ecogenètica dels bacteris i accelerant l’evolució de la microbiosfera.
«L’home ha determinat una nova època geològica en què la naturalesa ha quedat estressada i modificada per la seua acció»
És essencial comprendre que la major part dels antibiòtics són substàncies naturals. En realitat, ha d’existir un nombre molt elevat (centenars de milers?) d’antibiòtics naturals, i només una molt petita part (menys de cent) han arribat a ser produïts industrialment i utilitzats en la medicina humana i animal. Quina és la funció natural dels antibiòtics? Els antibiòtics són substàncies que intervenen en les comunicacions intercel·lulars, substàncies «organitzadores» dels cicles vitals i de l’homeostasi de les poblacions i comunitats microbianes. El paper dels antibiòtics en la naturalesa no és necessàriament, com podria semblar a primera vista, el d’intervenir com a armes en la «guerra entre bacteris». El seu efecte inhibidor del creixement d’altres microorganismes tindria, en primer lloc, una funció defensiva, no ofensiva; d’altra banda, aquest efecte inhibidor no té com a objecte eliminar altres bacteris, sinó només la prevenció d’un sobrecreixement excessiu dels microorganismes en un ecosistema integrat. La difusió dels antibiòtics segregats per bacteris productors assegura una «zona exclusiva» a una certa distància d’aquests. En els límits d’aquesta zona, els bacteris potencialment competidors s’enfronten a concentracions antibiòtiques molt baixes, insuficients per a eliminar-los, però sí per a reduir-ne la taxa de creixement i evitar la sobrepoblació. Aquests fenòmens d’inhibició són sovint recíprocs i multilaterals, la qual cosa assegura la diversitat i l’equilibri del conjunt; els bacteris són profundament demòcrates, o, almenys, són un perfecte exemple, totalment compatible amb els enunciats de Thomas Hobbes (1588-1679), de la manera com les lleis naturals, reduint la llibertat (llibertat per a dominar) de cada individu, asseguren el manteniment de l’existència comuna, i, en suma, de l’existència biològica mateixa. Els antibiòtics són una part de la xarxa de senyals intercel·lulars i interpoblacionals que mantenen la diferenciació i la diversitat en la microbiosfera (Linares et al., 2006). Actuen per tant com a molècules-senyals, com a hormones que integren el funcionament de sistemes complexos. Com ocorre amb la major part de senyals, presenten una concentració «senyaladora» fisiològica probablement molt baixa.
La producció antropogènica d’antibiòtics equival a la producció de «senyals» intercel·lulars en quantitats inimaginablement altes, que s’alliberen a la microbiosfera. L’alta densitat de senyals deu produir un alt nivell de «soroll» indesxifrable, amb efectes deleteris sobre les xarxes informacionals dels sistemes biològics; les conseqüències ecològiques i evolutives d’aquests efectes som lluny de poder-les desxifrar.
La lluita contra els bacteris patògens: un problema global
Per descomptat, el perill més immediat i visible de l’alliberament al medi (incloent-hi els individus tractats) d’altes quantitats d’antibiòtics d’origen industrial és el desenvolupament de microorganismes resistents entre les poblacions bacterianes patògenes, que poden donar lloc a infeccions intractables. Com va dir Stuart Levy en el seu famós llibre The Antibiotic Paradox, el mal ús dels antibiòtics per part de l’home està causant que es devaluen com a fàrmacs curatius. En realitat, el problema de la resistència a antibiòtics ha arribat a un punt de no-retorn. Durant molt de temps –massa temps– s’ha postulat que un «ús adequat dels antibiòtics» (ras i curt: menor ús, amb millor detecció dels casos en què el tractament és realment necessari) hauria de portar a una reducció de les resistències. Aquesta seria la conseqüència d’un menor efecte selectiu, i també s’ha suposat que els bacteris resistents haurien de pagar un cert «cost biològic» per a mantenir aquesta nova funció, de manera que en absència d’antibiòtics els bacteris sensibles tindrien avantatge i acabarien per prevaldre. És veritat que a nivell individual, d’hospital o fins i tot de regió geogràfica, hi ha més resistència com més antibiòtics es consumixen. No obstant això, la pol·lució antibiòtica global ha portat a una vertadera invasió planetària de bacteris resistents. Com deia Carl Sagan en la seua novel·la Contact, «les fronteres són sempre arbitràries, el planeta és real», i en les regions amb millor «política d’antibiòtics» assistim ja a la invasió, des de fonts externes, de bacteris amb resistències als antimicrobians.

El mal ús dels antibiòtics en els llocs on hi ha grans masses de població humana i animal i un medi sanitari subòptim pot tenir conseqüències globals. El bacteri Staphylococcus aureus va ser «humà» a la Xina fa molts anys, va passar als porcs, es va transmetre activament a les granges, es va adaptar als animals i va reduir la patogenicitat per a l’home, però en aquest procés va adquirir els mecanismes genètics de resistència a antimicrobians. A Europa, de nou el clon resistent CC398 ha contaminat humans. / Carl Jones
Els països de l’Orient, cada vegada més interconnectats amb l’Occident, posseeixen grans masses de població humana i animal, un mitjà sanitari subòptim amb greus deficiències en la sanitat mediambiental, i el seu creixent desenvolupament els permet un alt grau d’utilització d’antimicrobians. El resultat és un «reactor» on l’evolució de la resistència a antimicrobians s’està precipitant. Dos exemples reflecteixen aquesta situació. El primer és la inesperada aparició en casos humans a Holanda de Staphylococcus aureus amb resistència a meticil·lina (a tots els antibiòtics beta-lactàmics). Estudis moleculars han demostrat que el clon bacterià responsable, S. aureus CC398, arribà a Europa a través d’animals (porcs) d’origen xinès. Aquest bacteri va ser «humà» a la Xina fa molts anys, va passar als porcs, es va transmetre activament en les granges, es va adaptar als animals i va reduir la patogenicitat per a l’home, però en aquest procés va adquirir els mecanismes genètics de resistència a antimicrobians. A Europa, de nou el clon resistent CC398 ha contaminat humans. El segon exemple es relaciona amb l’aparició a Europa (Suècia i Regne Unit) de soques d’enterobacteris amb un nou enzim de multiresistència a beta-lactàmics, la Nova Delhi metal·lobetalactamasa (NDM), procedent de la «importació» d’un cas humà des de Nova Delhi, a l’Índia. S’ha demostrat de fet que la soca està molt disseminada en l’Índia, on probablement es va produir l’emergència. A Europa ha tingut lloc una disseminació secundària que també ha afectat a Espanya.
Claus evolutives
Quines són les claus evolutives de la invasió planetària de la resistència als antibiòtics? Què podem fer per controlar aquesta situació? La primera clau evolutiva és la massiva producció industrial de fàrmacs antimicrobians, l’ús massiu que se’n fa en medicina, veterinària i agricultura, i l’alliberament consegüent d’aquestes substàncies al medi ambient. Com hem vist, l’efecte esperat és la selecció de poblacions resistents, però també l’acceleració de la variació bacteriana i la distorsió del sistema de senyals que regula l’homeostasi de la microbiosfera. Seria necessari regular no sols l’ús adequat, sinó la biodegradació (antibiòtics biodegradables) o almenys el confinament i tractament dels residus que continguen antibiòtics.
La segona clau evolutiva és la interacció entre els bacteris colonitzadors o patogènics d’homes i animals amb els microorganismes del medi ambient. Els bacteris mediambientals (del sòl, en particular de la rizosfera; i de l’aigua, en especial dels sediments) contenen un completíssim repertori de gens de resistència (el resistoma mediambiental) que poden ser transferits per elements genètics mòbils als bacteris perillosos per a la salut pública. Els bacteris d’origen humà i animal (imaginem aigües residuals d’hospitals, de granges) estan passant amb poques limitacions al medi ambient, contaminen els ecosistemes amb gens de resistència amplificats per acció antropogènica, i poden al seu torn rebre nous gens des dels bacteris mediambientals. La densitat d’interaccions és enorme en països hiperpoblats amb baix nivell sanitari. És incomprensible que els epidemiòlegs i sanitaris no hagen estat capaços de proposar seriosament l’absoluta necessitat d’impedir el contacte entre bacteris humans-animals i mediambientals (Baquero et al., 2008). Necessitem tecnologia d’esterilització dels nostres residus (aigües fecals) abans de ser alliberats al medi, tant a escala industrial (per exemple depuradores a l’eixida dels hospitals) com familiar, en regions de baix nivell sanitari (minitancs sèptics).
«El perill més immediat i visible de l’alliberament al medi d’altes quantitats d’antibiòtics d’origen industrial és el desenvolupament de microorganismes resistents entre les poblacions bacterianes patògenes»
La tercera clau evolutiva és la disseminació global dels clons bacterians d’alt risc que fan circular la resistència a antibiòtics a escala planetària, i disseminar-la a altres bacteris. Aquests clons circulen probablement per les que Mark Ragan va qualificar d’«autopistes de la circulació de gens». L’àmplia circulació assegura el progressiu reclutament de nous gens i el desenvolupament de bacteris multiresistents. Hem de millorar la nostra tecnologia per detectar amb tècniques ràpides aquests clons d’alt risc en persones, animals i medi ambient, i identificar les «autopistes» per les quals circulen en el planeta. Hem de millorar les nostres possibilitats d’eliminar aquests clons perillosos, amb una «terapèutica dirigida al clon» (clone-directed therapy) o aplicant estratègies de vacunació específiques. Hi ha precedents de l’èxit potencial d’aquestes intervencions, com la vacunació contra clons resistents de Streptococcus pneumoniae o Haemophilus influenzae.
La quarta clau evolutiva es basa en el fet que l’evolució de la resistència als antibiòtics es desenvolupa en el si d’un sistema multijeràrquic complex. Els gens de resistència, les plataformes genètiques en què se situen, els elements genètics mòbils (capaços de passar de cèl·lula a cèl·lula) en què s’insereixen aquestes plataformes, les cèl·lules bacterianes on entren els elements mòbils, els complexos clonals a què pertanyen aquestes cèl·lules, les espècies i comunitats microbianes, els ecosistemes, constitueixen distintes unitats evolutives embotides les unes dins de les altres, és a dir, formant una estructura introgressiva en múltiples nivells (Bapteste et al., 2012). De fet, caldria desenvolupar una epidemiologia integrada multijeràrquica, per poder realitzar estudis de biologia de poblacions independentment per a cada unitat evolutiva, i induir els efectes de les variacions dels distints elements en el sistema complex (Baquero et al., 2013). Coneixent aquestes dades, serà possible en el futur realitzar una vertadera intervenció eco-evo (incloent-hi «fàrmacs» per a curar de resistència determinats ecosistemes, com el microbioma humà; Baquero et al., 2011).
En suma, la confluència de coneixements ecològics i evolutius serà necessària en el pròxim futur per a comprendre i corregir l’important problema de salut pública, o, si es vol, de salut global, que constitueix l’exposició de la microbiosfera a quantitats massives d’antibiòtic, el reflex més pròxim del qual és la resistència a antibiòtics en bacteris que infecten l’home i els animals.
1. El terme eco-evo, acrònim d'«Ecologia i Evolució», fa referència a l'aproximació biològica que considera la possibilitat d'estudiar i actuar integradament en l'ecologia (senyals ambientals) i l'evolució (modificació hereditària dels organismes com a resposta adaptativa a aquests senyals). (Tornar al text)
REFERÈNCIES
Bapteste, E. et al., 2012. «Evolutionary Analyses of Non-genealogical Bonds Produced by Introgressive Descent». PNAS, 109(45): 18.266-18.272. DOI: <10.1073/pnas.1206541109>.
Baquero, F.; Coque, T. M. i F. de la Cruz, 2011. «Ecology and Evolution as Targets: the Need for Novel Eco-evo Drugs and Strategies to Fight Antibiotic Resistance». Antimicrob Agents Chemother, 55(8): 3.649-3.660. DOI: <10.1128/AAC.00013-11>.
Baquero, F.; Martínez, J. L. i R. Cantón, 2008. «Antibiotics and Antibiotic Resistance in Water Environments». Current Opinion in Biotechnology, 19: 260-265. DOI: <10.1016/j.copbio.2008.05.006>.
Baquero, F.; Tedim, A. P. i T. M. Coque, 2013. «Antibiotic Resistance Shaping Multilevel Population Biology of Bacteria». Frontiers in Antimicrobials, Resistance and Chemotherapy. Prepublicat online: 6 de març de 2013. DOI: <10.3389/ fmicb.2013.00015>.
Galán, J. C.; González-Candelas, F.; Rolain, J. M. i R. Cantón, 2013. «Antibiotics as Selectors and Accelerators of Diversity in the Mechanisms of Resistance: from the Resistome to Genetic Plasticity in the β-lactamases World». Frontiers in Antimicrobials, Resistance and Chemotherapy. Publicado online: 8 de febrer de 2013. DOI: <10.3389/fmicb.2013.00009>.
Levy, S. B., 2002. The Antibiotic Paradox. Da Capo Press. Cambridge, MA.
Linares, J. F.; Gustafsson, I.; Baquero, F. i J. L. Martínez, 2006. «Antibiotics as Intermicrobial Signaling Agents Instead of Weapons». PNAS, 103(51): 19.484-19.489. DOI: <10.1073/pnas.0608949103>.