|
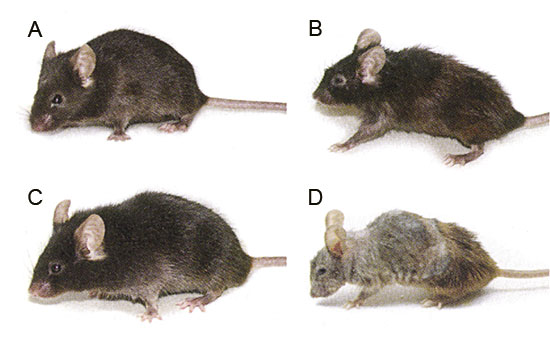
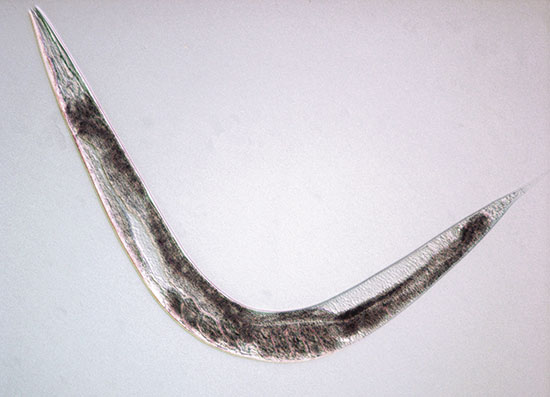
Genes modifying the lenght of life: longevity and premature aging. Aging is one of the most complex biological processes determined by both genetic and environmental factors. According to developmental genetics theories, aging is a genetically and controlled continuum of development and maduration. Alternatively, the genetic contribution to aging could be limited to providing a predisposition for the organism to respond to changes or the other challenges life demands. Regardless of how genetic elements participate in aging, the genetic approach has been used as a tool to identify these elements. Considerable progress has been made in discovering genes that regulate longevity by identifying single gene mutation that lead to increased longevity in worms, flies and rodents. In human several genetic diseases display some features of accelerated aging. In contrast, centenarians are the best example of successful aging. To achieve their extreme age, centenarians are likely to lack numerous gene variants that are associated with premature mortality, and they may be more likely to carry protective variants as well. L’envelliment és un dels processos biològics més complexos dels organismes pluricel·lulars i les seues causes cal buscar-les tant en factors ambientals com genètics. S’han proposat dos possibles mecanismes d’acció dels factors genètics en el control d’aquest procés. D’acord amb les teories genètiques del desenvolupament, l’envelliment no és més que un continuum del desenvolupament i la maduració des de la formació del zigot, es tracta d’un procés programat genèticament. Com a alternativa, la contribució genètica podria més aviat modular la diferent capacitat dels individus a respondre davant els canvis soferts al llarg de la vida. Aquesta seria una concepció menys determinista del paper dels gens, més en sintonia amb les teories estocàstiques que proposen com a causa de l’envelliment el dany que aleatòriament poden sofrir les molècules vitals. En aquest sentit, alguns autors donen suport al fet que molts dels canvis soferts durant l’envelliment són deguts a les alteracions provocades pels radicals lliures, molt especialment per les espècies reactives de l’oxigen generades pel metabolisme aerobi. Si els gens controlen la capacitat de defensa dels organismes enfront de les alteracions degeneratives, podrien, per tant, determinar la durada de la vida i el procés d’envelliment. Independentment de si els gens participen de forma activa (a través de rutes més o menys establertes) o de forma menys directa (conferint major o menor vulnerabilitat), s’han desenvolupat nombroses estratègies encaminades a identificar aquests elements genètics. Els estudis realitzats en organismes model han contribuït de manera decisiva en aquest projecte. Models genètis per a l’estudi de l’envelliment La primera aproximació experimental que la durada de la vida és un caràcter hereditari es va realitzar en mosques del gènere Drosophila. Es va observar que diferents soques i línies derivades d’individus adults capturats de les poblacions naturals tenien diferents però reproduïbles expectatives de vida. Posteriorment, els experiments de selecció van assenyalar l’existència de gens amb capacitat d’augmentar de forma significativa aquestes expectatives. Aquests experiments van demostrar la plasticitat del caràcter, en què intervenen dos elements principals: el genoma de l’individu i l’ambient en el qual es desenvolupa. No obstant això, és molt difícil identificar, quants i quins gens estan involucrats en aquest procés. L’estratègia més comuna ha estat la recerca d’aquells gens que quan experimenten mutacions en la seua seqüència alteren la durada de la vida. La majoria dels estudis s’han centrat més en l’allargament de la vida que en la seua reducció, ja que aquest últim cas sol anar acompanyat d’alteracions patològiques que dificulten l’estudi del procés. S’ha vist que aquests gens poden participar en funcions molt diferents: en el metabolisme respiratori, en la defensa antioxidant, en la replicació i reparació del DNA, en el control del cicle cel·lular… Mutacions que allarguen la vida Figura 1. Les mutacions en el gen daf-2 poden augmentar al doble la vida del nemàtode C. elegans. Des de la identificació del gen daf-2 es va iniciar la recerca del que s’han anomenat “gens de la longevitat”. Els candidats són aquells que participen en la ruta d’acció de la insulina i vies acoblades, en definitiva gens reguladors de la utilització de l’energia. Molts d’ells, com els que participen en la transducció del senyal insulínic, apareixen conservats en els animals. La plasticitat en la durada de la vida, evident en la filogènia animal, es podria deure a la variació en el temps de l’alliberament d’hormones que controlen la vitalitat i la mortalitat, així com a la variació a la resposta a aquestes hormones. En Drosophila s’han descrit dos exemples molt notables de gens que prolonguen la vida. Una reducció parcial del nivell d’expressió del gen methuselah resulta en un 35% d’increment de la durada de la vida mitjana. Les mosques mutants són, a més, resistents a diversos tipus d’estrès, incloent-hi la dessecació, l’augment de la temperatura, la inanició i els radicals lliures. Aquest gen codifica un probable receptor acoblat a la proteïna G i s’especula amb la possibilitat que aquesta proteïna intervinga en el cost sensitiu de la mosca en la via insulínica. L’altre locus que augmenta la longevitat en Drosophila és Indy (I’m not dead yet, “encara no sóc mort”), que codifica per a un possible transportador en el cicle de Krebs, amb certa homologia amb el transportador del dicarboxilat de mamífers. Una reducció de l’expressió d’Indy augmenta al doble l’expectativa de vida mitjana i més del 40% la vida màxima possible. Les mosques no perden la seva capacitat de reproducció ni tampoc la seua activitat física. S’ha proposat que les mutacions en Indy poden induir un estat similar a la restricció calòrica. La hipòtesi de l’estrès oxidatiu, com a causa de l’envelliment és una de les que més s’ha tingut en compte. Si aquesta hipòtesis és correcta, es pot esperar que l’augment de la dosi d’aquells gens que codifiquen per a enzims antioxidants puguen allargar la vida. De fet els mutants de Drosophila amb pèrdua de funció gènica en qualsevol dels tres enzims antioxidants catalasa, superòxid dismutasa dependent de Cu/Zn (SOD) i tioredoxin reductasa (TxR), exhibeixen una vida més curta en la fase adulta. No obstant això, la introducció d’una còpia addicional del gen SOD no ha donat lloc a mosques més longeves com es podria esperar. Tampoc les mosques transgèniques que sobreexpressen el gen de la catalasa tenen vides més llargues. En general, els resultats obtinguts dels experiments d’augment de dosi en aquest tipus de gens han estat bastant contradictoris. En una sèrie de treballs molt interessants, s’ha descrit un increment de la vida de les mosques entre un 40-50% quan qualsevol dels gens humans SOD1 o SOD2 se sobreexpressa en un teixit específic en Drosophila: les motoneurones de l’adult. També s’ha plantejat el possible paper de les proteïnes de plegament (chaperons) en l’envelliment. Tenen un paper de protecció en la cèl·lula: prevenen l’agregació de molècules defectuoses, dissolen agregats proteics, ajuden al correcte plegament de les proteïnes alterades. La proteïna de xoc tèrmic HSP70 constitueix una de les proteïnes de plegament més importants i el seu nivell augmenta amb l’edat. S’ha publicat que un moderat xoc tèrmic en una soca de Drosophila portadora de dotze còpies addicionals del gen hsp70 condueix a un descens significatiu de la mortalitat en els adults. Recentment, s’ha demostrat que la sobreexpressió d’aquesta proteïna pot protegir de la degeneració observada en els models establerts en Drosophila per a les malalties de Huntington, Parkinson i altres patologies neurodegeneratives. Mutacions que redueixen la vida En els mutants de ratolí, a més d’observar-se una reducció en la durada de la vida, es detecta de forma prematura la presència de certes alteracions que van associades a l’envelliment, com osteoporosi, pèrdua de greix subcutani, pèrdua de pèl i atròfia general de diversos òrgans (figura 2). És el cas, per exemple, dels ratolins amb alteracions funcionals en els gens XPD, o p53. El primer codifica per a una DNA helicasa, implicada tant en la reparació del DNA danyat com en la transcripció. La hipòtesi amb la qual actualment es treballa per explicar l’efecte de la disminució de l’activitat d’aquest gen en els ratolins és una important disminució en el recanvi cel·lular a causa d’un alt nivell de apoptosi causat per la falta de reparació dels errors en el DNA. També es postula un increment de mort cel·lular i una falta de recanvi cel·lular en els ratolins mutants amb un guany de funció del gen p53, un gen clau en el cicle cel·lular. Figura 2. Els ratolins deficients en el gen XPD es desenvolupen normalment durant els primers mesos, però comencen a mostrar símptomes d’envelliment de forma prematura al voltant dels tres mesos. Longevitat i envelliment en humans Centenaris i la síndrome de la longevitat Recentment, s’ha identificat una regió en el cromosoma 4 humà, portadora d’un gen possiblement implicat en la longevitat. Dels 50 gens presents en aquesta regió, s’ha prestat atenció al gen MTP (que codifica per a una proteïna microsomal) donada la seua implicació en el muntatge de les lipoproteïnes. S’ha observat l’associació entre diversos polimorfismes d’aquest gen amb la resistència a la insulina i amb la distribució del greix, i s’ha observat la menor prevalença d’alguns d’aquests polimorfismes en les persones longeves. Altres gens candidats s’han localitzat tots en una mateixa regió cromosòmica: en 11p15.5. Es tracta dels gens TH (tirosina hidroxilasa), INS (proinsulina), IGF2 (factor 2 de creixement similar a insulina), HRAS1 (protoncogen) i SIRT3 (sirtuina 3). Tots formen part de rutes funcionals conservades en l’evolució i s’ha postulat que podrien coordinar la durada de la vida des dels invertebrats a l’home, controlant el metabolisme energètic i la resposta enfront de l’estrès. Alguns d’aquests gens s’han considerat dianes per a l’acció de nous medicaments que puguen prolongar la vida en condicions saludables. Síndromes d’envelliment prematur en humans La síndrome de Werner va ser descrita en l’any 1904 i té una incidència molt variable, entre 1 i 20 casos per milió. Els pacients desenvolupen prematurament arteriosclerosi, intolerància a la glucosa, osteoporosi, pèrdua de pèl, atròfia de la pell i menopausa en el cas de les dones. L’envelliment progressiu fa que el seu aspecte siga d’uns trenta anys més que l’edat real i la majoria mor, generalment, abans dels cinquanta anys (figura 4). El gen responsable es va localitzar, el 1991, en el cromosoma 8p mitjançant l’anàlisi de lligament en famílies afectades. La malaltia s’hereta amb un patró recessiu. El 1993 es va concretar que aquest gen devia participar en el recompte de les divisions cel·lulars, ja que els cultius de fibroblasts dels pacients només es divideixen unes vint vegades en lloc de cinquanta o seixanta com ocorre en les cèl·lules normals. Aquest gen, anomenat WRN, codifica una helicasa de la família RecQ, amb capacitat de desenrotllar el DNA i implicada en processos de replicació i reparació del DNA. En les cèl·lules dels pacients s’observa un augment d’aberracions cromosòmiques, elevades taxes de mutacions gèniques i recombinació no homòloga. Per aquestes característiques, aquesta síndrome es classifica dintre de les síndromes amb inestabilitat cromosòmica. El paper dels telòmers i de la telomerasa La telomerasa és l’enzim responsable de mantenir la longitud del telòmer. És activa durant la gametogènesi, i permet la viabilitat a llarg termini de les cèl·lules germinals. Aquest enzim es troba reprimit durant la diferenciació de les cèl·lules somàtiques, per aquest motiu aquestes van perdent seqüència telomèrica en cada cicle de replicació. La presència de telomerasa en diversos tipus de càncers humans està en sintonia amb l’elevada capacitat de divisió de les cèl·lules tumorals. Actualment, s’ha aconseguit demostrar in vitro que les cèl·lules poden viure més temps si s’allarguen artificialment els telòmers dels seus cromosomes. Falta veure si aquesta tècnica seria aplicable a un ésser viu perquè poguera gaudir d’una vida més llarga de la que és pròpia de la seua espècie. M. Dolores Moltó i Carmen Nájera. Departament de Genètica, Facultat de Ciències Biològiques, Universitat de València.
|
«L’envelliment és un dels processos biològics més complexos dels organismes pluricel·lulars i les seues causes cal buscar-les tant en factors ambientals com genètics»
Figura 3. Els nens amb progèria mostren un aspecte mes propi dels ancians.
«Alguns investigadors intenten comprovar en si mateixos si una dieta hipocalòrica pot retardar l’envelliment en humans»
Figura 4. L’efecte de la síndrome de Werner es pot observar en aquesta dona comparant la seua imatge quan era una adolescent i als 48 anys.
«S’ha vist que els descendents dels centenaris tenen majors nivells de lipoproteïnes d’alta densitat (colesterol bo) i nivells més baixos de lipoproteïna de baixa densitat (colesterol dolent)» |
Gens que modifiquen l’extensió de la vida: longevitat i envelliment prematur