| © M. Lorenzo El futur de l’alimentació és la nutrició personalitzada, és a dir, dietes intel·ligents dissenyades d’acord amb les demandes específiques de genotips individuals i de la seva història. |
||
|
Nutrigenomics: personalized nutrition. Actualment és creixent el coneixement al voltant de les relacions entre salut i alimentació. És ben coneguda la relació entre el nostre benestar i longevitat amb la diversitat bioquímica dels aliments que mengem, a més d’altres condicionaments ambientals. Al mateix temps també va augmentant la difusió del fet que les àmplies diferències que es donen entre individus en la resposta a l’alimentació depenen de les característiques particulars codificades en els nostres gens i de les adaptacions implementades a les diferents condicions experimentades per cada persona al llarg de la seva vida. Entorn d’això sorgeix la nutrigenòmica, com a disciplina emergent que estudia com interaccionen els aliments i els seus components amb la informació codificada en els nostres gens i amb tot l’entramat metabòlic que se’n deriva, així com les seves conseqüències a tots els nivells. La nutrigenòmica pretén el coneixement extensiu i integrat de la manera com les dietes o els seus components afecten els sistemes biològics a tots els nivells, des de l’expressió de la informació genètica que els caracteritza (transcriptoma), la seva composició en proteïnes (proteoma) i les diferents biomolècules o metabòlits que els constitueixen (metaboloma) i com tot això es tradueix en el funcionament d’aquests sistemes i repercuteix en l’organisme complet. La nutrigenòmica s’ocupa també de conèixer i caracteritzar la diferent resposta a l’alimentació segons el genotip (nutrigenètica) i segons la història alimentària individual (epigenètica). Sovint nutrigenòmica i nutrigenètica es consideren dues disciplines diferents. La nutrigenètica, o genòmica nutricional, pretén entendre com les característiques genètiques d’un individu determinen la seua resposta a la dieta, i per aconseguir-ho aquesta disciplina es basa en la consideració dels polimorfismes subjacents. En abraçar un camp més ampli, la nutrigenòmica tracta de determinar la influència dels aliments sobre el genoma, i prova de relacionar els diferents fenotips resultants amb la resposta genètica, cel·lular o fisiològica i, en general, del sistema biològic, i així també comprèn l’estudi de la resposta diferencial associada a genotips (nutrigenètica) i a fenotips particulars. Un objectiu últim de la nutrigenòmica és també el desenvolupament d’aliments que s’ajusten a les conveniències de salut de persones individuals. En realitat, el veritable repte de fons és la integració de tota la informació, la de les dades i coneixements aportats per les noves tecnologies òmiques (genòmiques i postgenòmiques) amb les que aporta la nutrició clàssica i el metabolisme humà; tot allò que permet desvelar els efectes d’un agent extern sobre un organisme. No és estrany, doncs, que al caient dels avenços vagin sorgint nous termes i conceptes com el de «Biologia de sistemes», «Metabolisme integrat» o «Biologia nutricional de sistemes», que tracten de delimitar parcel·les concretes del coneixement. Aquí considerem que el terme «nutrigenòmica» és prou ampli i apropiat per a englobar, almenys de moment, tots aquests nous desenvolupaments en l’àmbit de l’alimentació i la salut a què ens hem referit. En realitat, tenim coneixements nutrigenòmics des de fa molts anys i els apliquem; com per exemple quan restringim la dieta de determinades persones afectades per malalties degudes a variants o mutacions gèniques individuals (els denominats errors congènits del metabolisme) o quan es prescriu no ingerir determinats aliments a certs grups de població que, a diferència d’uns altres, presenten reaccions adverses enfront d’un determinat component alimentari. No obstant això, el marc que configura la nutrigenòmica és molt més ampli, considera els polimorfismes (les diferents variants gèniques), en els quals la presència d’un al·lel o un altre suposa només certa diferència, encara que sigui petita, pel que fa a determinada funció, i considera també les combinacions de múltiples variants que, tractades individualment, poden no tenir efecte funcional però que en combinació determinen noves propietats (Palou et al., 2004). Considera també la història metabòlica de cada persona, el resultat de l’exposició a diferents nutrients i altres factors al llarg de les diferents etapes de la vida (epigenètica); sens dubte aquesta història individual contribueix significativament a una resposta també individualitzada. Considera també els mecanismes implicats en els efectes de l’alimentació i la transcendència d’aquests efectes a tots els nivells fenotípics i en particular com afecten la balança que, a banda i banda, condueix cap a la funció o la disfunció, la salut o la malaltia. |
«La nutrigenòmica pretén el coneixement extensiu i integrat de la manera com les dietes o els seus components afecten els sistemes biològics a tots els nivells» | |
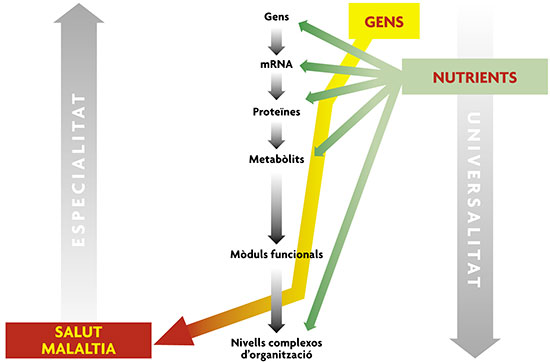 © Mètode Els efectes dels aliments sobre els sistemes biològics es poden descriure mitjançant la informació nutrigenòmica (perfil genètic, expressió de RNA missatgers, proteïnes i metabòlits). Aquests efectes poden consistir en canvis o desplaçaments del sistema que controla el pes corporal i contribuir d’aquesta manera a l’obesitat; en nutrigenòmica ens agradaria que la descripció dels gens / expressió gènica / proteïnes / metabòlits, en una persona, ens permetés predir les possibles desviacions de la seva homeòstasi ja en les persones sanes, és a dir, abans que els sistemes haguessin quedat irreversiblement decantats cap al desenvolupament, a curt, mitjà o llarg termini, de malalties. (Adaptat d’Oltvai i Barabasi, 2002). |
«La nutrigenòmica s’ocupa de conèixer i caracteritzar la diferent resposta a l’alimentació segons el genotip i segons la història alimentària individual»
«En realitat tenim coneixements sobre nutrigenòmica des de fa molts anys, i els apliquem» |
|
|
LES NOVES TECNOLOGIES EN LA NUTRIGENÒMICA La nutrigenòmica utilitza les tècniques tradicionals en metabolisme i nutrició però també les noves tecnologies bioquímiques i, en particular, les denominades tecnologies òmiques (transcriptòmica, proteòmica, metabolòmica), es nodreix dels ràpids avenços en el coneixement dels gens que conformen el genoma, els seus mecanismes de regulació i com certs components dels aliments incideixen en aquests sistemes; i es beneficia dels grans progressos en el coneixement de la bioquímicca i fisiologia humana i en particular del metabolisme. Així, la nutrigenòmica dota d’un valor afegit els coneixements epidemiològics i els continguts clàssics de la nutrició, conferint a aquesta ciència una sòlida capacitat predictiva. (del grec, “complet”) que apareixen en la literatura científica. El consorci per als SNP (Single Nucleotide Polymorphisms) està localitzant nombrosos polimorfismes en el genoma humà que determinen diferències en les característiques fenotípiques individuals que es troben en la població. La genòmica es pot descriure com l’estudi i caracterització de la seqüència de tots els gens presents en una determinada espècie. Derivats d’ella, podem considerar la «genòmica funcional», que cobreix els aspectes del coneixement de les funcions dels diferents gens i com aquests gens interaccionen o s’influencien entre si, i la transcriptòmica, que utilitza les tecnologies de microxips (microarrays) de cDNA o d’oligonucleòtids com a aproximacions per a analitzar l’expressió gènica (es poden determinar milers de mRNA en qualsevol mostra biològica en unes determinades condicions). El transcriptoma és el conjunt de tots els mRNA d’un fluid, cèl·lula, teixit o mostra biològica en general. En aquests moments és la tecnologia òmica més àmpliament utilitzada i la que gaudeix d’unes millors possibilitats de validació i estandardització per a, pràcticament, tots els mRNA transcrits, encara que es requereix una quantitat de mostra relativament gran per aïllar prou quantitat del mRNA que es necessita. La proteòmica pretén determinar totes les proteïnes d’una mostra biològica, incloent-hi l’abundància relativa, distribució, modificacions post-traduccionals, funcions i interaccions amb altres molècules biològiques i, encara que es van obtenint ja resultats, en aquests moments es perfilen desenvolupaments tecnològics que la convertiran en una tècnica molt poderosa. La metabolòmica (o metabonòmica, menys preferible aquí per estar més associat al perfil de metabòlits en els estudis de fàrmacs) pot definir-se com l’anàlisi quantitativa de tots els metabòlits, endògens i exògens, d’un determinat fluid biològic, teixit o, en general, d’un sistema biològic determinat. Independentment que la proteòmica i, més encara, la metabolòmica requereixin del bagatge de més estudis que ens proporcionin d’estàndards i procediments de rutina, aplicables de manera generalitzada, per al desenvolupament complet dels objectius d’aquestes tècniques en nutrició, manquen més eines matemàtiques. Avui no tenim tractaments apropiats per als molts milers de dades que generen els estudis i, tot i ser difícil de precisar, creiem que es processa menys del 2% de la informació obtinguda; la resta es perd. Això obliga a aplicar estratègies de selecció dels paràmetres a analitzar, que permeten abaratir el cost dels procés per bé que no està clar que sigui l’opció més apropiada. Una eina fonamental pendent és l’establiment de perfils òmics definitoris d’estats de «salut estàndard» que puguin servir com a referència o control en els diferents estudis. Anàlogament podem referir-nos a l’establiment de perfils nutrigenòmics per a altres condicions com ara la diabetis mellitus tipus 2, les obesitats i altres malalties o condicions fisiològiques d’interès (vegeu més endavant). Una de les majors dificultats la trobem a l’hora d’analitzar els conjunts de dades i variables de manera combinada, tenint en compte, a més, que corresponen a diferents coordenades d’un espai multidimensional, definit per camps distints (genètic, clínic, nutricional, metabòlic, metabolòmic, etc. i d’altres variables) que reflecteixen, cadascuna amb pautes i lleis particulars, la informació sobre els processos homeostàtics i els equilibris entre salut i malaltia. La determinació de fenotips de salut nutricional (FSN) útils (vegeu més endavant) constitueix un dels majors reptes. BIOMARCADORS NUTRIGENÒMICS Un elevat nombre de revisions ja il·lustren la capacitat d’identificar en edats primerenques determinades sensibilitats de les persones a malalties relacionades amb la dieta, el que podria reforçar (juntament amb l’assessorament dietètic i d’estil de vida, i el coneixement d’interaccions dieta-genotip) els beneficis de la dieta sobre la salut humana i avançar en el coneixement de les bases científiques de la relació entre dieta En nutrigenòmica pretenem descriure el sistema biològic (el funcionament d’una cèl·lula, teixit, sistema biològic en general, o el nostre organisme complet en el cas més ampli que aquí ens interessa) en «la seva totalitat»; en termes de la seva composició de milers de mRNA, proteïnes i metabòlits, i les combinacions de tots ells. Amb això ens agradaria poder descriure «completament» cada sistema homeostàtic, per poder percebre desplaçaments d’aquest sistema, previs a l’aparició d’alteracions o factors de risc que tard o d’hora poden donar lloc a determinades alteracions més definides (malalties o altres fenotips que ens interessin). En aquest sentit, els biomarcadors nutrigenòmics resulten de conjunts de dades característiques de la resposta (a la dieta o a una determinada composició o pauta alimentària) del sistema biològic considerat, indicatius de la derivació del sistema cap a una determinada condició considerada potencialment adversa; per exemple, cap al desenvolupament d’hipertensió. Són ja nombrosos els estudis nutrigenòmics que mostren relació entre els components de la dieta i la salut. Alguns exemples són el paper dels àcids grassos en el desenvolupament d’esteatosi hepàtica o del fetge gras, l’efecte del calci i de l’hemo sobre el risc de càncer de colon, o els efectes de l’oli d’oliva, de l’alcohol, de la vitamina D, etc. És lògic que un perfil complet de molts biomarcadors, basats en centenars o milers de paràmetres, representi més fidelment l’estat de salut o benestar que no els actuals i escassos biomarcadors, disponibles rutinàriament. Entre les dificultats actuals que cal superar hi ha el fet que, de moment, es requereix una quantitat relativament gran de mostra per a aïllar prou material per fer les anàlisis i el fet que, en general, l’accés a teixits humans (descomptant sang, orina i altres fluids i descamacions, practicables fàcilment) és limitat. Si bé les biòpsies de pell, múscul i teixit adipós són relativament accessibles i poden arribar a ser-ho de manera senzilla, els diferents tipus de cèl·lules sanguínies ofereixen les més interessants possibilitats a priori. En el futur ens espera el desenvolupament de noves tècniques d’anàlisi no invasives. És possible determinar perfils tissulars característics i identificar gens candidats, per exemple en relació amb l’obesitat, o bé marcadors d’efectes de nutrients, com la vitamina D, o identificar diversos agents i contaminants d’interès en seguretat alimentària. S’han descrit patrons específics d’expressió genètica en cèl·lules sanguínies associades a malalties com ara tumors pulmonars o leucèmia que poden servir com a marcadors de malaltia, però està pendent la qüestió sobre els biomarcadors de premalaltia, previs a l’aparició dels factors i signes de risc tradicionalment considerats. |
||
 © M. Lorenzo L’exposició al tabac o l’exercici físic poden considerar-se factors menors, tot i la seua importància, si els comparem amb l’exposició continuada als aliments al llarg de la nostra vida. |
«Un objectiu últim de la nutrigenòmica és el desenvolupament d’aliments que s’ajustin a les conveniències de salut de persones individuals» | |
|
Fins ara, i tot i que moltes experiències no han estat publicades i per tant no s’han pogut compartir (un problema a solucionar per la comunitat científica, particularment pels editors), pot deduir-se que la variabilitat interindividual observada és elevada, si bé és cert que amb les dades que s’obtenen és factible establir concordances; per exemple, ja s’obtenen resultats bastant reproductibles de cada individu si s’ajusten bé les condicions, ritmes diaris, estacionals, formes d’alimentació, etc. D’aquesta manera els perfils nutrigenòmics es presenten com una estratègia molt prometedora per a avançar en el coneixement de la resposta fenotípica a les intervencions nutricionals. ENTORN DE LES RECOMANACIONS EN L’ALIMENTACIÓ ACTUAL En general, val la pena notar que l’exposició al tabac o a altres toxines, o l’exercici físic, que sabem que són agents molt capaços de determinar la nostra salut, són factors que poden considerar-se menors comparats amb la nostra exposició continuada als aliments al llarg de tota la vida; els aliments constitueixen el principal factor mediambiental que posa a prova el nostre organisme. Els referents de qualitat en alimentació han canviat i les demandes del consumidor canvien de manera accelerada. Mentre que durant el segle passat les preocupacions es van centrar primer a assegurar la disponibilitat d’aliments bàsics i, posteriorment, a assegurar-se que fossin innocus, i en nutrició prevenir les malalties carencials, assegurant un subministrament adequat de macronutrients i components essencials, avui la nostra societat es concentra més a afrontar (i de manera clau a través de l’alimentació) les denominades malalties cròniques del nostre temps: malalties cardiovasculars, diabetis, obesitat, diversos tipus de càncer, osteoporosi i malalties autoimmunes. El consumidor en les nostres societats desenvolupades, amb un creixement de la capacitat adquisitiva, no es conforma a exigir que els aliments siguin segurs, que la disponibilitat estigui assegurada i que siguin innocus, i no s’acontentarà amb el que tradicionalment s’esperava dels aliments (energia, nutrients per a la construcció o renovació de les nostres estructures corporals, que ens satisfacin la fam i el plaer de menjar, el seu paper en les relacions socials i en les tradicions, que la producció sigui respectuosa amb el benestar animal i amb el medi ambient). A més de tot això, espera que els aliments li proporcionin més salut i benestar (aliments funcionals). La legislació alimentària europea s’adapta als nous escenaris. A finals de 2006 concloïa a Europa l’ampli debat de la proposta sobre Declaracions Nutricionals i Declaracions de Salut en els Aliments (vegeu el Reglament (CE) núm. 1924/2006 relatiu a les declaracions nutricionals i de propietats saludables en els aliments, Diari Oficial de la Unió Europea L 12, 3-18, de 18 de gener de 2007), una iniciativa de la CE sobre les normes que han de regir uniformement en tots els estats membre per reduir la situació actual d’anarquia en la publicitat sobre aliments-salut (cada país feia la seva pròpia interpretació –sovint oscil·lant– de les propietats o beneficis que poden ser o no al·legats en etiquetes, anuncis publicitaris, etc.), que afavoreix la proliferació de publicitat enganyosa, no sustentada en evidències científiques, i afecta tots els consumidors, incloent-hi la població infantil i juvenil. La nova legislació inclou prohibicions d’al·legacions nutricionals o de salut per a aquells aliments que no tinguin un «perfil nutricional» mínimament saludable (aliments rics en greix saturat, sal, etc.), perfil que ha de ser avaluat de manera independent pel panell de nutrició de l’EFSA (European Food Safety Authority). La idea subjacent és que només s’han de permetre les al·legacions de salut provades científicament i, atès que les al·legacions de salut poden estimular el consum d’aquells aliments que en gaudeixin, no sembla raonable que les al·legacions beneficiïn el consum d’aliments amb un perfil nutricional inadequat. Pot ser que, de moment, sigui políticament més correcte continuar dient que no hi ha aliments bons o dolents (perquè és cert que els efectes depenen de les dosis); però el coneixement científic aporta cada dia més evidència que hi ha diferències molt marcades entre els diferents aliments, i no han de ser ignorades. A més, encara que avui dia ja s’han implantat recomanacions dietètiques per a millorar la salut i disminuir el risc de ECV, càncer, hipertensió, diabetis tipus 2, obesitat, i altres malalties cròniques, amb beneficis provats segons les estadístiques, la veritat és que aquestes recomanacions s’han establert sobre la base de la població general i no de manera individual. Sense desconsiderar els beneficis en general, les diferències tan dràstiques en les respostes de cada persona individual a una determinada dieta posen de manifest les limitacions d’aquestes recomanacions generals, i també que coneixem els mecanismes de manera molt limitada. En paral·lel a una millor formació i informació nutricional del consumidor, els canvis aniran donant pas des d’una posició «paternalista» de l’administració (amb recomanacions generals per a menjar de manera saludable i variada en general i que asseguren –amb fortificació d’aliments si es considera necessari– l’evitació de carències) fins a una situació que propicia més l’elecció, fonamentada, del consumidor d’aquells aliments i ingredients de la dieta que més li convinguin a la seva salut i benestar. ALIMENTS FUNCIONALS I DIETES INTEL·LIGENTS La capitalització dels coneixements sobre nous beneficis per a la salut i el benestar que es van delimitant és la base per al desenvolupament dels anomenats aliments funcionals. Certs components alimentaris i dietes resulten ser capaços de decantar adaptacions del nostre organisme, atès que afecten el manteniment d’equilibris homeostàtics determinants de les condicions de salut i benestar, en el sentit d’afavorir o prevenir determinades malalties cròniques o altres condicions d’interès. |
||
 © M. Lorenzo Avui dia, els consumidors no es conformen amb la disponibilitat i seguretat dels aliments, volen que a més els proporcionen salut i benestar. |
«La nutrigenòmica permetrà millorar tant la seguretat com l’eficàcia dels aliments» | |
|
La nutrigenòmica permetrà millorar tant la seguretat com l’eficàcia dels aliments perquè proporcionarà un nivell de comprensió més precís de les influències dels aliments i els seus components en els nostres sistemes homeostàtics, amb noves aproximacions per a la determinació d’efectes, beneficiosos o adversos, en fases precoces; per exemple, anticipadament al desenvolupament d’una malaltia. Això inclou l’alimentació dirigida a subgrups de població i fins i tot la nutrició personalitzada, dietes intel·ligents dissenyades d’acord amb les demandes específiques de genotips individuals i de la seva història. Per exemple, es pot pensar (i ja ha aparegut propaganda comercial agosarada que se n’ha fet ressò) que a partir d’una petita mostra de sang o a partir d’un altre tipus de mostra fàcilment obtenible, es pot efectuar (i es podrà fer fàcilment, amb rapidesa i a un cost acceptable) una prospecció nutrigenòmica (transcriptòmica, proteòmica, metabolòmica), contrastar els resultats amb els del DNA de l’individu (igualment mesurable) i així poder obtenir una selecció intel·ligent de dietes variades, saludables (recomanables, per exemple, per als propers vint dies), equilibrades en macronutrients i micronutrients i amb la càrrega òptima de compostos bioactius, a més de gustoses. Les principals dificultats que haurien de superar-se tenen l’arrel en la mateixa complexitat dels aliments i pràctiques alimentàries, i en la complexitat també dels nostres sistemes metabòlics i les seves subtils interregulacions, així mateix cal tenir en compte els problemes de percepció social, qüestions ètiques i implicacions econòmiques i socials. Actualment s’està acumulant molta informació; el genotipatge dels individus que participen en estudis dietètics d’intervenció s’ha incorporat a molts dels protocols d’estudi a gran escala; els estudis a gran escala observacionals de les relacions entre dieta i malaltia també van incorporant la investigació de les interaccions entre dieta i genotip. El concepte de nutrició individualitzada, el consell dietètic adaptat a cada individu, ha capturat la imaginació dels investigadors de la nutrició, tant en salut pública com en terapèutica. Però hem dit imaginació i no aplicabilitat i comercialització immediata. Les oportunitats per a la indústria alimentària a l’hora de proporcionar aliments funcionals i productes específics adaptats a subgrups segons genotips específics també han estat reconegudes, i el dogma general que diu que en una dieta «hi caben o encaixen tots els aliments» ha començat a qüestionar-se. Els atractius que ofereix la nutrició personalitzada, així com les implicacions ètiques i socials que presenta, han atret l’atenció dels mitjans generals de comunicació. Tenint en compte les tendències actuals i la disponibilitat ja de plats preparats de tots els tipus i característiques, amb sabors i olors que reflecteixen fidelment els orígens tradicionals, reconeixedors, hauríem d’afrontar el coneixement de la resposta nutrigenòmica a aquests preparats tan complexos, i no només el coneixement del perfil nutrigenòmic de nutrients o components individuals dels aliments. |
||
|
EPIGENÈTICA I DESENVOLUPAMENT DE MALALTIES L’alimentació, particularment durant les etapes primerenques del desenvolupament, pot condicionar fortament la nostra salut al llarg de la vida. Així, l’alimentació de la futura mare constitueix un factor primordial –més del que anteriorment es pensava– en el desenvolupament del nen, especialment pel que concerneix a la seva futura salut i resistència a malalties. Actualment se sap que algunes malalties que es presenten en l’edat adulta, i que eren atribuïdes a un estil de vida malsà o a factors genètics, són el resultat directe de l’entorn uterí durant l’embaràs o de l’alimentació durant la lactància. Nombrosos estudis epidemiològics amplis realitzats en els últims vint anys han demostrat que les condicions nutricionals durant etapes crítiques del desenvolupament, especialment la gestació i període postnatal primerenc (principalment la lactància) afecten la susceptibilitat a patir determinades malalties en edat adulta, entre elles malaltia cardiovascular, obesitat, diabetis tipus ii, osteoporosi i altres problemes i alteracions. Els mecanismes biològics subjacents no són ben coneguts, però, tal com es dedueix d’estudis realitzats en models animals o in vitro, les diferències són causades per la interacció entre components dels aliments (o altres factors ambientals) amb els nostres cromosomes, que condueixen a un imprinting o programació d’esquemes metabòlics particulars en els individus, incloent-hi canvis permanents (epigenètica) que es transmeten en la multiplicació cel·lular i que poden conferir una susceptibilitat diferent a patir alteracions en edat adulta. Els estudis realitzats en els últims anys en el nostre laboratori ens han permès descriure una nova funció per a una d’aquestes proteïnes que es troba de manera natural en la llet materna humana i que no està present en fórmules infantils: la leptina, la nova funció de la qual durant la lactància és conferir protecció enfront del desenvolupament de sobrepès o obesitat (i altres complicacions mèdiques associades) en l’edat adulta. El terme imprinting, o programació metabòlica, descriu els processos pels quals les cèl·lules adquireixen una certa memòria biològica per a manejar influències externes, i que pot ser transmesa a la descendència cel·lular. Implica que un estímul que operi en un període crític o sensible del desenvolupament (que podríem considerar com una finestra específica de sensibilitat) pot donar lloc a efectes persistents o permanents sobre l’estructura o la funció de l’organisme. L’epigenètica es refereix a aquestes alteracions estables en l’expressió gènica que no impliquen mutacions del DNA en si mateix però que confereixen un patró particular d’expressió gènica que es manté estable al llarg de les divisions cel·lulars. S’ha considerat que la metilació és la principal base epigenètica per a la programació metabòlica; les histones, proteïnes associades íntimament al DNA, poden contribuir a aquests canvis epigenètics i la metilació del DNA estaria relacionada amb la modificació d’histones. Encara que la leptina és produïda principalment pel teixit adipós, aquesta hormona també la produeixen altres teixits com la placenta i el múscul esquelètic i, en particular, la produeixen l’estómac i l’epiteli mamari, i és present de manera natural en la llet materna. Les concentracions de leptina en llet materna humana varien perceptiblement entre unes mares i altres, però el que és molt significatiu és que les llets artificials o de fórmula per a bebés no contenen leptina com a ingredient La llet materna és pràcticament l’únic aliment ingerit durant els primers mesos de la vida en nens alimentats exclusivament amb llet materna i, comparat amb la llet de fórmula, els resultats de diversos estudis epidemiològics apuntaven que la lactància materna confereix una major protecció enfront de l’obesitat i altres alteracions en edat adulta. S’ha mostrat també una correlació inversa entre la durada de l’alletament i el risc de sobrepès en l’edat adulta. Els receptors de leptina són presents en l’estómac humà i en l’aparell gastrointestinal del ratolí, i la leptina és capaç d’activar de manera directa les neurones aferents vagals que s’originen en les parets gàstriques i intestinals i acaben en el nucli del tracte solitari, proporcionant una informació ràpida al cervell. D’altra banda, es va descriure que la leptina subministrada amb la llet, o administrada per via oral en solució aquosa, podia ser absorbida per l’estómac immadur de rates lactants i passar a la circulació sanguínia. A més, la leptina subministrada amb la llet materna apareixia com la font principal de leptina en l’estómac durant la primera meitat de la lactància. Aquesta leptina exògena podria exercir efectes biològics en nounats, en un període en el qual tant el teixit adipós com els sistemes reguladors de la gana són immadurs. Així, ens plantejarem la hipòtesi que la leptina podria ser el compost específic (o almenys un d’ells) responsable dels efectes beneficiosos de la llet materna en la protecció contra l’obesitat en edats més avançades. Per provar-la, vam suplementar la lactància en rates amb dosis fisiològiques de leptina per via oral i observàrem els possibles efectes que això produïa sobre la regulació del pes corporal en l’edat adulta. Els resultats van demostrar que els animals que havien pres leptina durant la lactància presentaven en edats adultes menor guany de pes i menor acumulació de greix, i ingerien menys calories que els seus controls no tractats, tant sota condicions de dieta estàndard com en condicions de dieta rica en greix. La conclusió global dels estudis va ser que la suplementació amb quantitats fisiològiques de leptina durant la lactància protegeix enfront de l’acumulació de greix en l’edat adulta i que aquests animals semblen més sensibles a la regulació de la ingesta per leptina, a curt i a llarg termini. Així doncs, la leptina representa un paper important en les primeres etapes de la vida, com a component de la llet materna, en la prevenció de l’obesitat en edats més avançades. Altres estudis realitzats han confirmat aquests resultats i d’altres sobre la susceptibilitat a altres malalties relacionades amb l’obesitat. També, els resultats obtinguts en mares no obeses i en els seus fills fins als dos anys d’edat, en humans, indiquen que la ingesta de més leptina en la llet materna proporciona certa protecció als nens contra un augment excessiu del pes. La seqüenciació del genoma humà ens ha revelat no només un nombre de gens humans menor que l’esperat (les últimes estimacions el calculen en prop de 24.000 gens), sinó també la gran heterogeneïtat genètica de les poblacions humanes, una variabilitat genètica entre humans molt major que la prèviament suposada: es calcula que el genoma humà alberga uns deu milions de polimorfismes. A això s’uneix la complexitat derivada de les prolixes interaccions entre els gens i la seva regulació, així com la variabilitat epigenètica, l’«imprinting metabòlic»: la nostra història de la manera com mengem, com sentim, les influències de l’entorn, etc., va quedant gravada de manera permanent. Tot això promou un canvi profund en el pensament humà sobre com aquesta informació pot ser explotada òptimament, en benefici de la salut i el benestar. El paper dels polimorfismes genètics en la determinació de respostes heterogènies a exposicions ambientals com ara medecines, activitat física i dieta, és ja evident. La indústria farmacèutica ja explora aquesta oportunitat a través del desenvolupament de la farmacogenòmica i, de la mateixa manera, el sector de l’alimentació haurà d’implicar-se en el desenvolupament de la nutrigenòmica. L’oportunitat de desenvolupar comercialment tests nutrigenòmics o nutrigenètics sembla real, de fet hi ha un sector creixent de consumidors que ja els demanda i que és capaç d’assumir els costos, a pesar dels dubtes existents; per això els tests als quals pot ja acudir directament el consumidor són accessibles de manera creixent, tot i que considerem que aquesta comercialització encara és prematura. BIBLIOGRAFIA Andreu Palou. Laboratori de Biologia Molecular, Nutrició i Biotecnologia. Universitat de les Illes Balears. |
«Actualment se sap que algunes malalties que es presenten en l’edat adulta són el resultat directe de l’entorn uterí durant l’embaràs o de l’alimentació durant la lactància» |
|