| {rokbox text=||}images/stories/numeros/METODE_57/118b-57.jpg{/rokbox} |
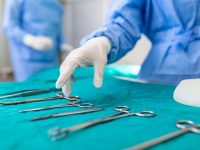
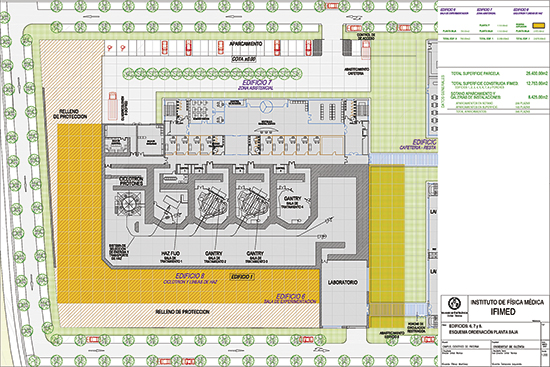
A l’esquerra, projecte de l’Institut de Física Mèdica (IFIMED). En la fotografia de dalt es mostra un ciclotró de protons obert (cortesia de IBA). Les dimensions externes són 5 m de diàmetre i 2 m d’alçada. |
|
|
Small Accelerators for Medical Application. Els acceleradors de partícules van ser principalment concebuts, dissenyats i utilitzats per a la investigació en física nuclear i física d’altes energies. Però, en l’actualitat, s’utilitzen cada vegada més en camps tan diversos com la ciència de materials, la biologia, la medicina o l’arqueologia. En el món hi ha més de 8.000 petits acceleradors de baixes energies (fins a uns pocs MeV per unitat de massa per a ions lleugers) dedicats a implantació d’ions, espectroscòpia de masses, emissió de raigs X induïts per protons (PIXE), etc. Hi ha prop de 250 ciclotrons dedicats a la producció d’isòtops, tant per a tractaments tumorals com per a usar-los en la tomografia per emissió de positrons. Majoritàriament acceleren protons o deuteris fins a 30 MeV d’energia. Hi ha també uns 10.000 acceleradors lineals d’electrons (linacs) que produeixen fotons d’alta energia per a radioteràpia. Hi ha prop de 30 acceleradors, entre instal·lacions d’investigació i hospitalàries, que funcionen per damunt de 60 MeV, per a radioteràpia amb ions, perquè permeten una adaptació precisa al tumor de la radiació en maximitzar-ne el control i reduir, al mateix temps, el risc d’efectes secundaris. Tots aquests petits acceleradors han utilitzat i continuen utilitzant la R+D sorgida de la construcció de grans acceleradors, l’objectiu principal dels quals és l’estudi de l’estructura de la matèria amb energies i resolucions cada vegada majors. En aquest article descriurem els principals aspectes d’un tipus d’aquests petits acceleradors dedicats a l’hadronteràpia, és a dir, a accelerar protons i ions lleugers per al tractament de tumors. Els primers acceleradors El 1945 W. Hansen va construir a la Universitat de Stanford un accelerador lineal de tot just 1 m de longitud, que accelerava electrons a 4,5 MeV. Funcionava a una freqüència de 3 GHz, prèviament inimaginable, freqüència possible gràcies al klystron polsat d’alta potència, inventat pels germans Varian i desenvolupat per als radars usats en la Segona Guerra Mundial. Hansen pensava a impulsar la investigació en física nuclear, però el seu invent va tenir un enorme impacte en medicina. El mateix any R. Wilson calculava, per encàrrec de E. Lawrence, la grossària del blindatge necessari per a un ciclotró de 150 MeV que s’anava a instal·lar a la Universitat de Harvard. El comportament de la radiació en travessar uns pocs centímetres de plom va ser per a ell una gran sorpresa. L’estret «pic de Bragg» al final del recorregut li va portar a suggerir, en un ara famós article, l’ús de protons per a irradiar tumors, ja que es preservarien així, molt més que no amb raigs X, els teixits sans travessats, contigus i situats més profundament. No obstant això, l’article va tenir poc d’impacte en la comunitat mèdica i va caldre esperar uns deu anys abans que no es tractaren els primers pacients, a Berkeley i a Harvard, amb feixos de protons produïts en acceleradors, dedicats en un principi a la física nuclear. Finalment, a Loma Linda, centre mèdic universitari de Califòrnia, es va construir el primer sincrotró de protons dedicat íntegrament a la protonteràpia. El 1993 es va començar a irradiar pacients en tres sales. No és per casualitat que el ciclotró de Loma Linda es construïra a Fermilab, el laboratori de física de partícules que va crear Wilson i que va dirigir fins al 1987. L’energia de l’accelerador està determinada per la profunditat de penetració en el cos humà: amb protons de 200 MeV s’arriba a uns 27 cm. Nous centres de tractament Des de 1993, uns 15.000 pacients en tot el món han estat tractats amb protons i, en aquest temps, s’ha mostrat que tenen els mateixos efectes biològics i clínics que els raigs X produïts per linacs d’uns pocs MeV. A començament de 2007 es va superar la fita de 50.000 pacients, irradiats en dotze laboratoris de física subatòmica i en més de deu centres de protonteràpia situats en hospitals. Deu centres més estan en construcció o en projecte en tot el món, perquè ja hi ha cinc empreses que proporcionen aquestes instal·lacions claus en mà. Aquest nombre ja justifica per ell mateix l’afirmació que la protonteràpia està en plena expansió. En aquests centres de protonteràpia s’utilitza o un ciclotró o un sincrotró (d’uns 5 o 7 m de diàmetre respectivament), ja que ambdós acceleradors tenen la fiabilitat necessària per a funcionar en un entorn hospitalari. En l’actualitat hi ha cinc centres als EUA, quatre al Japó, dos a la Xina, un a Suïssa i un a Alemanya. França, Corea i Itàlia també disposen d’un centre, bé ja en funcionament o bé finançat. A Espanya hi ha un centre, l’IFIMED (Institut de Física Mèdica), que es preveu que entre en funcionament cap al 2012. Veiem l’estructura d’un d’aquests acceleradors. Hi ha dos components principals: el sistema de producció d’ions i el sistema de distribució del feix. El primer produeix el feix de protons i el dirigeix a la sala apropiada, de tractament o d’experimentació, mitjançant un sistema de transport. Inclou el ciclotró i els sistemes de selecció d’energia i de transport del feix. El ciclotró de protons té una energia fixa de 230 MeV, i mitjançant un reductor variable d’energia s’obté l’energia necessària per a cada tractament (de 230 a 70 MeV). En un sincrotró no és necessària aquesta operació, perquè l’energia del feix és variable. Un sistema de transport connecta la zona de selecció d’energia amb el punt d’entrada de cada sala i permet proporcionar un feix centrat, amb les propietats adequades per a la zona experimental o de tractament. |
«Hi ha prop de 30 acceleradors que permeten una adaptació precisa al tumor de la radiació en maximitzar-ne el control i reduir, al mateix temps, el risc d’efectes secundaris» |
|
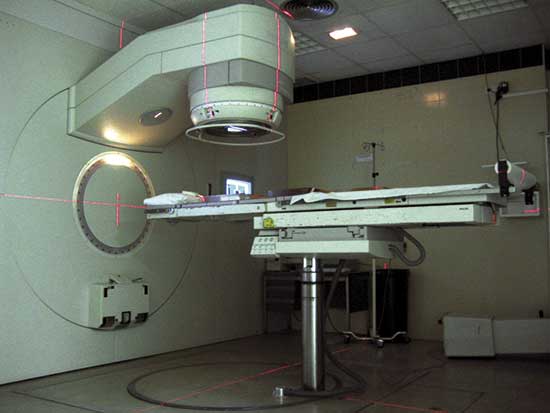
Accelerador lineal d’electrons de l’Hospital Universitari La Fe (València). Pot girar al voltant de la llitera, la posicio de la qual s’ajusta exactament amb un sistema de làsers (llums vermelles). |
«L’objectiu final de qualsevol sistema d’aplicació és produir un feix que abaste les dimensions adequades per al tractament» |
|
|
El sistema de distribució, situat en cada sala de tractament, dirigeix el feix de protons al lloc on es troba el pacient. Proporciona una distribució adequada de dosi, tant en sentit longitudinal com transversal. Conté un gantry, que és una estructura de 10 m d’altura capaç de girar ± 190º al voltant del pacient i de grandària adequada per a irradiar el pacient des de qualsevol angle, encara que també hi ha sales de feix fix a les quals aquest arriba horitzontalment. En tot cas, hi ha dispositius per a variar la posició del pacient segons sis graus de llibertat, que assoleixen una precisió de ± 0,5 mm. En la part final del sistema d’aplicació se situa un dispositiu amb l’equip necessari per a preparar i mesurar les propietats del feix i subministrar-lo de distintes maneres: dispersió simple o doble, escombratge uniforme o en pinzell. L’objectiu final de qualsevol sistema d’aplicació és produir un feix que abaste les dimensions transversal i longitudinal adequades a cada tractament. A més, tot el conjunt disposa d’un control global de seguretat, amb dispositius i programes redundants per garantir un alt nivell de seguretat, tant per al pacient com per al personal clínic, científic o tècnic. Quasi al mateix temps en què van començar a utilitzar-se protons en el tractament contra el càncer, es va iniciar l’ús d’ions pesants, és a dir, àtoms completament ionitzats. Si aquests ions són interessants és perquè, com que tenen major massa i càrrega que els del protó, poden dipositar una major energia per unitat de longitud de camí recorregut o transferència lineal d’energia, la qual cosa es tradueix en major eficiència al final de la corba de Bragg. És, en efecte, la major ionització el que produeix major efectivitat. El principal objectiu de l’atac amb radiacions és el DNA dins del nucli de les cèl·lules, o més precisament, la seua capacitat de reparació: les dosis locals molt altes produeixen un col·lapse d’aquest sistema. La dosi concentrada és més efectiva en comparació amb una radiació disseminada, i augmenta l’eficàcia biològica efectiva. Des del 2000 han estat tractats amb ions de carboni més de 350 pacients en el projecte pilot del laboratori de física nuclear GSI, a Darmstadt, Alemanya, i uns 3.500 pacients han estat tractats des de 1994 en l’accelerador mèdic d’ions pesants de Chiba, Japó. Els resultats clínics obtinguts en aquests laboratoris confirmen les prediccions radiobiològiques: que els ions de carboni tenen una eficàcia biològica major que els protons, perquè produeixen una ionització 24 vegades superior. El tractament amb ions de carboni és adequat per a tumors de creixement lent, que són resistents als protons i als fotons. Però l’ús d’ions de carboni presenta una complexitat molt major que l’ús de protons, no sols pel que fa al mateix accelerador sinó, especialment, al sistema d’aplicació i als gantries. Mentre que amb protons de 200 MeV s’assoleixen tumors a 27 cm dins del cos, són necessaris ions de carboni d’uns 4.800 MeV (400 MeV/u) per a assolir aquesta profunditat. En els últims cinc anys, s’han fet a Europa passos importants cap al desenvolupament i construcció de centres duals, que puguen utilitzar tant protons com ions de carboni, basats en sincrotrons. Però la companyia belga IBA està desenvolupant un prototip d’un ciclotró superconductor de 6 metres de diàmetre capaç d’accelerar ions de carboni fins a l’energia requerida de 400 Mev/u. Els futurs desenvolupaments, la R+D més interessant capaç d’introduir noves i més destacades millores al camp de l’hadronteràpia, estan relacionats en sentit ampli amb els avenços en la tecnologia d’acceleradors. Ugo Amaldi. Università degli Studi di Milano – Bicocca i Fondazione TERA. |
Petits acceleradors de partícules per aplicacions mèdiques
Pequeños aceleradores de partículas