|
Radiotherapy and its Recent Progress. La paraula radioteràpia significa «tractament amb radiacions», però, en medicina, quan es parla de radioteràpia es fa referència al tractament amb radiacions ionitzants. Només quan les radiacions posseeixen l’energia suficient per a produir ionitzacions en els teixits que travessen tindran la capacitat destructiva cel·lular que requereix el tractament dels tumors malignes. Encara que puga utilitzar-se excepcionalment en alguns processos benignes, l’aplicació fonamental de la radioteràpia és el tractament del càncer. El descobriment dels raigs X per Röntgen el 1895 i de la radioactivitat natural per Becquerel el 1896, completat amb l’aïllament del radi pel matrimoni Curie el 1898, constitueixen les fites històriques que marquen el punt d’arrancada de la utilització de les radiacions ionitzants amb fins terapèutics. Des del seu inici, es distingeixen dues modalitats: la radioteràpia externa, que utilitza equips productors de radiacions que emeten els feixos a determinada distància del pacient, i la radioteràpia interna, que utilitza fonts radioactives que es col·loquen en el tumor mateix. En el tractament extern, els aparells de raigs X van donar pas a generadors més potents com el betatró en els anys quaranta i, ja en els cinquanta, la denominada bomba de cobalt i l’accelerador lineal, i és aquest últim el que serveix de base a la radioteràpia actual. La radioteràpia interna, que denominem braquiteràpia o curieteràpia en honor del matrimoni Curie, es realitza introduint les fonts radioactives en l’organisme, en el tumor mateix o als seus voltants. De l’ús exclusiu de radi (226Ra) en els seus començaments, es va passar a utilitzar altres isòtops radioactius com el cesi (137Cs), iridi (192Ir), or (198Au), estronci (90Sr), iode (131I), ruteni (106Ru), etc., que es presenten en forma de tubs, agulles, fils o llavors. La característica fonamental de les radiacions utilitzades per combatre el càncer és la de produir ionitzacions en el medi biològic que travessen. Les radiacions ionitzants arranquen electrons dels àtoms de molt diverses molècules; es formen aleshores radicals lliures que són molt actius i que són responsables, per les reaccions químiques que provoquen, de les lesions biològiques cellulars (efecte indirecte). Aquestes radiacions poden també produir lesions cel·lulars de manera directa. Les dites lesions afecten fonamentalment molècules complexes, bàsiques per a la vida i reproducció cel·lulars, com és el DNA. Aquestes alteracions es tradueixen en ruptures, translocacions o inversions dels cromosomes amb el consegüent compromís de la viabilitat cel·lular. La radioteràpia és un dels tractaments bàsics i tradicionals del càncer. Té una acció local, com la cirurgia, a la qual amb molta freqüència s’associa, i és altament efectiva en el control dels tumors primaris. Però només sol tenir un efecte pal·liatiu en el càncer estès o disseminat (amb metàstasi), on només els tractaments que actuen sobre tot l’organisme, com ara la quimioteràpia i la immunoteràpia, poden tenir una finalitat curativa. La radioteràpia s’utilitza en prop de la meitat dels pacients amb càncer. Segons el Cancer Research Working Party, dels pacients amb càncer, es cura un 50% i la radioteràpia intervé en aquesta curació de manera decisiva i exclusiva en un 12% d’ells i associada a altres tractaments (cirurgia i quimioteràpia) en un 6%. Així, doncs, en el 18% dels càncers la radioteràpia representa un paper fonamental. L’ús de la radioteràpia està indicat en nombrosos tumors en funció de la localització i extensió que presenten, per la qual cosa cal distingir els grups següents: a) Tumors tributaris de radioteràpia exclusiva o associada a una cirurgia que preserva l’òrgan on assenta el tumor, com ara càncers de llavi, llengua, cordes vocals, pròstata, mamella… b) Tumors inoperables per la localització, com els del tronc cerebral o la nasofaringe. c) Tumors inoperables per l’excessiva extensió, com ara càncers de coll d’úter, pulmó, esòfag…, localment avançats. d) Tumors inoperables per mal estat general de pacient a causa de patologies associades. També està indicada la radioteràpia com a tractament pal·liatiu davant metàstasis que produesquen símptomes, com les òssies o les cerebrals. Avenços en radioteràpia La finalitat de la radioteràpia en el càncer ha estat, des dels seus començaments, administrar una dosi de radiacions ionitzants en el tumor prou elevada perquè el destruesca, limitant al mateix temps la dosi en els teixits sans adjacents per no provocar complicacions inacceptables. No obstant això, durant moltes dècades, va ser impossible progressar en aquest sentit donada la dificultat per determinar amb suficient exactitud la localització i extensió precisa dels tumors, com també la rudimentària planificació dosimètrica. Arran de la introducció en els anys vuitanta dels moderns mètodes d’obtenció d’imatges (TAC, RNM, PET…), de planificadors capaços de calcular la distribució de dosis en els teixits amb rapidesa i precisió, i d’acceleradors lineals dirigits per ordinadors i amb sofisticats additaments de conformació dels feixos de radiació, és possible avui dia que la radioteràpia moderna s’aproxime als objectius indicats. Radioteràpia conformada per modulació d’intensitat (IMRT) La radioteràpia conformada és la que administra una alta dosi de radiació en el volum tumoral amb una brusca caiguda de dosi cap als teixits sans peritumorals, en totes les direccions de l’espai, siga quina siga la forma del tumor. Es tracta d’una distribució de dosi que conforma el tumor en tres dimensions (3D). Si utilitzem múltiples camps convergents en el volum tumoral adaptats a la forma que aquest té en la projecció de cada feix, obtindrem una conformació acceptable de la dosi. No obstant això, davant tumors d’estructura irregular que envolten estructures sanes, només pot obtenir-se una conformació excel·lent utilitzant feixos de radiació d’intensitat modulada, i amb aquest objectiu s’usen col·limadors multilàmines acoblats als acceleradors lineals. Aquests col·limadors disposen de prop d’un centenar de làmines, el moviment independent dels quals, guiat per un programa d’ordinador, durant la irradiació, fa possible la desitjada conformació de la dosi. |
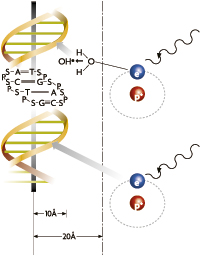
Mecanismes de lesió cel·lular per radiacions ionitzants. Es mostra esquemàticament l’efecte indirecte per radicals lliures de l’aigua cel·lular, i l‘efecte directe sobre macromolècules (DNA). «Només quan les radiacions posseeixen l’energia suficient per a produir ionitzacions en els teixits que travessen tindran la capacitat destructiva cel·lular que requereix el tractament dels tumors malignes»
|
|
 Radioteràpia d’intensitat modulada (IMRT) mitjançant accelerador lineal amb col·limador multilàmines. |
«La radioteràpia té una acció local i és altament efectiva en el control dels tumors primaris» |
|
|
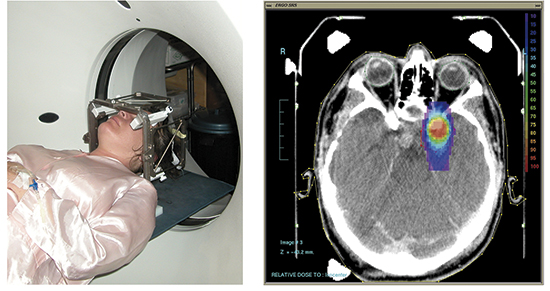
IMRT per tomoteràpia Un sistema modern d’IMRT utilitza un accelerador lineal muntat en un equip semblant a una TAC, rotant el capçal de l’accelerador lineal al voltant del pacient. Un col·limador multilàmines especial estreteix el feix en la direcció longitudinal del pacient, modificant les làmines mentre el capçal gira 360º. Després de cada gir complet es produeix un desplaçament de la taula per a irradiar, de la mateixa manera, la següent secció corporal. La dita forma d’irradiació segmentada per talls s’ha substituït últimament per una forma més contínua o helicoïdal. El sistema rotatori facilita la realització d’una TAC diagnòstica abans de cada sessió de radioteràpia, i això permet ajustar les dosis davant possibles desplaçaments del tumor al llarg dels dies de tractament. Es tracta d’un petit accelerador lineal compacte de 6 MeV, muntat sobre un braç robòtic industrial, que té la capacitat de moure’s amb total llibertat i gran exactitud, i, doncs, pot dirigir feixos molt fins de radiació cap al volum tumoral des de qualsevol punt de l’espai i amb qualsevol orientació. Radiocirurgia Es tracta d’un altre avenç tecnològic, dirigit fonamentalment al tractament de lesions cerebrals de dimensió reduïda. Es va denominar així perquè es tractava d’un procediment ablatiu, encara que incruent, de lesions petites, perfectament localitzades i ben definides, que es realitza en una única sessió, la qual cosa fa que s’assemble a un acte quirúrgic. La tècnica consisteix a dirigir amb gran exactitud feixos fins de radiació que parteixen d’una font externa, a través de múltiples portes d’entrada, cap a la lesió cerebral o blanc. Per aquest motiu se n’ha dit també radioteràpia per minifeixos convergents. Aquesta tècnica permet dipositar una dosi de radiació molt elevada al lloc de convergència dels múltiples feixos, que ha de coincidir amb la lesió, mentre que, fora d’ell, la dosi disminueix bruscament. S’aplica en general a lesions inaccessibles quirúrgicament, localitzades en una zona cerebral profunda o en una zona funcionalment important, inferior a uns 3 cm de diàmetre. Per a realitzar el tractament és necessari disposar d’un sistema de localització estereotàxic, adaptat al cap del pacient per mitjà de fixacions rígides, inserides als ossos del crani, que permeta definir les coordenades de qualsevol punt del cervell. La lesió es localitza per mitjà de les modernes tècniques d’imatge com ara TAC, RNM o angiografia digital, realitzades en condicions d’estereotàxia, és a dir, amb les referències del marc o sistema d’immobilització utilitzat. Radioteràpia estereotàxica És una tècnica híbrida entre la radioteràpia cerebral clàssica i la radiocirurgia, en què es combinen els avantatges biològics de la irradiació externa (múltiples sessions) amb la focalització precisa de la radiocirurgia. Utilitza guies d’estereotàxia no invasives, que ofereixen no obstant això una precisió de menys d’1 mm i que es poden col·locar nombroses vegades en el mateix pacient de manera idèntica, cosa que permet fer una irradiació fraccionada tot i mantenir les sofisticades tècniques de múltiples camps focalitzats en el tumor que s’usen en la radiocirurgia. Aquestes guies es fixen per mitjà d’empremtes dentals, taps d’oïdes o ponts nasals que es munten amb rapidesa i es toleren bé sense necessitat d’anestèsia. Vistos els beneficis de la radiocirurgia o de la radioteràpia estereotàxica fraccionada aplicades en lesions cerebrals, no és gens estrany que es pensara també a aplicar aquests principis a lesions localitzades al tronc, a pesar de ser més difícil, fonamentalment a causa de la mobilitat superior de les estructures extracranials. El 1994 es va desenvolupar un sistema estereotàxic corporal consistent en un marc immobilitzador que alberga un matalasset de buit o immobilitzador de poliuretà, així com un additament que, pressionant sobre l’abdomen, obliga a una respiració superficial. Evidentment el marc disposa de senyals i escales que permeten referenciar el sistema de coordenades per a estereotàxia. Amb aquests mètodes es redueix a menys d’1 cm la mobilitat diafragmàtica i s’aconsegueix que els desplaçaments d’estructures del tronc es limiten a pocs mil·límetres. Radioteràpia intraoperatòria (RIO) Va ser ideada ja el 1907 per Beck, cirurgià alemany, que la va aplicar a pacients amb càncer gàstric o de còlon que no aconseguia extirpar en l’acte quirúrgic. En aquells casos va desplaçar el tumor cap a l’obertura quirúrgica i el va sotmetre a una radioteràpia de raigs X. Beck deia que «com que la muntanya no va a Mahoma, Mahoma ha d’anar a la muntanya», és a dir, «com que el tub de radiació no arriba al tumor, el tumor profund ha de desplaçar-se cap al tub». Però no va ser fins als anys seixanta i setanta quan, ja amb equips de radioteràpia de megavoltatge mitjançant acceleradors lineals, es va desenvolupar la moderna RIO. Inicialment es procedeix a la resecció quirúrgica del tumor i, en els casos en què queda malaltia microscòpica o subclínica al llit o les àrees limfàtiques adjacents, s’aplica la RIO. Habitualment per mitjà de feixos d’electrons d’energies que permeten cobrir només el volum blanc, amb la qual cosa es protegeixen els òrgans que es troben a més profunditat i, també, aquells més superficials o adjacents que s’aparten mecànicament. |
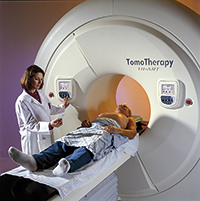
Equip de tomoteràpia, un sistema de radioteràpia que permet veure la posició i la grandària exacta d’un tumor en temps real. |
|
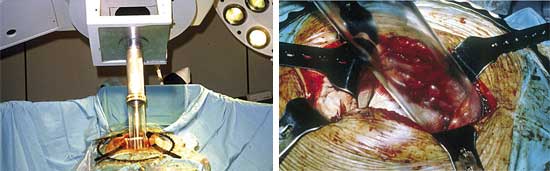 Radioteràpia intraoperatòria en un tumor pelvià. |
«Arran de la introducció en els anys vuitanta dels moderns mètodes d’obtenció d’imatges és possible avui dia que la radioteràpia s’aproxime als objectius indicats» |
|
|
Radioteràpia amb hadrons: protons i ions L’avantatge d’aquest tipus de partícules pesants consisteix en el fet que amb elles es pot obtenir una distribució millor de dosi en els teixits irradiats que l’aconseguida amb raigs X o amb electrons, cosa que permet dipositar una dosi més elevada de radiació en el tumor i menors dosis en els teixits sans pròxims a aquest; es facilita així, per tant, la radioteràpia conformada. Això és possible perquè en la profunditat desitjada, segons l’energia que se’ls proporcione, es dipositarà la major part de la seua energia gràcies a l’acció de frenada que sobre elles exerceixen els electrons del medi. El «pic» que representa aquest dipòsit d’energia i de dosi en el medi irradiat, poc abans que l’hadró s’ature, es denomina pic de Bragg. Així, doncs, hauran d’aplicar-se hadrons d’energies amb un pic de Bragg que coincidesca amb la profunditat a què estiga el tumor. Per davant seu, la gran velocitat dels hadrons farà que es diposite una dosi baixa; a la profunditat del tumor, l’alentiment previ a la detenció d’aquest permetrà alliberar dosis altes; mentre que per darrere d’ell, com que ja s’hauran aturat aquestes partícules, la dosi serà pràcticament nul·la. Per un altre costat la penombra, és a dir, la caiguda de dosi en les vores laterals del feix, és molt nítida, i passa en pocs mil·límetres del 100% de la dosi a valors insignificants. Pel que fa als protons, les primeres experiències en pacients es van iniciar el 1954 en el sincrociclotró de Berkeley, encara que el tractament de pacients es va iniciar amb el ciclotró de Harvard a començament dels seixanta. Després d’haver-hi tractat milers de pacients, es van establir en els anys noranta les indicacions i directrius de la radioteràpia amb protons. Els resultats favorables de les experiències de Harvard van impulsar altres estats americans i altres països a iniciar el tractament de tumors amb protons obtinguts en ciclotrons i sincrotrons dedicats a la investigació física. Avui dia funcionen una vintena de centres de protonteràpia, quasi tots ubicats a l’Amèrica del Nord, Europa i Japó. A més, està prevista la instal·lació del primer centre espanyol de protonteràpia a València. Les característiques físiques de distribució de dosi en els teixits irradiats, que hem descrit anteriorment, faran especialment indicada aquesta radioteràpia en la destrucció de neoplàsies que requeresquen una dosi elevada i que es troben prop d’estructures sanes especialment sensibles a les radiacions, la lesió de les quals podria comportar seqüeles greus. |
||
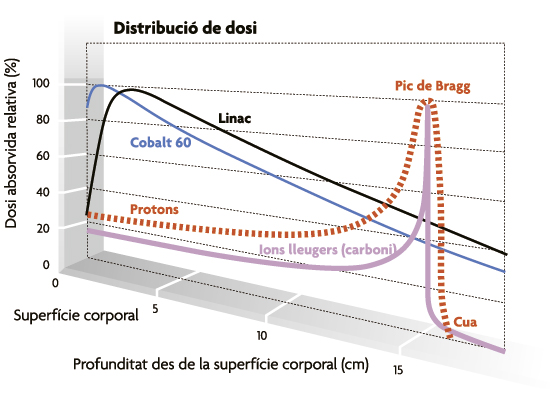 
En la figura superior es mostren les distribucions de dosi obtingudes amb raigs X (Cobalt 60), electrons (Linac), protons i ions lleugers. En la figura inferior es mostra la distribució de dosi en profunditat per a un feix de protons. L’elevat dipòsit d’energia en profunditat es correspon amb el denominat «pic de Bragg». |
«Els ions afegeixen a l’avantatjosa distribució de dosi una major densitat d’ionització en els teixits que travessen, que es tradueix en una major eficàcia biològica en determinats tumors» |
|
|
Els ions, especialment els de carboni i neó, afegeixen a l’avantatjosa distribució de dosi ja descrita, a causa del pic de Bragg, una major densitat d’ionització en els teixits que travessen, que es tradueix en major eficàcia biològica en determinats tumors. Les primeres experiències en el món es van realitzar, al mateix temps que la dels protons, a Berkeley i, encara que el 1993 es van suspendre les seues activitats clíniques, les experiències prossegueixen en altres centres, entre els quals destaquem el centre hospitalari dedicat a la radioteràpia amb ions construït a Chiba (Japó) i el GSI de Darmstadt (Alemanya), les informacions del qual seran crucials en el desenvolupament d’aquesta nova modalitat de radioteràpia. Moderna braquiteràpia La braquiteràpia va experimentar un notable avanç a partir dels anys vuitanta gràcies al desenvolupament de sofisticats equips que permeten que les fonts radioactives puguen implantar-se amb facilitat i precisió en qualsevol lloc de l’organisme. Com que es poden manipular per control remot, no plantegen cap perill per al personal que utilitza aquest material. Un altre avantatge és la incorporació d’una varietat d’isòtops radioactius que emeten diferents tipus de radiacions. Guiar la introducció dels isòtops per mitjà d’imatges en temps real (per exemple l’ecografia), com ocorre amb les llavors de iode-125 en el càncer de pròstata, és una altra manera de garantir la posició precisa de les fonts radioactives. Uns altres dels avantatges d’alguns d’aquests equips és que poden estar dotats de material radioactiu amb una gran activitat, i així la dosi per unitat de temps és molt elevada. D’aquesta manera els tractaments, que abans duraven uns quants dies (braquiteràpia de baixa taxa de dosi) es redueixen a fraccions d’hora i, per tant, es poden realitzar de manera ambulatòria. D’aquesta tècnica se’n diu braquiteràpia d’alta taxa de dosi. Una altra manera d’administrar la braquiteràpia amb aquests moderns equips és la denominada braquiteràpia polsada. En compte d’un tractament continu es donen períodes d’irradiació curts, separats per espais de temps majors sense irradiació. S’utilitza, per tant, una alta taxa de dosi, però es manté la durada del tractament, tan prolongat com en el mètode de baixa taxa. D’aquesta tècnica s’intenten obtenir els beneficis d’ambdues modalitats. |
||
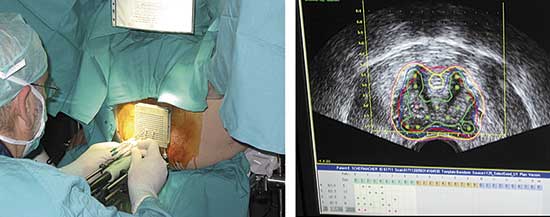
Braquiteràpia amb llavors de iode-125 en un càncer de pròstata. A la dreta es pot observar la distribució de les llavors. |
«La radioteràpia té un efecte de caràcter local i representa un paper fonamental en el 18% dels pacients amb càncer que aconsegueixen curar-se» |
|
|
Finalment, altres millores dels equips de braquiteràpia actuals són la possbilitat d’implantar els aplicadors per mitjà de tècniques d’estereotàxia en qualsevol tumor, per profundament que estiga localitzat. De vegades fins i tot s’haurà d’utilitzar l’abordatge quirúrgic per a col·locar els aplicadors –que solen ser catèters fins de material plàstic– en la resta tumoral que no puga ser extirpada. Veiem, per tant, que la indicació pot ser semblant a la de la radioteràpia intraoperatòria, però substituint el feix d’electrons per la inserció dels referits catèters, els extrems de la qual seran exteriors per a, després de l’acte quirúrgic, introduir-hi les fonts radioactives i fer-les arribar al tumor. Nous reptes La radioteràpia, amb més d’un segle d’existència, continua sent en l’actualitat un dels tractaments bàsics del càncer. Igual que la cirurgia, té un efecte de caràcter local i representa un paper fonamental en el 18% dels pacients amb càncer que aconsegueixen curar-se. Els avenços més destacats en radioteràpia es relacionen amb les altes tecnologies, la finalitat de les quals és poder irradiar amb la dosi adient el tumor i evitar que les radiacions arriben als teixits sans pròxims a ell. Aquests avenços s’han desenvolupat al llarg de les dues últimes dècades del segle xx i s’estan introduint a Espanya en la dècada actual. Ha de recalcar-se que en el desenvolupament d’aquestes tècniques ha influït decisivament el fet de poder determinar amb exactitud l’extensió dels tumors utilitzant les modernes tècniques d’imatge (TAC, RNM, PET…). Altres avenços tecnològics, no abordats en aquesta exposició, es relacionen amb els modificadors de la resposta biològica a la radiació, (radiosensibilitzants i radioprotectors). No ha d’oblidar-se finalment que també avui dia la biologia molecular té camp d’acció en les aplicacions de la radioteràpia. No cal sinó esmentar que podrà arribar a determinar-se quins tumors poden ser especialment radiosensibles i, per tant, tributaris de radioteràpia, i quins tumors seran radioresistents i, per tant, refractaris a aquesta tècnica. Ignacio Petschen Verdaguer i Mª Carmen García Mora. Servei d’Oncologia Radioteràpica, Hospital Universitari La Fe, València. |
Radioteràpia i el seus avenços recents