Seguint la pista del VIH
Els estudis i la comprensió de la Sida

El VIH o virus de la immunodeficiència humana té un gran impacte sanitari, social i econòmic; les teràpies actuals permeten controlar la infecció però no s’ha trobat tractament guaridor ni vacuna efectiva. Per a aconseguir aquests objectius, ha de tenir-se en compte la gran variabilitat genètica i la ràpida evolució del VIH, associades, per exemple, a l’aparició de variants de resistència a fàrmacs o de canvis antigènics.
Paraules clau: filogènia, biodiversitat, variabilitat genètica, mutació, salut pública, virus.
Què és el VIH i quina importància té?
La sida o síndrome de la immunodeficiència humana adquirida és un problema de salut pública mundial: des del descobriment del virus de la immunodeficiència humana (VIH) el 1983 han mort prop de 30 milions de persones i n’hi ha més de 40 milions d’infectades, la majoria en països en vies de desenvolupament. El VIH és un retrovirus que infecta específicament cèl·lules del sistema immunitari que expressen el receptor de membrana CD4, principalment els limfòcits T4. Com a conseqüència, causa el debilitament gradual del sistema immunitari. En fases avançades, provoca l’aparició de malalties oportunistes i alguns tipus de càncer característics de la sida. En absència de tractament, la mort es produeix de mitjana uns deu anys després de la infecció, encara que hi ha gran variabilitat en el temps de progressió de la malaltia depenent de les característiques del virus i del sistema immunitari del pacient.
«Mitjançant estudis evolutius es pot tractar de predir com respondrà el virus a la presència de fàrmacs, o quines variants és més probable que es propaguen en un futur»
L’estudi de l’evolució del VIH ha fet llum sobre la seua història natural però també sobre els mecanismes de patogènesi. Mitjançant estudis evolutius es pot a més tractar de predir, per exemple, com respondrà el virus a la presència de fàrmacs, o quines variants és més probable que es propaguen en un futur. De fet, els estudis evolutius han tingut un impacte positiu en el disseny del tractament de malalties humanes en general. Per exemple, l’estimació de la taxa de mutació (probabilitat d’aparició de canvis en el material hereditari) del VIH i del virus de l’hepatitis C va mostrar que cada dia apareixen en l’interior d’un pacient tots els canvis possibles d’un sol nucleòtid. Per tant, la resistència a fàrmacs és pràcticament inevitable llevat que usen teràpies combinades que actuen sobre diferents dianes i que requeresquen de l’aparició de múltiples canvis genètics en el virus perquè aquest desenvolupe una resistència.
Orígens i epidemiologia
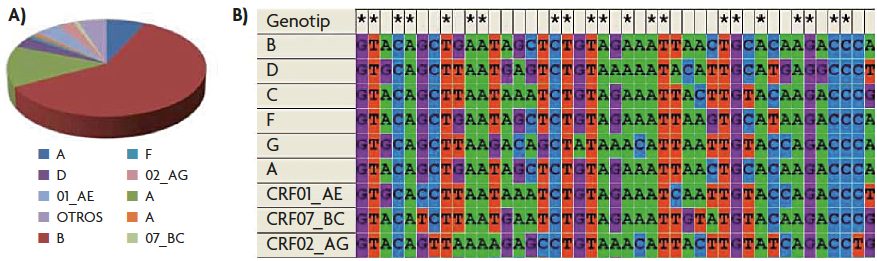
Els estudis de variabilitat i evolució ens han permès saber que hi ha dos tipus de VIH, el VIH-1 i el VIH-2, amb distinta procedència geogràfica i emparentats amb distints virus de la immunodeficiència de simis (VIS). Ambdós es van originar com a conseqüència d’una zoonosi, és a dir, una malaltia que es transmet d’animals a humans. El VIH-1 es va originar en els ximpanzés després d’un o més esdeveniments de recombinació entre diferents VIS que permeteren saltar la barrera d’espècie a causa de factors ecològics o genètics (Gao et al., 1999), mentre que el VIH-2 procedeix probablement de VIS del mangabei gris. El VIH-1 provoca la majoria de les infeccions i és el més virulent dels dos tipus. La divergència observada en el genoma complet entre el VIH-1 i el VIH-2 és aproximadament del 40 % al 60 %. Entre distints subtipus de VIH-1 pot arribar fins al 35 %, mentre que dins del grup M (que causa el 95 % de les infeccions per VIH) s’ha estimat que està entre el 10 % i el 30 %. Els majors valors de divergència s’observen en el gen que codifica per a l’embolcall (env)(Brenner, 2007). En la figura 1 es pot observar l’abundància dels diferents genotips de VIH-1 en el món i un exemple de la diversitat existent en el gen env entre els distints genotips de VIH-1.
«La transmissió del virus de mare a fill pràcticament es pot eliminar si s’aplica el tractament en les primeres setmanes de l’embraràs»
L’epidemiologia s’ocupa d’estudiar la causa, incidència, distribució i control de les malalties en les poblacions humanes. Des d’un punt de vista aplicat és important unificar el procés epidèmic i l’evolució dels patògens, ja siga relacionat amb l’evolució de la resistència a fàrmacs o de la virulència del patogen, el disseny de vacunes, o l’emergència de nous patògens i malalties transmeses per aquests. D’especial interès és poder comprendre com un patogen pot envair i propagar-se reeixidament en la població. L’informe d’ONUSIDA de 2010 mostra que les noves infeccions per VIH estan disminuint des de final dels anys noranta en la majoria de països afectats a l’Àfrica subsahariana gràcies a mesures preventives com l’ús del preservatiu. Contràriament, en alguns països de l’Europa de l’Est i Àsia central la incidència del VIH ha augmentat. A més, el major accés al tractament ha donat lloc a una disminució significativa de les morts per VIH i la transmissió vertical o de mare a fill pràcticament es pot eliminar si s’aplica el tractament en les primeres setmanes de l’embaràs.
Mecanismes evolutius
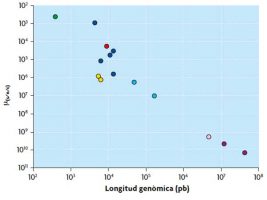
La mutació origina nova variabilitat genètica, mentre que la recombinació (en sentit ampli) produeix gran variabilitat genètica. Sobre aquesta variabilitat genètica poden actuar factors determinístics (com ara la mutació, la migració o la selecció) o aleatoris (deriva genètica). Alguns virus usen l’ARN com a material genètic en lloc de l’ADN, i aquests es caracteritzen per presentar taxes de mutació particularment elevades. Aquest és el cas del VIH, que usa per a replicar el seu genoma una polimerasa especial que copia ARN i el converteix en ADN, anomenada transcriptasa reversa. La majoria de polimerases que usen ARN com a motlle no tenen activitat correctora d’errors i això dóna lloc a mutacions, la qual cosa propicia que en una població viral hi haja variabilitat genètica. En la figura 2 es pot observar com varia la taxa de mutació en distints organismes. La major taxa de mutació es va descriure en un viroide de plantes; dins del grup dels virus, els d’ARN posseeixen les majors taxes de mutació, seguits dels virus d’ADN de cadena simple i virus d’ADN de doble cadena; el VIH té una taxa de mutació que es troba dins del rang dels virus d’ARN. Els organismes amb estructura cel·lular posseeixen taxes de mutació unes 100.000 vegades menors que les dels virus d’ARN.
Un altre aspecte molt important en l’evolució del VIH és la recombinació. El virió de VIH posseeix dues còpies del genoma en forma d’ARN i la transcriptasa reversa posseeix la capacitat de saltar d’una cadena a l’altra durant la síntesi de ADN, la qual cosa dóna lloc a molècules recombinants (Simon-Loriere i Holmes, 2011). La recombinació va representar un paper clau en l’origen del VIH i podria originar un nou tipus de VIH en el futur. La recombinació pot tenir efectes en l’expansió del rang d’hoste, virulència del virus, evasió del sistema immunitari o adquisició de resistència a fàrmacs. Per exemple, la forma recombinant circulant 01_AE, una vegada es va establir al nord de Tailàndia, va augmentar en freqüència i va predominar ràpidament en la resta de Tailàndia, Laos, Cambotja i Vietnam (Stephens, 2005). La deriva genètica és el procés pel qual les freqüències al·lèliques canvien a l’atzar d’una generació a la següent a causa d’efectes de mostratge en les poblacions. La intensitat és major com menor és la grandària poblacional, i en el cas del VIH ocorre principalment en la transmissió entre persones, perquè aquesta comporta colls d’ampolla en la grandària de la població viral. De fet està acceptat que la infecció per VIH sol començar amb la transmissió d’una o poques partícules infeccioses (Keele et al., 2008).
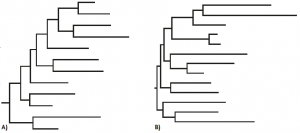
Els colls d’ampolla també poden ocórrer dins del pacient, per exemple, en subdivisions tissulars. La selecció natural, al seu torn, provoca canvis en les freqüències al·lèliques actuant sobre mutacions i/o genomes que influeixen sobre l’eficàcia biològica. La selecció pot ser adaptativa o positiva quan s’afavoreixla fixació de mutacions que siguen beneficioses en determinat ambient, o negativa quan s’eliminen mutacions deletèries. El sistema immunitari de l’hoste i els tractaments amb antivirals exerceixen una forta pressió de selecció sobre el virus, com veurem tot seguit. Els mecanismes evolutius que actuen sobre les poblacions virals poden tenir un paper diferent dins de l’hoste i entre hostes. Per exemple, quan s’observen les relacions filogenètiques de variants virals del gen env que codifica per a l’embolcall del virus podem distingir dos patrons distints; d’una banda les filogènies intrahoste indiquen l’acció d’una pressió de selecció, mentre que els arbres filogenètics interhoste suggereixen que la deriva té un paper més important (Grenfell et al., 2004) (figura 3).
Evasió del sistema immunitari
El sistema immunitari de l’hoste té un component innat (inespecífic) i un altre d’adaptatiu (específic). La resposta innata es caracteritza per la febre i la inflamació entre altres símptomes, els quals són controlats per processos com la secreció de citocines (per exemple, interferó). En el cas del VIH, a més, l’enzim APOBEC3G (una proteïna que edita ADN de cadena simple) participa en la resposta innata i provoca mutacions durant el procés de síntesi d’ADN viral a partir de l’ARN que inactiven el virus. Per a contrarestar-ne l’efecte, el VIH va incorporar al seu genoma un gen denominat factor d’infectivitat viral (vif) (Kirchhoff, 2010). Quant a la resposta específica, en vertebrats hi ha una sèrie de gens que codifiquen per al complex major d’histocompatibilitat (MHC). Aquest presenta porcions de les proteïnes virals denominades epítops, la qual cosa permet posar en marxa una resposta immunitària contra el virus.
«Una de les dificultats per al desenvolupament d’una vacuna contra el VIH-1 és l’elevada variabilitat genètica i la ràpida evolució del virus»
Les poblacions humanes són extraordinàriament variables per als gens MHC i per tant reconeixen distints epítops virals. S’ha demostrat que algunes variants del MHC permeten respondre millor a la infecció que altres i estan associades a una progressió més lenta de la malaltia (Buckheit III et al., 2012). Per a entendre això, és necessari considerar l’evolució del VIH dins dels pacients. La pressió exercida per la resposta immunitària específica fa que se seleccionen mutants del virus amb capacitat per a evadir aquesta resposta. No obstant això, aquestes mutacions poden comprometre la capacitat del virus per a dur a terme el seu cicle infecciós si afecten regions importants de les proteïnes virals (regions conservades). Són precisament aquelles variants del MHC capaces de reconèixer epítops virals en regions conservades les que estan associades a un millor pronòstic.
Resistència a antivirals
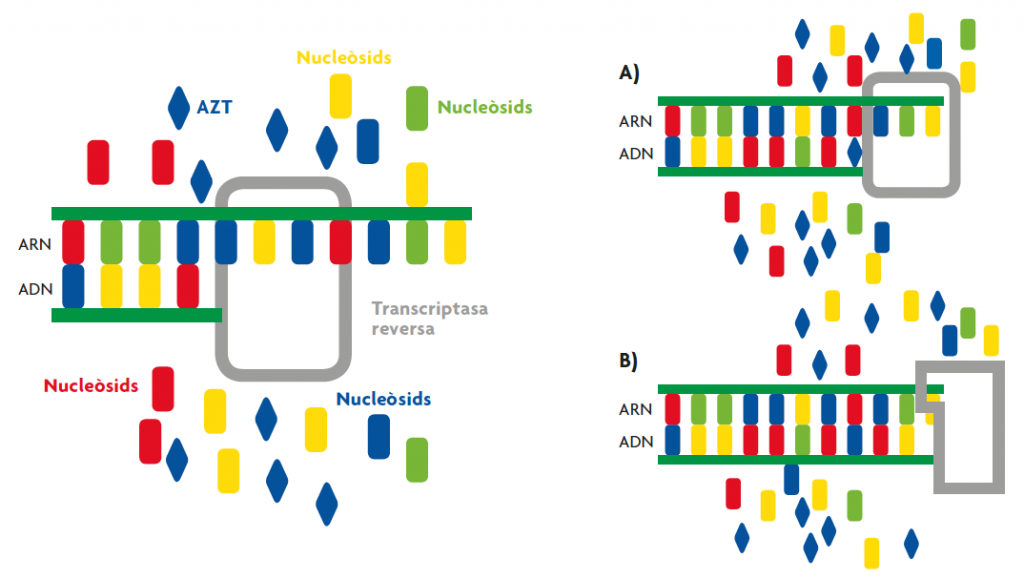
Com que els virus són paràsits intracel·lulars obligats i usen la maquinària cel·lular, és complicat trobar compostos que únicament afecten l’activitat viral, ja que també poden afectar negativament les cèl·lules hoste. Una aproximació al disseny de nous fàrmacs consisteix, doncs, a identificar els passos específicament virals del cicle infecciós. La transcriptasa reversa i la proteasa encarregada de processar la poliproteïna codificada pel VIH són dianes ideals, atès que són exclusives del virus. El primer compost contra la transcriptasa reversa que va mostrar efectivitat va ser l’azotimidina (AZT), un anàleg de nucleòsid amb estructura semblant a la dels nucleòtids que componen l’ADN. Quan en la cèl·lula és present l’AZT, la transcriptasa reversa l’afegeix per error a la cadena d’ADN de nova síntesi, cosa que interromp la síntesi (figura 4). No obstant això, es va observar que després d’un o dos anys de tractament, els pacients amb VIH deixaven de respondre i la malaltia continuava progressant. La resistència es devia a mutacions en el gen de la transcriptasa reversa, que eren convergents, és a dir, apareixien en poblacions virals de diferents pacients.
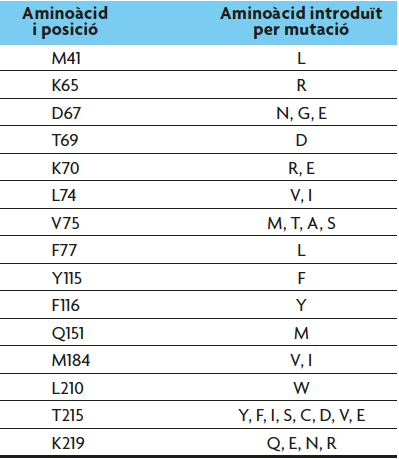
Algunes de les mutacions descrites localitzades en el centre actiu de la transcriptasa reversa són L74V i T215Y (la nomenclatura indica el canvi d’aminoàcid i la posició en què ocorre) (Bennett et al., 2009) (taula 1); a més algunes causen resistència encreuada a altres antivirals anàlegs de nucleòsid (Margeridon-Thermet i Shafer, 2010). A causa d’això, la composició genètica de la població de VIH va canviar amb el temps, en resposta a la presència de l’AZT. Això és un clar exemple d’evolució per selecció natural. Conseqüentment el tractament actual consisteix en combinacions de tres o quatre fàrmacs que inclouen inhibidors de la transcriptasa reversa i de la proteasa. Aquesta teràpia combinada és molt efectiva per bloquejar la replicació del virus i reduir la càrrega viral en la sang. No obstant això, com que el virus està latent en algunes cèl·lules, el bloqueig no és total, i això permet que, potencialment, puguen aparèixer partícules virals resistents, la qual cosa impediria l’eradicació del virus.
«La pressió exercida per la resposta immunitària específica fa que se seleccionen mutants del virus amb capacitat per a evadir aquesta resposta»
Disseny de vacunes
Una vacuna indueix la resposta immunitària específica cel·lular i humoral de manera que l’individu vacunat desenvolupa una memòria immunitària que li permet combatre millor el patogen. Tradicionalment s’han usat distintes estratègies com els patògens inactivats (per calor o químicament), atenuats, o compostos que els patògens presenten en la seua superfície que actuen com a determinant antigènic i són reconeguts per les cèl·lules del sistema immunitari. La vacunació ha tingut gran èxit en la prevenció i control de diverses malalties com ara la poliomielitis, la verola, el xarampió, la rubèola o la grip. En canvi, encara no s’han desenvolupat vacunes eficaces contra el VIH-1 o el virus de l’hepatitis C. Una de les dificultats per al desenvolupament d’una vacuna contra el VIH-1 és l’elevada variabilitat genètica i la ràpida evolució del virus. Com que el VIH-1 mostra una variabilitat tan gran, sobretot en el gen que codifica per a la proteïna de l’embolcall, una vacuna que protegesca contra un subtipus determinat podria no protegir o protegir parcialment contra altres subtipus del virus.
No obstant això, els estudis epidemiològics assenyalen que una vacuna amb una baixa eficàcia podria disminuir la incidència del VIH-1 en un percentatge significatiu (ONUSIDA, 2010). En aquesta línia, destaca l’estudi dut a terme l’any 2009 en la població tailandesa. Els resultats de la fase III d’assajos clínics van mostrar una eficàcia del 30 % en la protecció contra el VIH. La vacuna consistia en la combinació d’un vector que expressa immunògens (substàncies que indueixen la resposta immunitària adaptativa) del VIH-1 i una versió recombinant de la proteïna de l’embolcall (Rerks-Ngarm et al., 2009). Encara que aquest resultat no és prou per a aplicar de manera generalitzada la vacuna, dóna pistes per saber cap a on han d’orientar-se noves investigacions per a millorar la resposta immunitària mitjançant noves construccions, l’ús de diverses dosis o fins i tot l’administració de més i millors adjuvants (potenciadors de la resposta immunitària) que se subministren junt amb aquesta.
Conclusions i perspectives de futur
Per la importància de la sida, s’han destinat molts recursos econòmics per a estudiar el VIH. Els principals objectius dels grups d’investigació són desenvolupar fàrmacs antivirals eficaços i una vacuna. S’ha acomplert en gran manera el primer objectiu, però, no obstant això, l’obtenció d’una vacuna eficaç sembla llunyana. L’alta variabilitat del VIH, a causa de l’elevada taxa de mutació i recombinació, junt amb la latència que caracteritza la infecció, el fa especialment difícil de combatre. Per tant, el coneixement i la comprensió dels mecanismes evolutius que governen l’evolució del VIH són clau per a saber no sols com es va originar la malaltia, sinó també com es desenvolupa, com tractar-la, com pot canviar en el futur i, idealment, com eradicar-la.
Referències
Bennett, D. E. et al., 2009. «Drug Resistance Mutations for Surveillance of Transmitted HIV-1 Drug-Resistance: 2009 Update». PLOS One, 4: e4724. DOI: <10.1371/journal.pone.0004724>.
Brenner, B. G., 2007. «Resistance and Viral Subtypes: How Important Are the Differences and Why Do They Occur?». Current Opinion in HIV and AIDS, 2(2): 94-102. DOI: <10.1097/COH.0b013e32801682e2>.
Buckheit III, R. W. et al., 2013. «The Implications of Viral Reservoirs on the Elite Control of HIV-1 Infection». Cellular and Molecular Life Sciences, 70(6): 1009-1019. DOI <10.1007/s00018-012-1101-7>.
Gao, F. et al., 1999. «Origin of HIV-1 in the Chimpanzee Pan troglodytes troglodytes». Nature, 397: 436-441. DOI: <10.1038/17130>.
Grenfell, B. T. et al., 2004. «Unifying the Epidemiological and Evolutionary Dynamics of Pathogens». Science, 303(5656): 327-332. DOI: <10.1126/science.1090727>.
Keele, B. F. et al., 2008. «Identification and Characterization of Transmitted Early Founder Virus Envelopes in Primary HIV-1 Infection». PNAS, 105(21): 7552-7557. DOI: <10.1073/pnas.0802203105>.
Kirchhoff, F., 2010. «Immune Evasion and Counteraction of Restriction Factors by HIV-1 and Other Primate Lentiviruses». Cell Host and Microbe, 8(1): 55-67. DOI: <10.1016/j.chom.2010.06.004>.
Margeridon-Thermet, S. i R. W. Shafer, 2010. «Comparison of the Mechanisms of Drug Resistance Among HIV, Hepatitis B, and Hepatitis C». Viruses, 2(12): 2696-2739. DOI: <10.3390/v2122696>
ONUSIDA, 2010. Informe mundial. Informe del ONUSIDA sobre la epidemia mundial del SIDA. Disponible en: <http://www.unaids.org/en/media/unaids/contentassets/documents/unaidspublication/2010/JC1958_GlobalReport2010_full_es.pdf>.
Rerks-Ngarm, S. et al., 2009. «Vaccination with ALVAC and AIDSVAX to Prevent HIV-1 Infection in Thailand». The New England Journal of Medicine, 361: 2209-2220. DOI: <10.1056/NEJMoa0908492>.
Simon-Loriere, E. i E. C. Holmes, 2011. «Why do RNA Viruses Recombine?». Nature Reviews Microbiology, 9: 617-626. DOI: <10.1038/nrmicro2614>.
Stephens, H. A. F., 2005. «HIV-1 Diversity Versus HLA Class I Polymorphism». Trends in Immunology, 26(1): 41-47. DOI: <10.1016/j.it.2004.11.001>.





