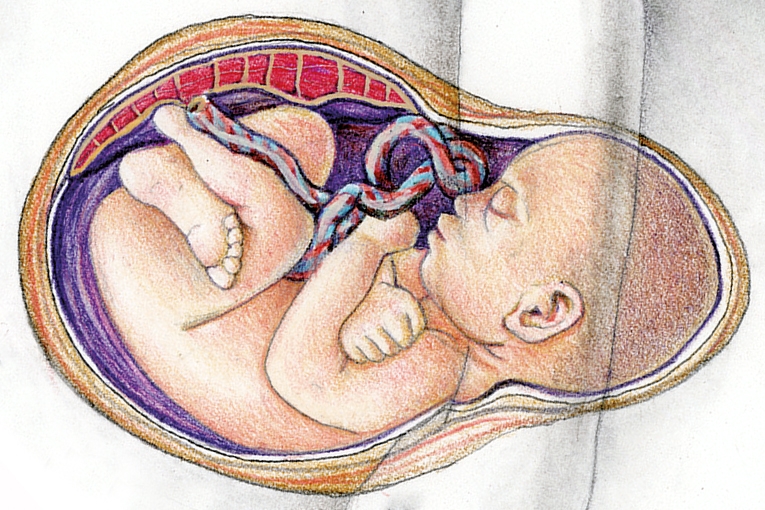
«Ja el nàixer és un gran plor», ens canta Raimon. Hi ha dos moments crucials que fiten tota vida humana: el naixement i la mort. La mort arriba de moltes maneres, agònica o tranquil·la, patint lentament o per un gran trauma sobtat, conscients o sense adonar-nos-en. El naixement, però, gairebé sempre va acompanyat d’un gran plor; un plor necessari per respirar de manera autònoma i conseqüència del xoc que ens produeix ser expulsats del confortable úter matern i trobar-nos en un ambient hostil, sec i fred, que no abandonarem fins a la mort.
Tota la nostra vida, i la mort, està acompanyada de microbis. De tota la nostra existència, només els primers nou mesos (dins l’úter), o això és el que es pensava, estem aïllats del contacte o la interacció amb els microorganismes. Ja durant el part, la nostra pell i el tub digestiu comencen a colonitzar-se. En trencar-se el sac amniòtic, desprendre’s la placenta i passar per la vagina de la mare, la nostra pell delicada es va «contaminant» de microbis. Immediatament després continuem incorporant més microbis, aquesta vegada ja a dins la boca i la resta del tub digestiu, a causa del contacte amb el cos de la mare i de l’ambient.
En el transcurs d’un embaràs normal i saludable, el cos de la mare experimenta canvis importants anatòmics, fisiològics i bioquímics. Primer augmenta el greix corporal; posteriorment, segons avança la gestació, hi ha una reducció de la sensibilitat a la insulina. Durant l’embaràs s’observen nivells elevats de citoquines circulants, és a dir, un augment de l’estat d’inflamació i síndrome metabòlica que condueix cap una mena d’«obesitat». Aquesta «obesitat» fisiològica i la pèrdua de sensibilitat a la insulina són beneficioses, ja que afavoreix el creixement del fetus i prepara el cos de la mare per a la demanda energètica de la lactància. Durant l’embaràs es produeix un canvi en el sistema immunitari de la mare per evitar el rebuig del fetus (a nivell de placenta), però, per altra banda, augmenta la resposta inflamatòria de les mucoses, cosa que pot conduir a, per exemple, gingivitis. La placenta permet passar al fetus l’oxigen i nutrients, i retirar els productes de rebuig, sense que hi hagi barreja de la sang materna i la fetal. La placenta, per tant, intervé en la nutrició, el control del creixement i la regulació del metabolisme, fent les funcions de pulmons, intestí i ronyons del fetus, que solament començaran a treballar de manera autònoma a partir del part.
Durant l’embaràs s’havien descrit canvis importants en la microbiota de la mare, tant del tracte intestinal com de la vagina. Però ara s’està veient que també experimenten modificacions importants la microbiota oral, la de la pell i la de la placenta. Aquests canvis en la microbiota de la mare semblen crucials per al futur desenvolupament d’una microbiota «sana» del neonat. Durant l’embaràs, la microbiota de la vagina disminueix en diversitat i dominen algunes espècies de Lactobacillus, com ara L. crispatus, L. jensenii o L. johnsonii. L’enriquiment d’aquestes espècies té significat biològic. Per exemple, L. jensenii metabolitza el glucogen, que s’incrementa amb l’augment dels nivells d’estrogen, i que contribueix a l’acidesa vaginal. A més, L. jensenii pot presentar en la superfície cel·lular proteïnes que inhibeixen alguns patògens que causen infeccions de transmissió sexual, com ara Neisseria gonorrhoeae. Finalment, L. crispatus i L. jensenii produeixen peròxid d’hidrogen, que podria protegir contra algunes infeccions bacterianes de la vagina. Després del part, L. johnsonii colonitza el tracte intestinal del neonat, ajudant-lo a digerir la llet.
«La placenta fa les funcions de pulmons, intestí i ronyons del fetus, que solament començaran a treballar de manera autònoma a partir del part»
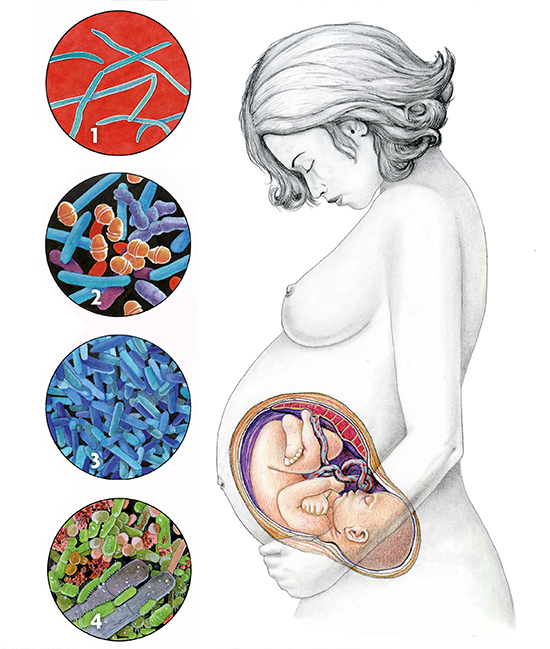
Microbiota de diferents parts del cos d’una dona. 1. Fusobacterium, en líquid amniòtic (només en situació patològica, en dones que pateixen part prematur). 2. Microbiota normal de la placenta, representada per un baix nombre de bacteris, però pertanyents a diferents grups (com ara els fílums Firmicutes, Tenericutes, Proteobacteria, Bacteroidetes i Fusobacteri). 3. Microbiota de la vagina, on normalment predomina L. acidophilus, però durant l’embaràs es fan abundants altres espècies del mateix gènere, com ara L. crispatus, L. jensenii i L. johnsonii. 4. Microbiota de la pell corresponent a una zona humida, com ara el pubis, on predominen els fílums Firmicutes i Actinobacteria.
Sempre s’havia pensat que la placenta no tenia cap microbi, però recentment s’ha observat que la placenta té alguns tipus de microorganismes, tant gram-positius com gram-negatius. Generalment, aquests microorganismes no són patògens, però, en alguns casos, les variacions en la seva composició podrien ser l’origen de trastorns poc coneguts de l’embaràs, com ara el part prematur, que es produeix en un de cada deu embarassos. La inflamació de la placenta pot provocar contraccions i el part prematur. Aquests resultats reforcen observacions prèvies que relacionaven les malalties periodontals de la mare amb els parts prematurs.
El tracte intestinal del fetus s’ha considerat que no tenia cap microbi, però sembla que l’exposició del fetus als microorganismes podria ser abans del part, pels microorganismes que colonitzen la placenta. El que ja se sabia és que alguns pocs microorganismes patògens, com ara els bacteris Treponema pallidum (sífilis) o Listeria monocytogenes (listeriosi) i el virus VIH (sida), eren capaços de travessar la barrera placentària i penetrar al cos del fetus a través de la sang. D’aquesta manera, el nadó podria tenir una infecció congènita amb greus seqüeles i que fins i tot pot causar la mort. La composició bacteriana del tracte intestinal d’un nadó tan sols una setmana després de néixer és complexa, dinàmica i fluctuant. Els nens no presenten una microbiota equilibrada similar a la dels adults fins al voltant del primer any. En la primera setmana de vida l’intestí ja està colonitzat per Actinobacteria (incloent-hi Bifidobacterium), Proteobacteria, Bacteroides, i en menor proporció, Firmicutes (o gram-positius, com ara Lactobacillus, que és el microorganisme dominant en la vagina). Pel contrari, en els neonats prematurs amb un pes inferior a 1.200 grams dominen els Firmicutes i Tenericutes, i tenen menor proporció d’Actinobacteria. A més del tipus de part, l’alimentació per lactància materna o artificial té un gran impacte en la microbiota del nounat. La lactància materna selecciona aquells organismes capaços d’utilitzar els constituents de la llet materna. Els oligosacàrids de la llet humana són els principals factors de creixement per Bifidobacterium, i també pels Bacteroidetes.
Quan considerem la història de la microbiologia, podem dir que ha tingut tres edats d’or. La primera, sens dubte, és la que van començar Pasteur i Koch, durant l’últim quart del segle xix, i en la qual es van identificar la major part de les malalties infeccioses. La segona correspondria a les dècades dels quaranta i cinquanta del segle xx, quan el descobriment i aplicació dels antibiòtics van suposar la primera arma efectiva contra les infeccions. Finalment, la tercera ha estat l’edat de la genòmica, en les dues últimes dècades del segle xx. Però ja en el segle xxi estem entrant en una quarta edat d’or, on la seqüenciació massiva de tots els microorganismes presents en un determinat lloc (pell, boca, intestí, etc.),
o metagenòmica, ha permès descobrir la presència i possible funció de microorganismes que ni tan sols se sospitaven. Es calcula que en una boca normal hi ha fins a set-centes espècies de bacteris –encara que el concepte habitual d’espècie en animals i plantes és molt diferent del que podem considerar «espècie» en els bacteris.
En els últims anys s’han fet grans progressos no només en la identificació, aïllament i cultiu dels membres de la microbiota intestinal, sinó també en el desenvolupament d’eines i models genètics que permeten estudiar la interacció entre el microbioma (o conjunt de gens dels microbis del cos), i la genètica i fisiologia de l’hoste. La combinació d’aquestes eines per realitzar nous estudis en el futur aprofundirà en gran mesura la nostra comprensió de les dianes moleculars en la interacció homeostàtica entre la microbiota intestinal i el nostre cos, i, per tant, promet revelar noves formes de tractar les malalties i mantenir la salut.
Ricard Guerrero. Membre de l’Institut d’Estudis Catalans.
Mercè Berlanga. Professora agregada interina del departament de Microbiologia i Parasitologia. Universitat de Barcelona.
© Mètode 83, Tardor 2014.
El primer plor
El primer llanto