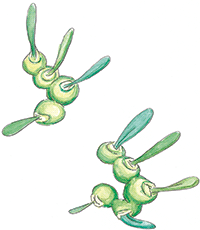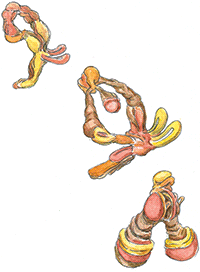
|
© Cortesia del Dr. Francesc Cebriá (Institut de Biomedicina de la Universitat de Barcelona-IBUB) |
||
|
Segons les investigacions realitzades en 1987 per Rebeca Cann i Alan Wilson, de la Universitat de Califòrnia (Berkeley), tots els éssers humans actuals tenim el nostre origen en una petita tribu que va habitar a l’Àfrica. Sorprenentment, les diferències trobades en l’ADN mitocondrial d’éssers humans actuals van demostrar que aquest procedia de l’ADN d’una dona que degué haver viscut fa només 200.000 anys (Cann et al., 1987). Això ens en fa a tots nosaltres cosins llunyans, i converteix aquella dona en Eva, la mare de tots. Avui és espectacular la diversitat humana. En tot aquest temps, els humans hem anat diferenciant-nos: ulls ametllats, pell i cabell de diferents colors i textures, diferents estatures i complexions. D’una manera semblant, els incomptables tipus de cèl·lules que poblen el cos de cada un de nosaltres s’han diferenciat a partir d’una primera única cèl·lula, la mare de totes les nostres cèl·lules, el zigot, que es va originar en unir-se un òvul i un espermatozoide. És a dir: a més de la nostra mare (la de tots els dies, que ens pega un calbot quan plantem els colzes damunt la taula), segons sembla tenim una mare de fa 200.000 anys i una altra que era només una cèl·lula, el zigot. Però n’hi ha més. Naix una nova mare Es podria dir que tot va començar amb Rudolf Virchov, l’autor d’un desconcertant pictograma que el 1858 va recórrer amb estrèpit les publicacions científiques i cercles acadèmics: omnis cellula e cellula. Tota cèl·lula prové d’una altra cèl·lula. Fins ací, cap problema, i tots podríem posar-nos d’acord que, en el nostre cos, una cèl·lula de la pell prové d’una altra cèl·lula de la pell, i que una cèl·lula muscular prové d’una altra cèl·lula del múscul. Però el temps va demostrar que no és tot tan fàcil. Quaranta anys després, els investigadors europeus es van agitar novament davant d’un descobriment sorprenent: les distintes cèl·lules de la sang (leucòcits, eritròcits, megacariòcits…) provenien totes d’un tipus particular de cèl·lula que es trobava en la medul·la òssia, la qual van anomenar cèl·lula mare (en anglès, stem cell). Això significava que, una vegada adults, teníem en el nostre cos cèl·lules que continuaven exercint de mares, diferenciant-se i originant diferents tipus de cèl·lules segons les necessitats del cos, la qual cosa li permet regenerar-se. Aquest procés de diferenciació cel·lular, que té lloc en el desenvolupament de l’embrió, segons sembla continuava de manera semblant dins de la medul·la òssia una vegada adults. Això significava que davant d’una malaltia es podria regenerar el sistema de cèl·lules sanguínies a partir de les cèl·lules mare? El 1963, els investigadors Ernest McCulloch i James E. Hill van donar amb la resposta: van trasplantar cèl·lules de medul·la òssia a ratolins en què el sistema de cèl·lules sanguínies havia estat seriosament danyat mitjançant radiacions. Després del trasplantament, els ratolins van començar a regenerar el sistema sanguini. Actualment, als malalts que han rebut tractaments de quimioteràpia –que solen afectar les cèl·lules sanguínies– se’ls reconstrueix el sistema immunològic mitjançant trasplantaments de medul·la òssia. Però els experiments de McCulloch i Hill obrien una nova pregunta: Aquestes cèl·lules mare només podien regenerar les cèl·lules sanguínies o també altres tipus de cèl·lules? Hi havia altres cèl·lules mare per als altres tipus de cèl·lules? La llista de malalties que es podrien tractar és immensa, i les possibilitats, infinites. I tot ha començat a anar molt de pressa. Les dades aportades pels experiments realitzats obren un horitzó sense límits, i les possibles aplicacions apareixen a un ritme vertiginós: diabetis, lesions medul·lars, Parkinson, cor… És increïble el que podem fer avui, i ningú no sap el que podrem fer demà. Un cos de recanvi? El nostre cos és fet de cèl·lules, i quan les cèl·lules moren o deixen de funcionar, també ho fa el nostre cos, i morim, la qual cosa per a la majoria de nosaltres resulta bastant enutjosa. El nostre organisme té mecanismes per evitar-ho, però lamentablement, l’envelliment o els accidents poden (i solen) superar la nostra capacitat de regeneració. Això és el que preocupa Juan Carlos Chachques, investigador en l’Hospital George Pompidou, de la Universitat de París. Chachques aconsegueix reparar cors danyats mitjançant el trasplantament de cèl·lules mare. En compte de substituir l’òrgan sencer per un altre d’un donant (amb el seriós inconvenient de trobar un donant adequat que vulga cedir el seu cor), Chachques explica que extrau cèl·lules mare del mateix pacient per reemplaçar les cèl·lules que han deixat de funcionar. «A través d’una punció en la medul·la òssia del pacient anem al centre de producció de cèl·lules mare; aspirem el material del qual després, per tècniques de centrifugació, extraiem una alta concentració d’aquestes cèl·lules. Una vegada injectades en el lloc de la cicatriu que deixa l’infart, aquestes cèl·lules es diferencien i permeten regenerar el teixit cardíac», indicava l’investigador en una entrevista.1 Aquesta notícia, publicada en la revista Annals of Thoracic Surgery (Chachques et al., 2004), és meravellosa per als afectats de lesions de cor, que veuen la seua qualitat i esperança de vida decréixer sense poder fer gaire. La solució està dins dels seus ossos! Lamentablement, aquestes cèl·lules mare adultes semblen no funcionar en tots els casos: les cèl·lules mare sanguínies (situades en la medul·la òssia) van ser capaces de regenerar cèl·lules sanguínies i del cor, però no qualsevol teixit. Davant d’això, per regenerar altres teixits a partir de cèl·lules adultes, els investigadors han caminat en dues noves direccions: trobar cèl·lules mare per a cada tipus de teixit o bé intentar que les cèl·lules mare sanguínies o altres «obliden» la seua procedència i siguen capaces d’originar altres tipus de cèl·lules. Hernán López-Schier i Pilar Muñoz Cánovas són investigadors en el Centre de Regulació Genòmica de Barcelona, i estudien la participació de cèl·lules mare en la restauració i regeneració de cèl·lules sensorials i musculars. López-Schier segueix la pista d’unes estranyes cèl·lules que semblen amagar-se: «Quan les cèl·lules sensorials són destruïdes, aquestes noves cèl·lules apareixen, probablement derivades d’algun tipus de cèl·lula mare encara desconegut, i regeneren les cèl·lules sensorials. Després, desapareixen novament.»2 Per a Muñoz-Cánovas, les cèl·lules mare representen un paper important en el desenvolupament i restauració muscular, mitjançant la intervenció d’una molècula inflamatòria anomenada interleucina 6 (IL·LTRE-6). Segons la investigadora «aquestes dades podrien facilitar el descobriment de noves vies alternatives per a restaurar la pèrdua de massa muscular en les persones grans o en aquelles afectades per malalties amb atròfia muscular».3 Les aportacions de López-Schier (López-Schier i Hudspeth, 2006) i Muñoz-Cánovas (Serrano et al., 2008), publicades en les revistes PNAS i Cell Metabolism, semblen indicar que els teixits sensorials i musculars tenen les seues pròpies cèl·lules mare, capaces d’originar aquells tipus de cèl·lules que les cèl·lules mare sanguínies no poden generar. Llavors, per què no fer que les cèl·lules mare que ja són presents en el teixit treballen? Això és exactament el que investiga un grup de l’Imperial College London: en una publicació recent en Cell Stem Cell (Simon et al., 2009), descriuen que, mitjançant la injecció de diferents drogues en la sang, promouen la formació de diversos tipus de cèl·lules mare en l’interior del cos, del tipus adequat en cada teixit. I si intentem aconseguir cèl·lules mare per a un teixit a partir de cèl·lules d’altres teixits? L’any 2000, la idea va començar a solidificar: els experiments avançats en ratolins indicaven que manipulant en les cèl·lules mare sanguínies es podien generar també cèl·lules nervioses o hepàtiques. Des de llavors, la conservació de les cèl·lules mare de la sang del cordó umbilical ha començat a considerar-se una mena d’«assegurança de vida». Però la tècnica ha anat més enllà: el 2006, Shinya Yamanaka, investigador de la Universitat de Kyoto, al Japó, va aconseguir desdiferenciar cèl·lules adultes diferenciades de ratolí i tornar-les a un estat embrionari. Màgia? No. Yamanaka va descriure en la revista Cell que va infectar cèl·lules de la pell amb virus manipulats genèticament que portaven quatre gens acuradament triats (Takahashi i Yamanaka, 2006). Els virus es van inserir en l’ADN de les cèl·lules junt amb els gens així transportats (factors de transcripció) i van aconseguir «desdiferenciar-les», de manera que mostraven característiques de cèl·lules mare. Havien nascut les cèl·lules pluripotents induïdes (IP). Hipotèticament es podrien aconseguir cèl·lules mare de gairebé qualsevol cèl·lula! Per a Juan Carlos Izpisúa, del Centre de Medicina Regenerativa de Barcelona (CRMB), els seus resultats en Nature Protocols (Giorgetti et al., 2010) indiquen que el procés fins i tot es podria simplificar. «El nostre treball indica que podem reprogramar amb només dos factors, eliminant-ne així dos que són oncogens (gens del càncer)», assegurava el científic en un article publicat en El País.4 Izpisúa forma part del grup d’investigadors que ha desenvolupat una metodologia per tractar els pacients d’anèmia de Fanconi, una rara i greu malaltia genètica. Seguint la tecnologia de les IP, investigadors d’aquest grup, dirigits per Ángel Raya i Juan Carlos Izpisúa, van extraure cèl·lules de la pell d’un pacient, i, mitjançant enginyeria genètica, van corregir els gens mutats i desdiferenciaren les cèl·lules perquè «oblidaren» que eren cèl·lules de la pell. Aquestes cèl·lules pluripotents induïdes sanes eren capaces de convertir-se en cèl·lules mare sanguínies lliures de la malaltia, i, per tant, teòricament capaces de regenerar el sistema sanguini dels afectats. Aquests resultats, publicats en la revista Nature (Raya et al., 2009), en pocs anys podrien aplicar-se a humans. No obstant això, hi ha alguns problemes: els gens introduïts per «desprogramar» les cèl·lules són oncogens (gens relacionats amb l’aparició de càncer), i es mantenen en les cèl·lules quan aquestes són reinserides en el pacient. No podria això provocar càncer en el pacient? De fet, aquest sembla un risc possible. Investigacions recents indiquen que els tumors contenen cèl·lules mare. Segons Allan Mufson, director de la secció de Biologia del Càncer en el National Cancer Institute, als EUA, aquestes cèl·lules són les responsables de l’existència i expansió dels tumors. «No són el mateix que les cèl·lules mare normals. Tot indica que hi ha una petita població de cèl·lules dins dels tumors que són les responsables del progrés del tumor. Són les úniques que poden originar nous tumors», explicava Mufson en un article de la revista Live Science.5 María Blasco, investigadora del Centre Nacional d’Investigacions Oncològiques (CNIO), i Juan Carlos Izpisúa, del CRMB, segueixen la pista a p53, un gen relacionat amb el càncer que quan està mutat permet la desdiferenciació de les cèl·lules. Tots dos investigadors estan convençuts que p53 intervé de manera clau en els dos processos: càncer i desdiferenciació. Blasco, coautora d’un article sobre el tema publicat recentment en la revista Nature (Marión et al., 2009), afirma: «Fa uns anys es va demostrar que els tumors anaven plens de cèl·lules danyades que persistien, i alguna cosa semblant veiem en les IP que han eliminat p53, i en els teixits que se’n deriven: que són plens de danys». Per a Izpisúa, del CMRB, la raó és clara, segons assenyalava en un article d’El País:6 «Això vol dir que p53 també actua com un guardià contra la reprogramació de les cèl·lules somàtiques en l’organisme normal. Això és important per a la hipòtesi que es discuteix fa temps: que el càncer consisteix en una desdiferenciació de cèl·lules diferenciades.» Al capdavall, una de les capacitats que les cèl·lules veuen limitada a mesura que es diferencien és la capacitat de multiplicar-se. En el càncer, un grup de cèl·lules recuperaria aquesta capacitat en desdiferenciar-se. Essencialment, aquest procés és també el que ha de dur-se a terme per aconseguir cèl·lules mare IP. Llavors, si els mecanismes són tan semblants, com evitarem que les cèl·lules mare IP desenvolupen tumors una vegada dins de l’organisme? La solució sembla passar per una acció transitòria dels gens usats per desdiferenciar les cèl·lules. En compte d’usar gens inserits, una solució possible és aportar només les proteïnes que codifiquen aquests gens, amb un efecte de més curt termini, o, com afirma Thomas Graf, investigador del Centre de Regulació Genòmica, «potser aquest obstacle es puga superar tractant les cèl·lules derivades de la pell amb substàncies químiques, en compte de retrovirus, per a induir la reprogramació».7 Tot sembla estar preparat perquè puguem generar cèl·lules mare capaces de donar lloc a qualsevol tipus de cèl·lula. Seria fantàstic aconseguir «fabricar» en el laboratori un òrgan complet a partir de les pròpies cèl·lules mare del pacient per a trasplantar-li’l després. Però les cèl·lules presenten una organització en teixits i òrgans, en simetries i estructures complicades i indispensables per a la seua funció. Com reconstruir un òrgan sencer? Amb què dirigir les cèl·lules en el seu creixement en les tres dimensions de l’espai? El 2008, a l’Hospital Clínic de Barcelona, va tenir lloc un trasplantament de tràquea bastant peculiar: l’equip d’investigadors, dirigit per Paolo Macchiarini, va usar la tràquea d’un donant com a «bastida» per construir-ne una de nova amb cèl·lules mare de la pacient. Segons descriuen en el seu treball, publicat en la revista The Lancet (Macchiarini, 2008), van prendre la tràquea del donant i van eliminar amb detergents les cèl·lules que contenia per deixar només el teixit connectiu de suport. En aquest teixit van fer créixer les cèl·lules mare extretes de la medul·la òssia de la pacient; van aconseguir així una tràquea que va ser trasplantada a la pacient i que fins al moment no ha generat rebuig; la construcció d’un òrgan. El mannÀ de les cÈl·lules mare, el futur i un consell El 1892, el biòleg alemany Hans Driesch va fer un experiment de resultats sorprenents: va aconseguir embrions d’eriçó de mar en l’estadi de dues o quatre cèl·lules i els va dividir en embrions d’una cèl·lula cadascun. Els embrions resultants van ser capaços de donar lloc cadascun a un nou organisme viu. Aquest experiment demostrava que les primeres cèl·lules embrionàries mantenen la capacitat de donar lloc a tots els teixits. Són totipotents. Això les converteix en ideals per a exercir com a cèl·lules mare! Cent anys després, l’investigador James Thompson, de la Universitat de Wisconsin, va aconseguir aïllar cèl·lules mare d’embrions i fer-les créixer de manera independent al laboratori: havia nascut la primera línia de cèl·lules mare embrionàries. El seu caràcter totipotent fa que, com a cèl·lules mare, siguen encara millors que les cèl·lules mare d’adult, o les IP, perquè no cal desdiferenciar-les, i evita els inconvenients que això significa. Anna Veiga, del registre de cèl·lules mare embrionàries del Centre de Medicina Regenerativa de Barcelona (CRMB), afirmava en una entrevista en El Periòdic:8 «Les cèl·lules mare tenen totes les potencialitats per a convertir-se en qualsevol tipus cel·lular. Treballem per esbrinar com es mantenen en l’estat neutre, per què són capaces de transformar-se, per exemple, en neurones o en cardiomiocits, i com es fa per a marcar-los el camí de la transformació.» Però res no és perfecte: encara que aquestes cèl·lules semblen ser, de moment insubstituïbles pel que fa a la investigació sobre els processos de diferenciació, presenten inconvenients per a l’ús terapèutic, i el seu ús ha implicat discussions ètiques al voltant de la naturalesa de l’embrió. En realitat, les cèl·lules embrionàries i les cèl·lules IP es diferencien en la manera com s’obtenen, i constitueixen un equip perfecte. Per a poder usar i trasplantar la cèl·lula mare a un pacient, l’ideal és que les cèl·lules mare hagen estat extretes d’aquest mateix pacient o parents pròxims, per evitar problemes de rebuig al trasplantament. Amb les cèl·lules IP aquest problema estava solucionat: n’hi havia prou d’extraure una mostra de pell del mateix pacient. En canvi, l’extracció de cèl·lules de l’embrió és una operació perillosa, el que dificulta disposar de les cèl·lules mare embrionàries de cadascun de nosaltres. Això, en conjunt amb les seues increïbles capacitats, fa que les cèl·lules mare embrionàries siguen considerades una joia per a la investigació, mentre que les IP es perfilen com a candidates a l’aplicació d’aquesta tecnologia. En definitiva, actualment les cèl·lules mare es poden obtenir per tres vies diferents, cadascuna amb els seus avantatges i inconvenients: cèl·lules mare embrionàries (procedents de les fases novelles de l’embrió), cèl·lules mare adultes (presents en teixits dels individus adults, com la medul·la òssia) i cèl·lules mare desdiferenciades (IP, cèl·lules adultes diferenciades sotmeses a tractaments en el laboratori perquè siguen novament pluripotents). Les cèl·lules mare són una tecnologia que té, com a màxim, deu anys. Cal solucionar les dificultats que han anat apareixent: el caràcter tumoral d’algunes cèl·lules mare en determinades circumstàncies, les metodologies per a obtenir les cèl·lules mare, el procés de rediferenciació, les estratègies de reconstrucció d’òrgans… Si bé és cert que els progressos esguiten els nostres periòdics i cada dia ens sorprenen les noves aplicacions d’aquesta tecnologia, hem de tenir present que la majoria dels estudis es realitzen encara en models animals, i que ajustar la tècnica als humans pot costar un temps, que els experts calculen entre tres i deu anys. Mentrestant, noves preguntes s’obren: Viurem mil anys? Existiran un dia «cèl·lules pare», capaces de desenvolupar en nosaltres òrgans que no ens són propis? Podrem curar un càncer fent que torne a diferenciar-se? Podrem reconstruir un braç sencer? Fins a quin punt regenerar neurones no implicarà una pèrdua de la memòria o de la identitat? Ja sabem que venim d’una mare de fa 200.000 anys. No sabem amb certesa, en canvi, fins on ens portarà aquesta altra nova, misteriosa i prometedora mare. En tot cas, mentrestant, fem cas de la nostra tercera mare (la dels calbots) i conduïm amb atenció. NOTES BIBLIOGRAFIA AGRAÏMENTS Jordi Domènech Casal. Doctor en Biologia. Grup Òliba de Museologia Virtual, grup d’investigació IN3. Universitat Oberta de Catalunya. Finalista del premi Ciencia en Acción 2009 i guanyador del premi Prisma al millor lloc web de divulgació científica 2011 pel Museu Virtual Interactiu Llegint el llibre de la vida.
|
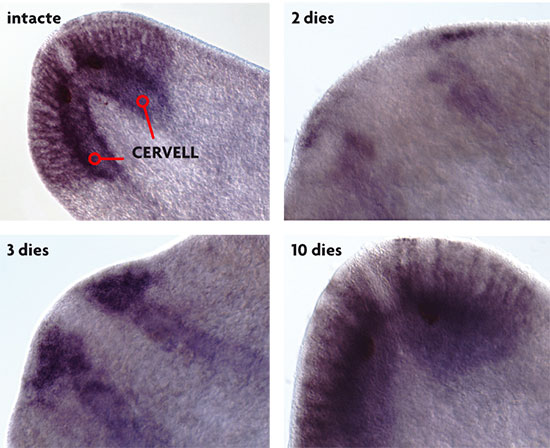
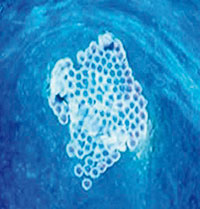
Julio López Tornel. Sèrie «Carn de paper», 2010. Aquarel·la, 21 x 29,7 cm. «La regeneració és una capacitat que espècies com la salamandra i l’estrella de mar tenen especialment desenvolupada i apareix sovint en la mitologia. Prometeu, un semidéu grec, va ser castigat per Zeus: el seu fetge havia de ser menjat eternament pels voltors a mesura que es regenerava. El monstre mític Hidra regenerava els seus caps quan eren tallats per l’espasa d’Hèrcules. El detall més curiós és que s’ha descobert que el fetge té realment capacitats regenerants, i que hi ha un minúscul animal, a qui s’ha anomenat oportunament “hidra”, que pot regenerar el cap quan aquest és tallat. Sense saber-ho, els grecs no anaven tan equivocats…»
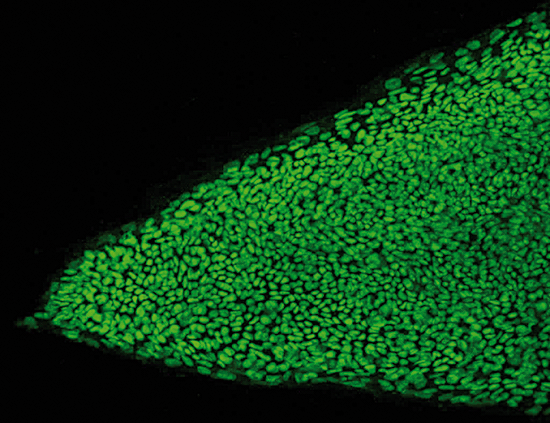
Julio López Tornel. Sèrie «Carn de paper», 2010. Aquarel·la, 21 x 29,7 cm. «A diferència de les cèl·lules mare embrionàries (totipotents), que poden convertir-se en qualsevol tipus de cèl·lula, les cèl·lules mare adultes són pluripotents, i per tant, només poden originar cèl·lules d’alguns teixits, sovint semblants al teixit en què estan allotjades. La resta de cèl·lules adultes rep el nom de cèl·lules «diferenciades», estan especialitzades en alguna comesa, no poden originar cap altre tipus cel·lular i les seues capacitats de multiplicació solen ser limitades.»
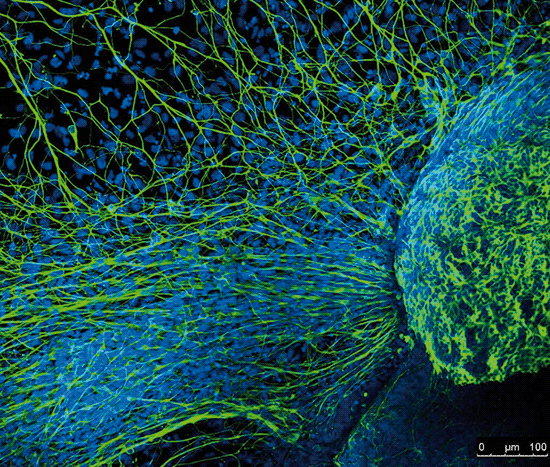
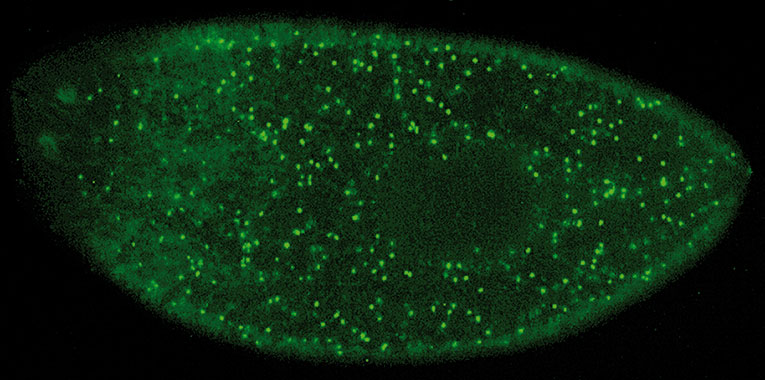
Mitjançant la inserció de cèl·lules indiferenciades, és possible regenerar teixits musculars del cor després de lesions cardíaques. En la imatge, el desenvolupament de miotubs en una regió del miocardi després del tractament amb mioblastos. «Fa 2.500 anys, Anaxàgores i Demòcrit van proposar en la seua teoria de la pangènesi l’existència de cèl·lules especials d’índole germinal (gèmmules), que serien les responsables de la formació de cada òrgan, i tindrien un paper rellevant en l’herència. Aquest últim extrem va ser descartat ben aviat, però el paper formador de les gèmmules recorda encara el de les cèl·lules mare específiques per a cada tipus de teixit.»
Julio López Tornel. Sèrie «Carn de paper», 2010. Aquarel·la, 21 x 29,7 cm. «Desdiferenciar cèl·lules significa aconseguir que cèl·lules diferenciades (cèl·lules adultes incapaces de donar lloc a un altre tipus de cèl·lula, com les de la pell) «obliden» a quin tipus de cèl·lula pertanyen i es transformen en cèl·lules mare pluripotents (capaces de donar lloc a múltiples tipus cel·lulars), que en el laboratori es poden diferenciar artificialment de nou cap a un altre tipus de cèl·lula. Aquest procés es coneix com a clonatge terapèutic: les cèl·lules obtingudes tenen el mateix adn que la cèl·lula originària. Es diferencia del clonatge reproductiu en el fet que aquest últim dóna lloc a un nou individu complet, genèticament idèntic a la cèl·lula que el va originar i al seu organisme d’origen.»
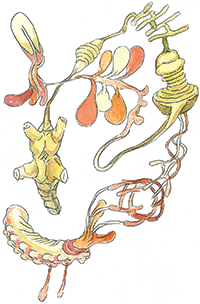
Julio López Tornel. Sèrie «Carn de paper», 2010. Aquarel·la, 21 x 29,7 cm. «Per a Aristòtil, la realitat es configura en potències (el que pot arribar a ser) i actes (el que és). La potència, o capacitat de realitzar un acte, es manté només mentre no es realitza l’acte: només podem triar menjar o no menjar una poma mentre no hem realitzat l’acte de menjar-la. Igualment, en la diferenciació cel·lular, la potència d’originar un tipus cel·lular o un altre es perd a mesura que es diferencia (s’actualitza) el tipus cel·lular al llarg del desenvolupament embrionari. Les cèl·lules mare embrionàries serien potència pura, les cèl·lules adultes diferenciades serien acte pur, mentre que les cèl·lules mare adultes serien un punt intermedi. Desdiferenciar les cèl·lules significa tornar-los la seua potència: el poder arribar a ser altres tipus de cèl·lules.»
Julio López Tornel. Sèrie «Carn de paper», 2010. Aquarel·la, 21 x 29,7 cm. «El trasplantament en la tradició literària, religiosa i cultural es presenta en formes variades: Frankenstein, de Mary Shelley, relata la creació de vida a partir d’òrgans diferenciats, mentre que el Golem, un personatge mític de la tradició jueva, és creat a partir de fang, material no diferenciat, totipotent. També l’Adam cristià és fabricat a partir del fang totipotent en la Bíblia, i es converteix en donant de cèl·lules mare de la seua costella per “fabricar” Eva: la primera clonació reproductiva.»
|
|
El llarg camí al començament
El largo camino al principio