El frau en els assaigs clínics
El cas Bezwoda i el tractament del càncer de mama
El frau dins la investigació científica és un tema poc comentat, malgrat la seua importància. Més encara si es tracta de recerca en temes de salut on els resultats d’un determinat assaig clínic poden suposar un canvi en la forma d’abordar certes malalties.
Alguns casos més cridaners i mediàtics apareixen ocasionalment als mitjans de comunicació, però aquest fenomen requereix uns mecanismes de control adequats per tal de minimitzar-lo o, millor dit, evitar-lo. Molt proper tenim el cas de la biòloga espanyola Susana González, acomiadada del Centre Nacional d’Investigacions Cardiovasculars en 2016 després que es retractaren quatre dels seus articles publicats a Nature i Cell Cycle per presumptes irregularitats en les investigacions sobre cèl·lules tumorals i cardíaques. L’any 2005 el científic nord-americà Eric Poehlman va ser condemnat per malbaratament de fons públics en les seues investigacions fraudulentes sobre una nova teràpia hormonal substitutiva en dones menopàusiques. D’especial rellevància per les seues conseqüències en l’opinió pública és l’exemple de la publicació en 1998 del cirurgià Andrew Wakefield, que relacionava de manera enganyosa l’administració de la vacuna triple vírica amb l’aparició d’autisme.
Un exemple potser menys conegut, però també de gran impacte, és el de Werner Bezwoda en el tractament del càncer de mama a finals de la dècada dels noranta. En el present article, a més d’analitzar aquest cas, ens plantegem com es poden detectar les investigacions basades en dades fraudulentes. Entre tota la recerca que es publica, com podem saber quina té prou evidència i quina s’ha de rebutjar?
Buscant l’evidència en medicina
Com es pot elegir el tractament més adequat en cada moment? Aquesta és una de les preguntes més importants, per no dir la pregunta clau, que es pot fer un professional sanitari davant d’un pacient.
Tot i que des de l’antiguitat s’ha considerat l’exercici de la medicina com una mena d’art, és obvi que es tracta d’una disciplina científica que s’ha de regir per normes objectives i sistemàtiques. D’aquesta forma, el principal objectiu de la investigació relacionada amb la medicina clínica moderna és racionalitzar el coneixement per a predir situacions futures i optimitzar les proves i els tractaments a aplicar. En aquest sentit, des de la meitat del segle XX es desenvolupa i s’aplica el model de medicina basada en l’evidència, el qual consisteix a integrar en l’experiència clínica individual la millor evidència provinent de la investigació científica, després de la seua revisió crítica i exhaustiva.
Aquest model estableix diferents nivells d’evidència i graus de recomanació d’una determinada pràctica, segons la procedència de les dades que donen suport a aquest tipus de tractament (Harbour i Miller, 2001). La principal font d’evidència són les metaanàlisis provinents de les revisions sistemàtiques d’un conjunt d’assaigs clínics d’alta qualitat, és a dir, amb una metodologia correcta i amb baix risc de biaix. Per tant, l’assaig clínic s’ha convertit en la pedra angular de la investigació en biomedicina. No obstant això, aquest mètode d’investigació és una innovació relativament recent, posterior a la Segona Guerra Mundial, i el seu desenvolupament procedeix d’una sèrie d’ajustos ad hoc que han produït un nou estil de pràctica encara obert i en formació (Cambrosio et al., 2006).
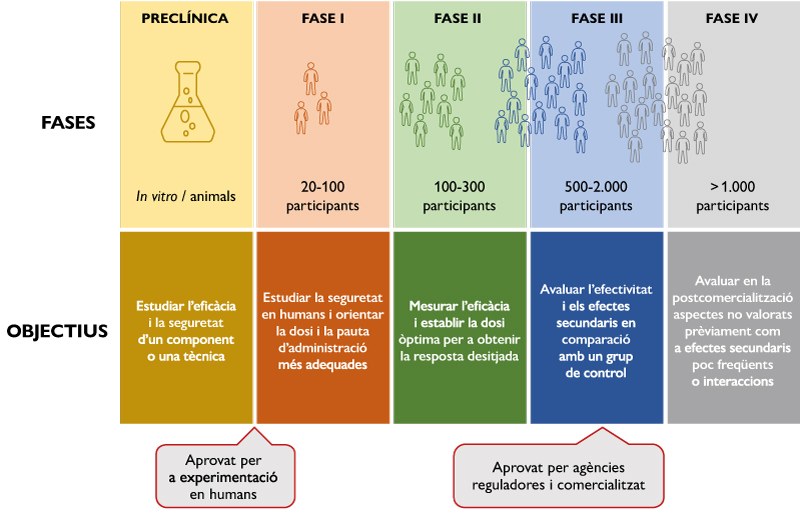
Un assaig clínic és un estudi d’investigació en què es tracta de demostrar quina estratègia de diagnòstic o tractament és millor. Per a dur-lo a terme, s’han de controlar la resta de variables per comprovar que l’efecte observat és només degut a l’acció experimental. També s’han de tindre en compte diferents paràmetres estadístics per a assegurar que els resultats no són deguts simplement a l’atzar. A la figura 1 es poden veure les fases d’un assaig clínic per les quals ha de passar una molècula o estratègia de tractament per a arribar a emprar-se en la pràctica clínica. Cadascuna d’aquestes fases va adreçada a un grup de població; té una metodologia concreta i uns objectius ben diferenciats.
Com qualsevol altre tipus de recerca, aquest model de «creació d’evidència» no està lliure d’inconvenients, com poden ser la possibilitat d’errors en el plantejament i desenvolupament de l’assaig així com la interpretació dels resultats en el context adient. En un pas més enllà, estaria també la possibilitat del frau deliberat per part del personal investigador en la fabricació, falsificació o plagi de les idees.
El càncer de mama i la quimioteràpia a altes dosis
Encara que la supervivència del càncer de mama haja millorat dràsticament des de l’inici dels tractaments oncològics, aquest tipus de tumor és el més freqüent i amb més mortalitat per a la dona a escala mundial.
En la dècada dels setanta s’havia iniciat el desenvolupament dels esquemes de quimioteràpia a altes dosis. Aquesta estratègia de tractament va conduir a una millora important de la supervivència d’alguns càncers agressius, com les leucèmies, els limfomes de mal pronòstic i alguns tumors infantils, i ha continuat perfeccionant-se fins a l’actualitat. Es basa en l’augment de la intensitat de les dosis per a destruir un major nombre de cèl·lules tumorals. I tot i que això és efectiu, també és un procés que ocasiona riscs i en el qual l’efecte advers més important ve determinat per la destrucció massiva d’altres cèl·lules com les de la medul·la òssia. Aquesta aplàsia medul·lar secundària s’ha de recuperar amb el trasplantament de precursors hematopoètics (cèl·lules mare que donen lloc als diversos tipus de cèl·lules sanguínies: glòbuls rojos, blancs i plaquetes), bé del mateix pacient o d’una persona donant compatible. Com és de suposar, a més de resultar molt tòxic, és extremadament car i s’ha d’administrar sols en aquelles situacions en què està correctament indicat.
Durant els anys vuitanta i noranta es va intentar utilitzar aquest tipus de quimioteràpia intensiva per als casos de càncer de mama de pitjor pronòstic i es van dur a terme alguns assaigs de fase II amb resultats prometedors comparats amb controls històrics. Tanmateix, entre 1993 i 1999 es varen publicar quatre estudis de fase III aleatoritzats, els de major evidència científica, que no demostraren diferències entre la quimioteràpia convencional i la d’altes dosis en pacients amb càncer de mama d’alt risc. A diferència d’aquests estudis, l’any 1995 Werner Bezwoda, cap del Servei d’Oncologia i Hematologia de l’Hospital d’Hillbrow (Johannesburg, Sud-àfrica) i professor del Departament de Medicina de la Universitat de Witwatersrand, va publicar al Journal of Clinical Oncology l’únic assaig de fase III que mostrava resultats positius per a aquest tipus de quimioteràpia en càncer de mama metastàtic (Bezwoda et al., 1995).
Tot i que aquest tractament no va arribar a estar recollit en cap guia de pràctica clínica i que la controvèrsia al seu voltant va omplir les revistes i els debats de les societats científiques, durant la dècada dels noranta, milers de pacients amb càncer de mama (més de 40.000 només als EUA) van rebre aquesta modalitat de quimioteràpia amb el trasplantament posterior de medul·la òssia arreu del món. Aquesta ràpida implantació d’un tractament experimental és un tema de gran interès, que ha estat estudiat per diferents autors i en el qual entren en joc, d’una banda, el desconeixement de la comunitat científica sobre quanta evidència és necessària i, d’altra, les diferents pressions socials (que mereixerien un article a banda).
El cas Bezwoda
En l’assaig clínic liderat per Werner Bezwoda es van incloure noranta pacients diagnosticades de càncer de mama metastàtic: la meitat d’elles va rebre un tractament estàndard i l’altra meitat quimioteràpia a altes dosis seguida d’un trasplantament autòleg de medul·la òssia de rescat.
Els resultats de l’estudi foren realment cridaners, ja que en el grup del tractament a altes dosis el percentatge de respostes tumorals completes, és a dir, la desaparició completa del tumor, fou del 51 % enfront del 4 % del grup que va rebre un tractament convencional. A més, es va evidenciar una diferència important en la duració de la resposta aconseguida i un gran augment de la supervivència global amb el tractament del grup experimental. Per altra banda, no van aparèixer efectes secundaris destacables en el grup de quimioteràpia intensiva –més enllà de l’aplàsia medul·lar esperada– i, sorprenentment, les morts degudes al tractament foren més nombroses en el grup amb dosis convencionals. Arran dels resultats, Bezwoda i els seus col·laboradors asseguraren haver demostrat que aquest tractament era un esquema vàlid per a determinades pacients amb càncer de mama.
La controvèrsia al voltant d’aquesta modalitat de quimioteràpia va tindre una gran repercussió en l’oncologia mundial i va provocar multitud de debats i publicacions al respecte (Mello i Brennan, 2001). Tanta va ser la seua importància i tan contradictoris els resultats dels assaigs publicats fins al moment que l’any 1999 es va convocar una reunió sobre el tema a l’Institut Nacional del Càncer dels Estats Units. Es va acordar iniciar un estudi ben dissenyat de fase III i d’abast mundial per tal d’esclarir la situació, però abans es va considerar necessari fer una auditoria sobre els resultats de l’estudi de Bezwoda, l’únic discordant i amb uns resultats més que sorprenents.
Per a dur a terme la investigació, es va designar un equip format per professionals de l’oncologia i la infermeria especialistes en assaigs clínics, que va revisar les dades de les pacients incloses en el treball de Bezwoda. Aquest, com a cap del servei clínic que custodiava les històries clíniques, no es va negar a la realització de l’auditoria, però només va permetre l’accés a les dades originals durant dos dies.
Com a resultat de la investigació, es va descobrir que en l’estudi de Bezwoda s’havien incomplit algunes de les principals normes recollides en la declaració de Hèlsinki i de bona pràctica clínica, que són indispensables per a iniciar un estudi d’aquestes característiques amb humans. Entre altres irregularitats, es va comprovar que cap de les participants havia signat un consentiment informat. A més, el protocol original no es va trobar enlloc, i mesos després el mateix Bezwoda va reconèixer que el protocol definitiu va ser escrit anys després de finalitzar l’estudi.
L’equip revisor tampoc va trobar evidència que s’haguera emprat cap tècnica d’aleatorització per assignar les pacients a un grup de tractament o altre. Per tant, aquest procés estava totalment esbiaixat i invalidava els resultats finals de l’estudi. Però encara es va sorprendre més quan només va poder trobar els historials mèdics de seixanta-una de les noranta pacients incloses. En aquest punt cal recordar que les normes de bona pràctica clínica recomanen la custòdia dels historials clínics de les persones participants en un assaig clínic al voltant de vint anys, inclús en alguns casos més de vint-i-cinc.
Una vegada analitzades les històries clíniques disponibles, sols en la documentació de vint-i-set pacients constava informació suficient per a decidir si eren elegibles per a l’estudi, i únicament nou complien tots els criteris d’inclusió. Tot i que Bezwoda només va reportar una mort en el grup de quimioteràpia intensiva, als historials hi havia evidència que tres pacients reberen el tractament amb xifres de plaquetes i hemoglobina molt baixes i sense constància de cap control posterior, per la qual cosa es pot suposar que van morir al medi extrahospitalari i no es va registrar tal informació. Respecte al seguiment de la resta de les pacients, només set seguien vives després de 1995 i es perdien tots els seguiments posteriors. Addicionalment, un equip d’estadística identificà importants errors en la codificació de les dades i l’anàlisi presentada a l’article.

La investigació del cas va concloure que l’estudi de Bezwoda no aportava dades verídiques. La informació recollida a l’auditoria es va publicar en 2000 a la revista The Lancet i en 2001 a Journal of Clinical Oncology junt amb una retractació de l’article original.
Davant la sospita de frau i amb les proves de l’auditoria, Bezwoda va publicar una carta, de la qual només hi ha algunes referències, on reconeixia la situació:
Jo, W. R. Bezwoda, per la present reconec que he comès una violació greu de l’honestedat i la integritat científica en una presentació realitzada a la Societat Americana d’Oncologia Mèdica […] Reconec el meu error i n’assumisc la plena responsabilitat. […] Demane disculpes a la comunitat científica. (The Cancer Letter, 2000, p. 4)
Posteriorment, Bezwoda va ser expulsat de les institucions on treballava i la Universitat de Witwatersrand va publicar un comunicat aclarint que la mala conducta de l’investigador no tenia res a veure amb la institució, la qual va col·laborar activament amb l’auditoria del cas. Els altres dos autors de l’article, Lesley Seymour i Roger Dansey, es mostraren col·laboradors amb la investigació i reconegueren no conèixer cap de les irregularitats, donat que ells no varen incloure pacients i sols hi van participar com a consultors. És ben curiós que la comunitat científica es va centrar només en el primer autor, que simplement va desaparèixer, i va oblidar les possibles implicacions de la resta de signants que han continuat exercint l’oncologia i dels quals es poden continuar llegint articles publicats en anys posteriors. Tampoc s’ha d’oblidar que l’article va passar el sistema de revisió per part d’una revista molt prestigiosa. Per tant, hem de preguntar-nos també si aquest és un mètode capaç de detectar la possibilitat d’error i frau o si simplement s’ha d’assumir la possibilitat que aquesta mena de desviacions puguen passar desapercebudes. De fet, recentment, i arran del treball retractat en juny de 2020 en què s’assenyalava que la hidroxicloroquina no sols no era un tractament eficaç enfront de la covid-19, sinó que agreujava el risc d’arrítmies i mort intrahospitalària, The Lancet va publicar la modificació de la seua metodologia de revisió d’articles. D’aquesta forma, en aquells estudis amb un gran volum de dades almenys un dels revisors ha de ser especialista en ciència de dades i ha de tindre accés a la informació original per tal d’analitzar-la com una part més del procés d’edició.
Possibilitat d’error i frau científic
L’honestedat i la veracitat són principis fonamentals de la investigació científica i l’adhesió a aquests principis és essencial tant per al progrés de la ciència com per a la percepció pública del treball científic i dels seus resultats. L’incompliment d’aquests principis és considerat com a mala conducta científica o frau, que no és el mateix que un error.
De forma simplificada, allò que té a veure amb un mal plantejament, mesura o anàlisi de les dades a estudi s’anomena error. Però el que es considera una mala conducta o frau té una altra implicació. Com diu el Codi Federal de Regulacions nord-americà:
Les males conductes en investigació inclouen la fabricació, la falsificació i el plagi tant en proposar, realitzar o revisar la recerca com en la forma de donar a conèixer els resultats. […] La mala conducta o frau en la investigació no inclou l’error involuntari o les diferències d’opinió. (Federal Register, 2005, 70(94), p. 28386)
Aquest últim punt és crucial, ja que la diferència entre un error i un frau és la intencionalitat d’enganyar.
Les raons per a cometre frau en investigació clínica varien molt d’un cas a un altre. El frau pot ser degut a l’ambició de prestigi, a interessos financers o a les dificultats per a dur a terme estudis complicats tot i saber que el centre on es duen a terme no està capacitat per a això. En el cas Bezwoda, quina era realment la seua intenció? Podria ser fruit d’un intent massa exagerat que els resultats quadraren amb el que volia que fora la conclusió? Aquest cas podria haver passat més desapercebut si els resultats no hagueren sigut tan espectaculars? Fins a quin punt el «maquillatge» o «processament» de les dades és freqüent a menor escala? I quines han de ser les conseqüències per a la persona que comet frau?
És possible el control absolut?
Com hem vist, aquest model d’evidència està amplament acceptat per la comunitat científica, però, com qualsevol altre, no està lliure de problemes. El que ens hem de plantejar és de quina forma podem intentar disminuir les possibilitats d’error i millorar els mecanismes de control per a evitar els comesos de forma deliberada.
D’entrada, seria convenient mesurar amb quina freqüència es produeixen els diferents tipus d’error i de frau i quina és la seua magnitud, tot i que això és molt difícil de quantificar de forma real.
Finalment, cal destacar que, al marge dels problemes ja coneguts, al mateix temps que evoluciona la investigació es descobreixen noves necessitats i punts febles per als quals s’han de proposar mecanismes reguladors. És ben cert que no es busca substituir l’assaig clínic, però sí opcions que complementen i controlen la forma d’arribar a l’evidència desitjada.
Referències
Bezwoda, W. R., Seymour, L., & Dansey, R. D. (1995). High-dose chemotherapy with hematopoietic rescue as primary treatment for metastatic breast cancer: A randomized trial. Journal of Clinical Oncology, 13(10), 24839. https://doi.org/10.1200/JCO.1995.13.10.2483 (retractació publicada l’1 de juny de 2001, a Journal of Clinical Oncology, 19[11], 2973).
Cambrosio, A., Keating, P., Schlicha, T., & Weisza, G. (2006). Regulatory objectivity and the generation and management of evidence in medicine. Social Science & Medicine, 63, 189–199. https://doi.org/10.1016/j.socscimed.
2005.12.007
Federal Register. (2005). Public Health service policies on research misconduct. U. S. Department of Health and Human Services. Federal Register, 70(94), 28386. https://www.govinfo.gov/content/pkg/FR-2005-05-17/pdf/05-9643.pdf
Harbour, R., & Miller, J. (2001). A new system for grading recommendations in evidence based guidelines. BMJ, 323(7308), 334–336. https://doi.org/10.1136/bmj.323.7308.334
Mello, M., & Brennan, T. A. (2001). The controversy over high-dose chemotherapy with autologus bone marrow transplant for breast cancer. Health Affairs, 20(5), 101–117. https://doi.org/10.1377/hlthaff.20.5.101
The Cancer Letter. (2000). South African investigator Bezwoda admits falsifying data in high-dose chemo study. The Cancer Letter, 26, 1–4. https://cancerletter.com/the-cancer-letter/20000211_1