
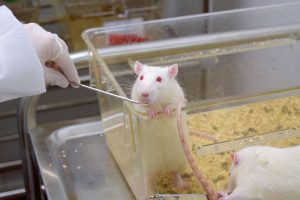
A finals de la dècada dels noranta, un grup de científics de la Universitat McGill del Quebec, a Canadà, va començar a investigar com influeixen les experiències d’infantesa en la capacitat de gestionar l’estrès durant l’edat adulta. Treballaven amb rates, ateses les grans semblances genètiques que tenen amb les persones i al fet que les femelles d’aquesta espècie tenen molta cura de les seves cries. No només les alimenten i els donen calor, sinó que les netegen, les amanyaguen i hi juguen (Figura 1). I durant els primers dies de vida, no les deixen mai soles, només uns minuts de tant en tant per alimentar-se elles. Però ràpidament tornen al seu costat.
L’experiment, publicat el 2004, era molt simple (Champagne et al., 2004). Durant la primera setmana de vida, separaven cada dia les mares de les seves cries tres hores seguides. Els posaven un biberó, perquè la gana no fos un factor d’estrès, i una manteta tèrmica, perquè no passessin fred. Per a les rates, aquest període equival als dos primers anys de vida d’un infant. En fer-se adultes, aquestes rates que s’han sentit desprotegides tres hores cada dia esdevenen molt més reactives i impulsives davant de situacions d’estrès, i són molt menys curioses i sociables que les que no han estat mai separades de les seves mares.
Aquest fet, com s’ha demostrat, correlaciona amb un increment significatiu en l’expressió del gen del receptor de glucocorticoides en una zona molt concreta del cervell, l’hipotàlem. L’hipotàlem està implicat en la consolidació de la memòria i en la resposta hormonal a l’estrès. Tanmateix, quin és el motiu pel qual la sensació de desprotecció durant la infantesa propicia canvis en l’expressió d’aquest gen? I quin significat biològic té? Com es va comprovar una dècada més tard, el motiu cal buscar-lo en les modificacions epigenètiques, que condicionen la funció gènica sense alterar els gens; i el significat biològic és l’adaptació de la funció dels gens a l’entorn concret on es desenvolupa i viu cada individu.
Modificacions epigenètiques: senyals per regular el funcionament del genoma
El genoma humà, com el de tots els mamífers, està format per uns 20.300 gens aproximadament. Totes les cèl·lules d’un individu tenen el mateix genoma, és a dir, el mateix nombre i tipus de gens, i també els mateixos al·lels; és a dir, les mateixes variants gèniques, les quals comporten petites diferències en el missatge que contenen els gens. Tanmateix, no tots els gens funcionen simultàniament en totes les cèl·lules, ni ho fan amb la mateixa intensitat. Els gens s’expressen només on i quan és necessària la seva activitat. Hi ha gens que cal connectar i desconnectar de manera dinàmica i precisa perquè la cèl·lula en qüestió pugui respondre de manera ràpida a les demandes de l’entorn. Altres gens, en canvi, han d’estar permanentment silenciats o alternativament activats en algunes cèl·lules, per tal que aquestes puguin realitzar correctament la seva funció. Per exemple, els gens implicats en la proliferació cel·lular s’han de desconnectar per sempre en les cèl·lules diferenciades, que ja no es reproduiran més.
«Les modificacions epigenètiques no alteren el missatge que contenen els gens; únicament regulen la seva expressió de manera simple i econòmica»
El mecanisme clàssic de regulació de l’expressió gènica (Figura 2), que es coneix des de mitjan segle XX, s’assembla a un interruptor. Perquè un gen es pugui expressar, cal que s’uneixin unes proteïnes específiques a unes regions del DNA que es troben normalment davant la zona codificant del gen. Aquestes proteïnes s’anomenen de forma genèrica factors de transcripció, i les regions del DNA a les quals s’uneixen, intensificadors. Cada gen té els seus propis intensificadors, que indiquen on i quan ha de funcionar, però sense els factors de transcripció adequats, el gen es manté inactiu. En aquest context, els factors de transcripció serien com els dits que premen els interruptors, és a dir, els intensificadors, per fer que un gen concret s’expressi. De la mateixa manera, també hi ha factors de transcripció que actuen de silenciadors i eviten així que el gen corresponent funcioni.
Aquest sistema resulta molt útil quan cal regular de manera dinàmica i ràpida l’expressió dels gens, però resulta energèticament molt costós. Les modificacions epigenètiques permeten abaratir-ho. Aquestes consisteixen en l’addició de molècules concretes a zones específiques del genoma, normalment a l’inici de la zona codificant d’un gen, o bé en les proteïnes histones que acompanyen el DNA per donar-li estabilitat. És com posar un senyal de trànsit de «prohibit circular» en un carrer per evitar que hi passin vehicles, o un de «direcció obligatòria» si volem que tots segueixin un mateix sentit. De la mateixa manera que un senyal de trànsit no altera la forma del carrer o de la carretera on està posat, sinó que únicament regula el flux de vehicles de manera senzilla, les modificacions epigenètiques tampoc alteren el missatge que contenen els gens; únicament regulen la seva expressió de manera simple i econòmica, sense necessitat d’anar sintetitzant factors de transcripció.
Tipus de modificacions epigenètiques
Hi ha diversos tipus de modificacions epigenètiques, segons on s’estableixen. N’hi ha que s’afegeixen directament al DNA, normalment just davant de l’inici de la zona codificant dels gens, en unes seqüències molt concretes de nucleòtids que s’anomenen illes CG –atès que estan formades únicament per nucleòtids citocina (C) i guanina (G)–. Consisteixen en l’addició de grups metil, una molècula química la fórmula de la qual és -CH3, i la seva funció és bloquejar completament l’expressió del gen al qual estan vinculades. Així, quan un gen no s’ha d’expressar més en un tipus cel·lular determinat, es metila. En aquest procés intervenen diversos enzims, que de manera molt controlada s’encarreguen de metilar els gens escaients, les metiltransferases.
La resta de modificacions epigenètiques s’afegeixen a les histones, que són les proteïnes que acompanyen el DNA per donar-li estabilitat estructural i funcional. En aquest cas, la situació és molt més complexa. Les modificacions epigenètiques més habituals que s’estableixen sobre les histones són les acetilacions. Consisteixen en l’addició de grups acetil (-CH3O) en aminoàcids concrets de les histones, els quals actuen de manera completament oposada a les metilacions del DNA. La seva funció és mantenir sempre actiu, és a dir, expressant-se, el gen al qual es troben vinculades. També hi ha diversos enzims que de forma controlada s’encarreguen d’acetilar les histones adequades, les acetilases. A través d’aquest sistema no cal que la cèl·lula vagi produint factors de transcripció per mantenir actius els gens que es troben sota control de les acetilacions, la qual cosa abarateix la regulació, ja que deixa fixats els gens que cal mantenir permanentment actius.
Un dels sistemes cel·lulars on s’ha analitzat amb més profunditat la funció de les metilacions i les acetilacions epigenètiques és la línia hematopoètica, que genera les diverses cèl·lules sanguínies. És un sistema cel·lular molt complex, format per molts tipus cel·lulars diferents (limfòcits, eritròcits, etcètera; vegeu la Figura 3), els quals provenen d’unes mateixes cèl·lules progenitores mitjançant processos de diferenciació successius. A cada procés de diferenciació s’activen o es desactiven uns gens determinats, i la manera d’assegurar que es mantenen activats o silenciats de manera permanent és introduint les modificacions epigenètiques corresponents de manera controlada.
«Les cèl·lules disposen d’una complexa maquinària enzimàtica encarregada d’afegir i també d’eliminar els diversos tipus de modificacions epigenètiques»
Les modificacions epigenètiques que s’estableixen en les histones són, tanmateix, molt més complexes. Les més abundants són les acetilacions, però no són les úniques. Se n’han detectat moltes més, com per exemple grups metil, fosfat, ubiquitina, sumoilina, biotina i poli-ADP ribosina, cascun dels quals té la seva pròpia fórmula química. En aquests casos, la funció reguladora depèn tant de la molècula concreta que s’afegeix com també de l’aminoàcil on s’ha unit en les histones, i actuen en conjunt de manera combinatorial. Això permet que l’activació no sigui una qüestió de tot o res (és a dir, o s’expressa o està silenciat), sinó que introdueix graus en la funcionalitat dels gens. En tots els casos hi ha enzims específics que regulen l’addició d’aquestes molècules de manera estricta.
Què passa quan no s’estableixen de manera correcta?
Les modificacions epigenètiques contribueixen a garantir el funcionament correcte dels programes genètics necessaris per a cada tipus cel·lular. Això implica que els errors epigenètics, és a dir, la manca o l’excés de metilacions o acetilacions, poden ocasionar patologies, degudes al funcionament anòmal dels gens implicats. Un dels casos més ben estudiats, per la seva rellevància sanitària i social, és el de la generació de tumors. Tots els processos cancerosos tenen un origen genètic, atès que impliquen gens que s’expressen en cèl·lules en què no ho haurien de fer, com per exemple els implicats en proliferació cel·lular en cèl·lules diferenciades, o alternativament, gens que han quedat silenciats en cèl·lules en què s’haurien de mantenir actius, com per exemple els anomenats gens supressors de tumors, la funció dels quals és precisament evitar la proliferació incontrolada de cèl·lules diferenciades.
És un dels camps que més fruits està donant en biomedicina. D’una banda, permet una millor diagnosi, la qual va associada a la utilització dels tractaments mèdics més adequats segons quin sigui l’origen genètic o epigenètic de cada procés cancerós. D’altra banda, afavoreix el disseny de nous fàrmacs, alguns dels quals fàrmacs epigenètics, els quals tenen per objectiu revertir les anomalies de l’epigenoma que causen la patologia. En aquests moments hi ha diverses teràpies epigenètiques en ús, que utilitzen molècules com la 5-azacitidina i la 5-aza-20-deoxicitidina per bloquejar les metiltransferases, i altres diverses en assaig.
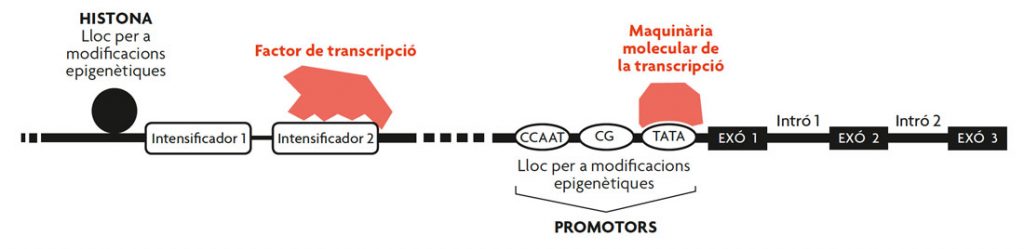
Figura 2. Esquema general de la regulació de l’expressió gènica. Perquè un gen es pugui expressar, cal que s’uneixin unes proteïnes específiques (anomenades genèricament «factors de transcripció») en unes regions del DNA que es troben normalment davant la zona codificant del gen (intensificadors). Les modificacions epigenètiques es poden establir o bé a les histones –proteïnes que acompanyen el DNA per donar-li estabilitat estructural i funcional– o just davant de l’inici a la zona codificant dels gens, en una seqüència concreta de nucleòtids que s’anomena «caixa CG» (atès que està formada per una sèrie de nucleòtids C i G encadenats), la qual es troba entre els anomenats «promotors» (que inclouen altres seqüències com les caixes CCAAT i TATA). A l’esquema es mostren també exons, porcions dels gens que són transcrites i traduïdes i formaran part de l’RNA missatger sintetitzat, i els introns, porcions de gens que, en canvi, seran descartades. / Font: Bueno, D. (2018). Epigenoma para cuidar tu cuerpo y tu vida. Barcelona: Plataforma editorial.
Els processos cancerosos no són les úniques patologies que s’han vinculat a alternacions en l’epigenoma. També s’ha vist que afecten malalties neurodegeneratives com la d’Alzheimer; trastorns cerebrals com esquizofrènia, malaltia bipolar i depressió, i patologies cardíaques i metabòliques, com alguns casos de diabetis de tipus 2, obesitat mòrbida, etcètera. És, per tant, un camp prioritari de recerca en biomedicina.
Com saben les cèl·lules a quins gens han d’incorporar modificacions epigenètiques?
Com s’ha esmentat, les cèl·lules disposen d’una complexa maquinària enzimàtica encarregada d’afegir i també d’eliminar els diversos tipus de modificacions epigenètiques. En alguns casos, s’estableixen de manera absolutament programada, com per exemple durant la diferenciació i la maduració de la línia cel·lular hematopoètica. El mateix succeeix durant la formació i la maduració dels diferents tipus cel·lulars que constitueixen el cos humà, més de 200.
Tanmateix, de vegades no es produeixen de manera programada, sinó que depenen de la interacció amb l’ambient, com en l’exemple amb què he obert l’article, el de les ratetes que se sentien abandonades per les seves mares. En aquest cas, l’estrès que provoca no notar la proximitat física de la mare activa gens relacionats amb la gestió d’aquest estrès, com per exemple el del receptor de glucocorticoides. Inicialment ho fa mitjançant el sistema de factors de transcripció ja esmentat, però si la situació es manté en el temps, el fet que aquest gen es mantingui sobreactivat propicia que s’activi la maquinària enzimàtica de les modificacions epigenètiques. Llavors s’afegiran les molècules corresponents per mantenir aquest gen, o el que correspongui, sobreactivat –o, en altres casos, per mantenir-lo silenciat–. S’han identificat les molècules implicades en aquests processos. És un mecanisme adaptatiu que permet assegurar un funcionament òptim del genoma segons la situació concreta de cada individu, al mateix temps que permet estalviar energia.
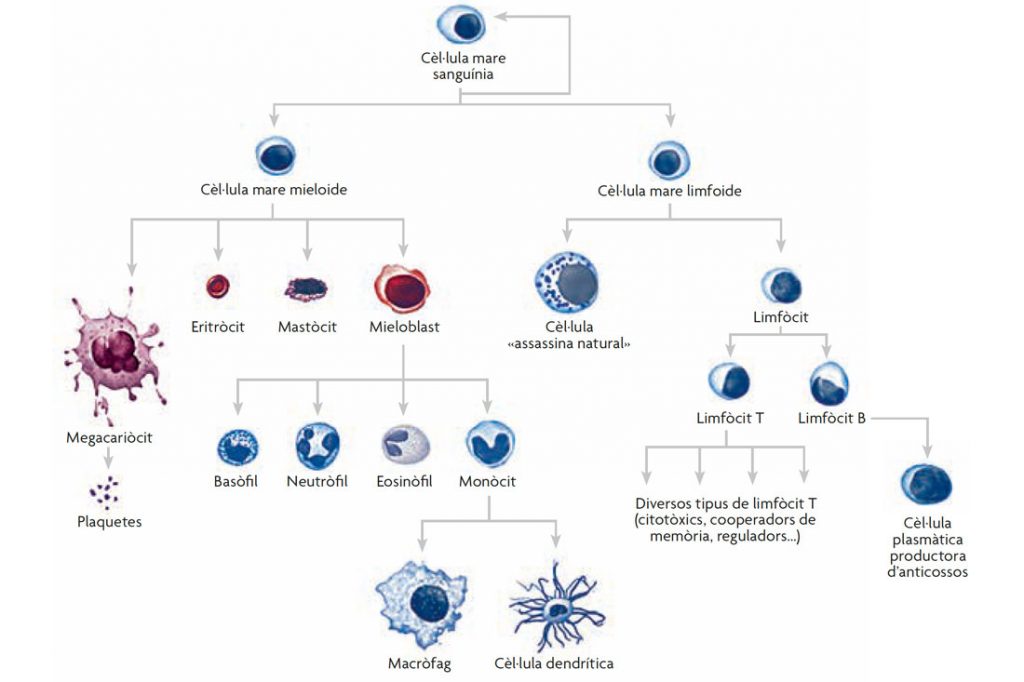
Figura 3. Esquema de l’establiment de la línia cel·lular hematopoètica a partir de cèl·lules mare sanguínies. La diferenciació dels diversos tipus cel·lulars adults implica l’establiment de modificacions epigenètiques específiques que activaran o silenciaran determinats gens de manera permanent. / Font: Bueno, D. (2018). Epigenoma para cuidar tu cuerpo y tu vida. Barcelona: Plataforma editorial.
En el cas de les ratetes, si no hi ha una protecció materna prou eficient, els resulta molt més adaptatiu mantenir el sistema d’estrès sobreactivat, atès que és el mecanisme que permet respondre ràpidament davant qualsevol amenaça que es pugui produir. Dit d’una altra manera, afavoreix la seva supervivència en l’entorn concret on viuen. Ara bé, a diferència del mecanisme de regulació de l’expressió gènica basat en factors de transcripció i en intensificadors, que és molt dinàmic, les modificacions epigenètiques són molt estables, i tendeixen a mantenir-se. Això fa que aquestes ratetes, quan es fan adultes, siguin molt més reactives i impulsives davant de situacions d’estrès, i molt menys curioses i sociables. De fet, aquests trets de comportament resulten avantatjosos en un entorn amenaçador, per evitar perills innecessaris.
Aquest efecte s’ha comprovat també en les persones. Per exemple, s’ha vist que els infants que de petits han patit situacions traumàtiques repetides, com assetjament físic, psicològic o sexual, incorporen modificacions epigenètiques en alguns gens que, de manera adaptativa, els fan més resistents a aquestes situacions, però que en assolir l’edat adulta els fan hiperreactius a les situacions d’estrès i propicien la manifestació d’alguns trastorns cerebrals, com depressió, entre altres. Alguns dels gens que s’ha vist que estan implicats es relacionen amb el cortisol, la vasopressina i l’oxitocina, entre altres hormones i neurohormones.
«De vegades, les modificacions epigenètiques no es produeixen de manera programada, sinó que depenen de la interacció amb l’ambient»
També l’alimentació i l’estil de vida influeixen en les modificacions epigenètiques. Per exemple, s’ha vist que una dieta pobra en aliments que continguin grups químics metil i acetil, indispensables per generar les modificacions epigenètiques necessàries, incrementa la predisposició a patir càncer; que una dieta pobra en proteïnes disminueix la metilació d’alguns gens implicats en el metabolisme dels glícids, els greixos i les proteïnes, i propicia mecanismes inflamatoris; que l’arròs integral conté una molècula, anomenada orynazol gamma, que incrementa la metilació del receptor DRD2 de la dopamina, un neurotransmissor implicat en els sentiments de recompensa, l’aprenentatge i l’optimisme, i que també regula les modificacions epigenètiques de gens que s’expressen al nucli estriat del cervell, una zona que gestiona la sensació de gana, la qual cosa contribueix a disminuir l’obesitat; que un consum excessiu de greixos trans promou modificacions epigenètiques en gens del metabolisme que incrementen la probabilitat de tenir obesitat i diabetis, i que algunes dietes equilibrades, com la mediterrània i la tradicional japonesa, contribueixen a un bon funcionament epigenòmic, entre molts més casos estudiats.
També el fum del tabac (Figura 4) altera les metilacions de més de 700 gens, entre els quals gens supressors de tumors, relacionats amb el sistema immunitari i amb la detoxificació de substàncies oxidants, la qual cosa explica l’increment de probabilitat de manifestar determinats tipus de càncer, una major susceptibilitat a les infeccions i un envelliment més ràpid. De manera similar, altres substàncies que causen addicció, com el cànnabis, la cocaïna i l’alcohol, modifiquen l’epigenoma d’alguns gens relacionats amb el funcionament cerebral, en aspectes com el sentiment de recompensa i la generació i la regulació de les emocions, la qual cosa ajuda a explicar els efectes a llarg termini d’aquestes substàncies sobre el caràcter i el comportament de les persones que en són consumidores

Figura 4. Les substàncies que conté el fum del tabac alteren les metilacions de més de 700 gens, entre els quals gens supressors de tumors, i d’altres relacionats amb el sistema immunitari i amb la detoxificació de substàncies oxidants, fet que repercuteix directament en la salut dels fumadors. / Pixabay
Finalment, per esmentar un parell d’exemples més entre els centenars que hi ha a la literatura científica, s’ha vist que la pràctica esportiva beneficia l’epigenoma de com a mínim 12 gens diferents, entre els quals n’hi ha d’implicats en la funció cardíaca, en el metabolisme i fins i tot en la plasticitat cerebral. També el treball intel·lectual contribueix a establir modificacions epigenètiques que afavoreixen la plasticitat cerebral. I fins i tot l’amistat contribueix a la formació de modificacions epigenètiques en gens relacionats amb la vasopressina, una neurohormona implicada en la gestió de les emocions de por i d’ira, i en l’establiment de relacions socials.
Es poden transmetre als fills? Cal ressuscitar el lamarckisme?
Abans de l’experiment amb què he iniciat aquest article, el dels efectes sobre l’epigenoma del sentiment d’abandonament durant la infantesa, la barbàrie humana en va proporcionar un de resultats completament inesperats (Schulz, 2010). Durant l’hivern de 1944 i 1945, les tropes nazis es batien en retirada a tot Europa, però per motius estratègics i simbòlics s’aferraven a conservar el nord-oest d’Holanda. Van destruir les principals vies de comunicació terrestre i van inundar la major part de camps de cultiu. Aquests fets van coincidir amb un hivern especialment fred, que va gelar els canals que se solien usar per transportar mercaderies. La combinació de tots aquests factors va propiciar la que s’ha conegut com a «gran fam holandesa». A finals de novembre de 1944, la dieta de la major part dels habitants de les grans ciutats holandeses es va reduir a unes 1.000 calories diàries, molt per sota de l’òptim, que se situa entre les 2.300 i les 2.900 calories diàries en els adults actius. A finals de febrer de 1945, la disponibilitat d’aliment havia disminuït fins al punt de proporcionar només 580 calories per dia.
«Substàncies com el cànnabis, la cocaïna i l’alcohol modifiquen l’epigenoma d’alguns gens relacionats amb el funcionament cerebral»
Després d’aquest episodi, el Govern holandès va començar a recopilar meticulosament dades sobre la salut de tots els holandesos, tant dels que havien patit la fam amb tota la seva cruesa com dels que vivien en zones agrícoles on havia estat menys severa. Quan es van analitzar les dades, durant la dècada de 1970, es va observar que les persones nascudes després de la fam de pares que d’adolescents o de nens l’havien patida manifestaven una incidència d’obesitat que duplicava els nivells normals, i tenien una probabilitat molt més alta de manifestar trastorns psiquiàtrics com esquizofrènia i depressió, i també de patir altres patologies com hipertensió, malalties coronàries i diabetis de tipus 2.
El motiu, com es va fer evident a començament de la dècada del 2000, és que tenien modificacions epigenètiques en una sèrie de gens que, si bé els adaptaven a les condicions severes de la fam, per exemple a través de la gestió de l’estrès, al mateix temps propiciaven els trastorns descrits. D’alguna manera, els progenitors havien condicionat les modificacions epigenètiques dels seus descendents encara no concebuts, adaptant-los al que ells havien patit, la qual cosa podria semblar que entronca directament amb la proposta de Lamarck de l’herència dels caràcters adquirits.
Tanmateix, no és aquest el cas, per dos motius crucials. D’una banda, aquestes modificacions epigenètiques no alteren la seqüència del DNA, com seria necessari per a considerar l’herència dels caràcters adquirits. Només afecten la manera com es regulen els gens, a través de modificacions epigenètiques. D’altra banda, després de dues o com màxim tres generacions, si no es mantenen les condicions que les han propiciat (en aquest cas, la fam), aquestes modificacions epigenètiques deixen de transmetre’s, i per tant deixen de formar part de la transmissió genètica. És únicament un mecanisme d’adaptació, que afecta els individus a nivell personal i en alguns casos els seus descendents directes, com a màxim fins a dues generacions. Com va dir Darwin, «la natura és complexa i adaptable». És en aquest context, el de l’adaptabilitat, on cal circumscriure la funció biològica de les modificacions epigenètiques.
«No només es modifica el nostre epigenoma a través de l’estil de vida que duem, sinó que també podem afectar el dels nostres fills»
Corol·lari
La lliçó que ens donen totes aquestes dades és important, atès que les modificacions epigenètiques no només afecten cada individu per ell mateix segons com sigui el seu estil de vida, sinó que també implica una responsabilitat cap a les generacions futures. S’ha vist, per exemple, que el consum de cànnabis durant l’adolescència propicia modificacions epigenètiques en els gàmetes que fan que en el futur els fills que hom pugui tenir manifestin una probabilitat més alta de patir depressió i altres alteracions emocionals durant la seva joventut i l’edat adulta. Així doncs, no només es modifica el nostre epigenoma a través de l’estil de vida que duem, sinó que també podem afectar el dels nostres fills, a través de l’estil de vida que els proporcionem, i fins i tot el dels fills encara no concebuts.
David Bueno és autor del llibre Epigenoma para cuidar tu cuerpo y tu vida (Plataforma Editorial, 2018).
REFERÈNCIES
Champagne, F. A., Chretien, P., Stevenson, C. W., Zhang, T. Y., Gratton, A., & Meaney, M. J. (2004). Variations in nucleus accumbens dopamine associated with individual differences in material behavior in the rat. The Journal of Neuroscience, 24(17), 4113–4123. doi: 10.1523/JNEUROSCI. 5322-03.2004
Schulz, L. C. (2010). The Dutch Hunger Winter and the developmental origins of health and disease. PNAS, 107(39), 16757–16758. doi: 10.1073/pnas.1012911107





