
L’Assemblea General de l’ONU va proclamar el 2011 com l’Any Internacional dels Boscos i l’Any Internacional de la Química, dues commemoracions que són el detonant de la nostra col·laboració en aquest número de primavera. Ajudades pel nostre assessor químic i autor de la secció La ciència a taula en Mètode, Fernando Sapiña, hem preparat una activitat que reuneix les dues celebracions: un sorprenent bosc químic.
L’Any Internacional dels Boscos resultarà útil per a prendre major consciència del fet que els boscos són part integrant del desenvolupament sostenible del planeta gràcies als beneficis econòmics, socioculturals i ambientals que proporcionen. Espanya té 14,4 milions d’hectàrees de boscos, fet que converteix el nostre país en el quart d’Europa amb majors recursos forestals després de Suècia, Finlàndia i França. El 88% de la superfície forestal d’Espanya té com a funció principal la protecció contra l’erosió del sòl i la desertificació, així com la regulació del cicle hidrològic. El 12% restant són boscos productius, que subministren gran part de la fusta que consumeix Espanya.
Per la seua banda, l’Any Internacional de la Química se celebra enguany sota el lema «Química: la nostra vida, el nostre futur». Els objectius d’aquesta commemoració són diversos: incrementar l’apreciació pública de la química com a eina fonamental per satisfer la necessitat de la societat, promoure l’interès per la química entre els joves i generar entusiasme pel futur creatiu de la química. Tot açò quan es compleixen cent anys del premi Nobel de Química atorgat a Marie Curie.
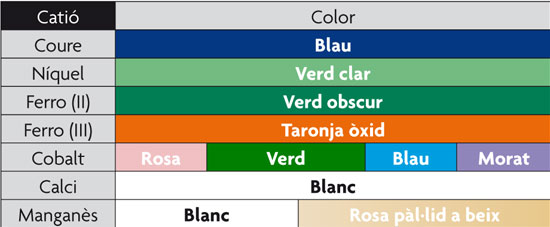
En aquest quadre es mostren els colors que aconseguiràs utilitzant cadascuna de les sals de metalls enumerades en la llista de materials.
Activitat: Crear un bosc químic
Aquesta versió del bosc químic l’hem experimentada i la presentem amb les possibilitats reals de fer-la.
Què és el que passa?
1. Quan posem en contacte cristalls d’una de les sals, per exemple, de clorur de cobalt (color vi), amb una dissolució de silicat sòdic (vidre líquid) en aigua, el cristall es comença a dissoldre i els cations (+) cobalt reaccionen amb els anions (–) silicat per formar un gel de silicat de cobalt (color blau).
2. A mesura que entra l’aigua en la zona interior del gel per òsmosi, es dissol el cristall, augmenta la pressió interna i, en un moment donat, el gel es trenca: pel punt de ruptura ix cap afora la dissolució de clorur de cobalt.
3. Com que aquesta dissolució és menys densa que la dissolució de silicat, es desplaça cap amunt des del punt de ruptura. La reacció entre els cations cobalt i els anions silicats produeix de nou més gel de silicat de cobalt. Així es van formant tubs de diferents grandàries, colors i formes, en funció de la natura de la sal afegida, cap a dalt del pot, tubs que recorden troncs d’arbres, i la combinació dels distints troncs evoca la imatge d’un bosc. També podeu aprofitar per conèixer el concepte d’òsmosi i les claus de l’experiment d’Arquímedes.
Materials
—Silicat de sodi (vidre líquid o vidre soluble). És fàcil de trobar a drogueries i botigues de pintures.
—Got de vidre reciclat.
—Proveta o got mesurador.
—Aigua destil·lada.
—Sals de metalls en pols o granulades: Sulfat de coure pentahidratat (Cu S O4, 5H2 O), sulfat de níquel heptahidratat (Ni S O4, 7H2 O), sulfat de ferro (II) heptahidratat (Fe S O4, 7H2 O), clorur de ferro (III) (Fe Cl3), clorur de cobalt hexahidratat (Co Cl2 , 6H2 O), clorur de calci (Ca Cl2 ) o sulfat de manganès monohidratat (Mn S O4, H2 O).

Alguns exemples de resultats de l’activitat.
Procediment
—Preparem la solució amb dues mesures d’aigua per una de silicat. Cal anar amb cura, el silicat es diu vidre líquid i quan s’asseca pot tallar.
—Ho barregem bé.
—Amb una espàtula, empolvorem la sal distribuint-la pel pot.
—Aquesta s’enfonsarà i començarà a créixer. Es pot repetir amb una altra en un altre pot. Pots experimentar!
—Després d’uns segons, començaran a créixer com uns fils, semblants a brins d’herba. Depenent de la sal, es formen diferents estructures i diferents colors (vegeu el quadre).
—Després de 30 minuts, el bosc ha completat el seu creixement.
Advertència. Aquesta solució no es conserva bé a l’aire lliure i s’ha de tapar amb un film de plàstic transparent en acabar. Tampoc s’ha d’introduir mai en un aquari, ja que és molt perjudicial per als peixos.
Si voleu conservar el bosc es pot canviar el silicat per oli corporal. Si coleu el silicat per llevar-li impureses, podeu reutilitzar-lo una altra vegada.
Per saber-ne més:
Science amusante.
Science and Plants for Schools.
WikiCiencia.





