Vigilants mediambientals
La fauna salvatge, sentinella de la contaminació mediambiental per resistència als antimicrobians a Catalunya

El creixent increment de resistències als antimicrobians (RAM) tant en éssers humans com en el bestiar s’atribueix en gran manera a l’ús excessiu o incorrecte d’aquests tractaments. L’alarmant aparició d’aquestes resistències en la medicina humana i veterinària ha impulsat el desenvolupament de diversos estudis de monitoratge dels nivells de contaminació RAM en el medi ambient. En aquest document es descriu l’aparició de gens de resistència als antibiòtics d’últim recurs en medicina humana, en una àmplia diversitat d’animals salvatges. Se suggereix que la fauna salvatge pot ser un bon sentinella de la contaminació ambiental per RAM, especialment en àrees molt poblades. D’altra banda, els animals salvatges també poden contribuir a la propagació de bacteris i gens RAM en el medi ambient i representar un risc zoonòtic per a les persones que hi estiguen en contacte estret.
Paraules clau: resistència als antimicrobians, gens de resistència a betalactàmics, Catalunya, gens resistents a la colistina, fauna salvatge.
En les últimes dècades, la prevalença de bacteris oportunistes i resistents als antimicrobians (BRAM) associades a les infeccions nosocomials ha augmentat considerablement en entorns intrahospitalaris. L’ús excessiu i el mal ús dels antibiòtics en la medicina humana i veterinària ha provocat la propagació de patògens resistents als antimicrobians (RAM), la qual cosa suposa un problema de salut global (Pitout i Laupland, 2008). L’alarmant aparició de RAM en la medicina humana i veterinària ha impulsat la realització de diversos estudis per a monitorar els nivells de RAM en el medi ambient. La implementació urgent de mesures de control basades en el marc d’una sola salut és necessària per a reduir l’impacte antropogènic sobre el medi ambient. S’ha suggerit que la fauna salvatge pot ser un bon sentinella de la salut ambiental per la seua proximitat amb les poblacions humanes, els animals domèstics i els ecosistemes naturals. Però a més, els animals salvatges poden actuar com a portadors asimptomàtics de patògens zoonòtics a llarg termini (Tsiodras et al., 2008), tant de virus (com la grip o el virus del Nil Occidental) com de bacteris (per exemple, Salmonella spp., Campylobacter spp. o Staphylococcus aureus resistent a la meticil·lina) o paràsits (com Cryptosporidium spp.). Per tant, poden contribuir a propagar aquests patògens entre el bestiar i fins i tot a les àrees urbanes, i incrementar, així, el risc d’infecció per als animals i els éssers humans.
Les β-lactamases d’espectre ampliat (BLEA) i les β-lactamases de tipus AmpC (ampC) són els enzims més comuns que incrementen la resistència antibiòtica a les cefalosporines d’espectre ampli entre els enterobacteris. Aquestes β-lactamases (bla) s’han diversificat àmpliament en resposta a l’ús clínic de medicaments de nova generació: cefalosporines, carbapenèmics i monobactàmics. Els enzims β-lactamases es poden classificar en tres grups. El primer conté les cefalosporinases codificades en el cromosoma de molts enterobacteris, com ampC, blaCMY, blaACT, blaFOX i blaMIR. Algunes variants d’aquests enzims s’han detectat també en plasmidis. El segon grup, les serina β-lactamases, és el de major grandària d’espectre ampli contra les penicil·lines, cefalosporinrs i carbapenèmics. Inclouen els enzims blaTEM, blaSHV, blaCTX, blaOXA i blaKPC. Aquests enzims estan codificats principalment en gens de plasmidis que es poden transferir horitzontalment a diferents gèneres de bacteris. Finalment, el tercer grup, les metalobetalactamases, depenen del zinc i inclouen els enzims blaNDM, blaIMP, blaVIM i blaSPM. L’aparició de la resistència als carbapenèmics –medicaments d’últim recurs utilitzats en entorns hospitalaris per a tractar infeccions greus provocades per enterobacteris resistents als antibiòtics betalactàmics– ha compromès les opcions terapèutiques per a la salut humana (Tzouvelekis et al., 2012). Especialment la variant OXA-48 de les carbapenemases és cada vegada més comuna entre les infeccions clíniques humanes a Europa (Grundmann et al., 2017).
Un altre antibiòtic humà d’últim recurs és la colistina. Els gens mòbils de resistència a la colistina (mcr) són gens de resistència mediats per plasmidis descoberts recentment en humans i animals destinats a l’alimentació (Skov i Monnet, 2016). Se sap que els gens mcr confereixen resistència al sulfat de colistina –un dels últims medicaments efectius contra els bacteris gramnegatius multiresistents (MDR, per les sigles en anglès de multi drug resistance)– (Sun et al., 2018). La colistina s’ha utilitzat en la medicina veterinària en les últimes dècades per a tractar les infeccions gastrointestinals del bestiar, principalment els porcs i l’aviram (EMA, 2016), però també de manera massiva per a la prevenció de la colibacil·losi en garrins. En conseqüència, el bestiar es considera el principal reservori de selecció i propagació de gens mcr a escala global. Avui dia existeix una tendència mundial a limitar l’ús de la colistina en la producció animal per aquesta gran preocupació en salut pública relacionada amb l’emergència i transmissió de gens resistents (Sun et al., 2018).
Estudis de la resistència als antimicrobians en la fauna salvatge de Catalunya
La propagació de β-lactamases d’ampli espectre s’ha estudiat profundament en els enterobacteris humans i del bestiar, però encara necessitem més estudis sobre la seua presència en el medi ambient i la fauna salvatge. Catalunya compta amb aproximadament 7,8 milions d’habitants, amb una densitat de població de 242,3 habitants per quilòmetre quadrat. La comunitat autònoma té una gran densitat de granges de bestiar, principalment porcí, i lidera la producció espanyola de carn de porc amb un rècord de 32,8 milions d’animals en 2020, un increment del 5 % respecte a l’any anterior, segons dades d’Eurostat.
En aquest context, els animals salvatges atesos en el Centre de Recuperació de Fauna Salvatge de Torreferrussa (localitzat als voltants de Barcelona) han sigut objecte de diferents estudis epidemiològics. Es va examinar tots els animals amb bastonets rectals o cloacals a la seua arribada al centre, abans de rebre qualsevol tractament farmacològic o antimicrobià. La causa d’hospitalització més freqüent estava relacionada amb factors antropogènics relacionats amb la persecució directa (ferides de bala, enverinaments, captivitat il·legal o paranys) o amb amenaces humanes involuntàries (col·lisions amb vehicles, tancaments o electrocució). Els mètodes de mostreig i els protocols de gestió dels animals es van adequar a les estipulacions del Servei de Fauna (Generalitat de Catalunya) en els seus protocols i principis ètics i a la legislació espanyola.
Ocells silvestres
Els primers estudis realitzats van revelar una prevalença significativa de bacteris resistents als antimicrobians en rapinyaires salvatges que mai havien rebut tractament antimicrobià. En concret, les anàlisis del 10 % i el 7,4 % dels rapinyaires salvatges van donar positiu, respectivament, en salmonel·la resistent a múltiples medicaments i en soques de Campylobacter resistents a les quinolones (Molina-López et al., 2011). Entre la gran diversitat de serotips de salmonel·la descoberts en l’estudi, destacava la Salmonel·la Typhimurium multiresistent DT104, resistent a l’ampicil·lina, el cloramfenicol, l’estreptomicina, la sulfonamida i la tetraciclina (ACSSuT), que es va trobar en aligots comuns (Buteo buteo) i mussols (Athene noctua).
En un altre estudi, el 6,3 % de rapinyaires (Bubo bubo, Tyto alba, Strix aluco, Falco tinnunculus, Gyps fulvus) també van donar positiu en salmonel·la, amb una predominança de la variant S. Typhimurium monofàsica 4,12:i:-, el perfil de la qual mostra resistència a l’ampicil·lina, l’estreptomicina, les sulfonamides i la tetraciclina (ASSuT), extensiu a la colistina i el cloramfenicol en alguns casos aïllats (Molina-López et al., 2015). A Europa, les soques monofàsiques se solen caracteritzar per un perfil de resistència ASSuT, i hi ha proves que els senglars (Sus scrofa) són probablement un dels reservoris de soques d’aquesta mena de fags a Espanya (Mateu et al., 2002) i Catalunya (Mejía et al., 2006).
D’altra banda, la freqüència d’aïllats de Campylobacter resistents a les fluoroquinolones sembla respondre consistentment a la pressió local selectiva d’antimicrobians. La presència de soques aïllades resistents a les quinolones en els altres ocells salvatges pot ser deguda a la ingestió de preses. A més, en espècies amb hàbits alimentaris carronyers, com el voltor comú (G. fulvus), la ingestió directa de residus d’antibiòtics i bacteris resistents als antibiòtics de la carronya del bestiar o de cadàvers d’animals salvatges contagiats podria ser una font d’infecció.
La implementació d’anàlisis de genotipatge va permetre fer un pas avant en l’estudi de la resistència antimicrobiana en la fauna silvestre. D’aquesta manera, en 2019 es va alertar (per primera vegada a Espanya) sobre la presència de gens de resistència a les cefalosporines en una gran varietat d’enterobacteris en mamífers –principalment eriçons i mustèlids– i ocells salvatges –sobretot rapaços– (Darwich et al., 2019). Significativament, la prevalença general de bacteris oportunistes i resistents als antimicrobians en l’estudi va ser del 13 % (17,3 % en mamífers salvatges i 11,5 % en ocells salvatges). Entre els mamífers, la major prevalença es va trobar en els eriçons (13,5 %); entre els ocells, va ser en els rapinyaires (7,3 %). La majoria de BRAM aïllades en aquesta fauna silvestre contenien una gran diversitat de gens resistents (50 % blaCMY-2, 23 % blaSHV-12, 20 % blaCMY-1 i 18 % blaCTX-M-15) trobats habitualment en les infeccions nosocomials dels hospitals humans, com ara Escherichia coli, Klebsiella pneumoniae, Citrobacter freundii, Enterobacter cloacae, Serratia marcescens i Proteus mirabilis.
Eriçons
L’eriçó comú (Erinaceus europaeus) és una espècie salvatge comuna i estesa a Europa. Els eriçons són insectívors petits, nocturns i coberts d’espines que viuen en una àmplia varietat d’hàbitats, generalment en contacte pròxim amb els humans, però també amb el bestiar en les zones rurals. En els últims anys, les poblacions d’eriçons ocupen cada vegada més zones amb activitat humana, com ara els jardins de les àrees residencials o les zones verdes de les grans ciutats. Algunes de les conseqüències d’aquesta interacció entre eriçons i humans és que se’ls sol alimentar, la qual cosa augmenta el risc de contacte físic. Per tant, realitzem un estudi amb una cohort d’eriçons comuns de la mateixa zona de Catalunya. Els resultats van mostrar que un 36,8 % dels espècimens eren portadors de gens RAM, amb una especial recurrència dels bacteris nosocomials humans amb gens BLEA i AmpC. A més, K. pneumoniae era el bacteri amb una major proporció de gens de resistència, seguida d’E. coli i C. freundii. Els gens detectats amb major freqüència també van ser blaCTX-M-15 (19,3 %), blaSHV-28 (10,5 %), blaCMY-1 (9,7 %), i blaCMY-2 (8,8 %). És interessant destacar que més de la meitat dels enterobacteris presentaven el fenotip multiresistent (MDR) amb un perfil ampliat de resistència estesa (XDR) en un 30 % dels aïllats. A més, hem descrit la presència de gens de la variant de carbapemenasa OXA-48 en enterobacteris d’eriçons que habiten zones urbanes molt poblades de Catalunya (Darwich et al., 2019; Garcias et al., 2021). Com que els carbapenèmics no estan permesos en els animals destinats a l’alimentació, la creixent presència de gens que codifiquen les carbapenemases en el bestiar, les mascotes i els animals salvatges és una alarmant prova de la contaminació ambiental antropogènica.

Podem trobar una possible explicació per a la major prevalença de gens de resistència als betalactàmics en els eriçons en els seus hàbits d’alimentació i ubicació. És a dir, ha d’estar relacionada amb l’exposició a aigües residuals o sòls contaminats amb bacteris resistents als antimicrobians i residus d’antibiòtics. S’ha demostrat que els cucs, un component biològic clau del sòl, contribueixen a propagar la resistència als antimicrobians en adquirir antibiòtics directament de la terra. Per tant, tenint en compte que la major part de la dieta dels eriçons consisteix en cucs i altres invertebrats, aquests mamífers es poden veure més exposats a aquestes substàncies antibiòtiques i gens de resistència que altres espècies animals (Garcias et al., 2021).
Senglars
Amb el mateix objectiu d’investigació, es va examinar la presència d’E. coli amb gens BLEA, així com altres patògens zoonòtics, en senglars (n = 200) que s’alimenten en l’àrea metropolitana de Barcelona. Les poblacions de senglars estan augmentant a un ritme constant a tot el món. Això és un motiu de preocupació, perquè els senglars s’han identificat com un reservori de zoonosis i de patògens, que reben a través de la seua alimentació. D’altra banda, són bons sentinelles per a monitorar l’impacte antropogènic del consum de productes alimentaris en les zones urbanes. Els resultats d’aquest estudi mostraren que el 8 % dels animals eren portadors de gens de resistència a les β-lactamases: blaCMY-2 (3,0 %), blaTEM-1b (2,5 %), blaCTX-M-14 (1,0 %), blaSHV-28 (1,0 %), blaCTX-M-15 (0,5 %) i blaCMY-1 (0,5 %). A més, es va detectar Clostridioides difficile toxigènic TcdA+ en dos exemplars per primera vegada a Espanya. Aquests resultats indiquen el gran valor de l’espècie com a sentinella dels bacteris resistents i d’agents zoonòtics en entorns urbans. De fet, els senglars que s’alimenten en localitzacions urbanes i periurbanes estaven més exposats a fonts de bacteris resistents a antimicrobians que els que habitaven entorns naturals. En concret, els gens de resistència betalactàmica es van aïllar amb major freqüència en els senglars urbans i periurbans (14 % de prevalença) que en els que habitaven al bosc (2 % de prevalença) (Darwich et al., 2021).
Animals semiaquàtics
Els estudis amb espècies salvatges d’ocells i mamífers han mostrat que aquests poden ser reservoris de vectors potencials per a la propagació de bacteris i gens de resistència als antimicrobians (Darwich et al., 2019). No obstant això, encara tenim poques dades sobre el paper dels animals semiaquàtics com a sentinelles de la salut ambiental. Per aquesta raó, l’estudi més recent del nostre equip es va centrar en la presència de bacteris i gens amb resistència antimicrobiana en animals semiaquàtics d’àrees urbanes molt poblades i zones de ramaderia intensiva de Catalunya, principalment de producció porcina i avícola (Mengistu et al., 2022).
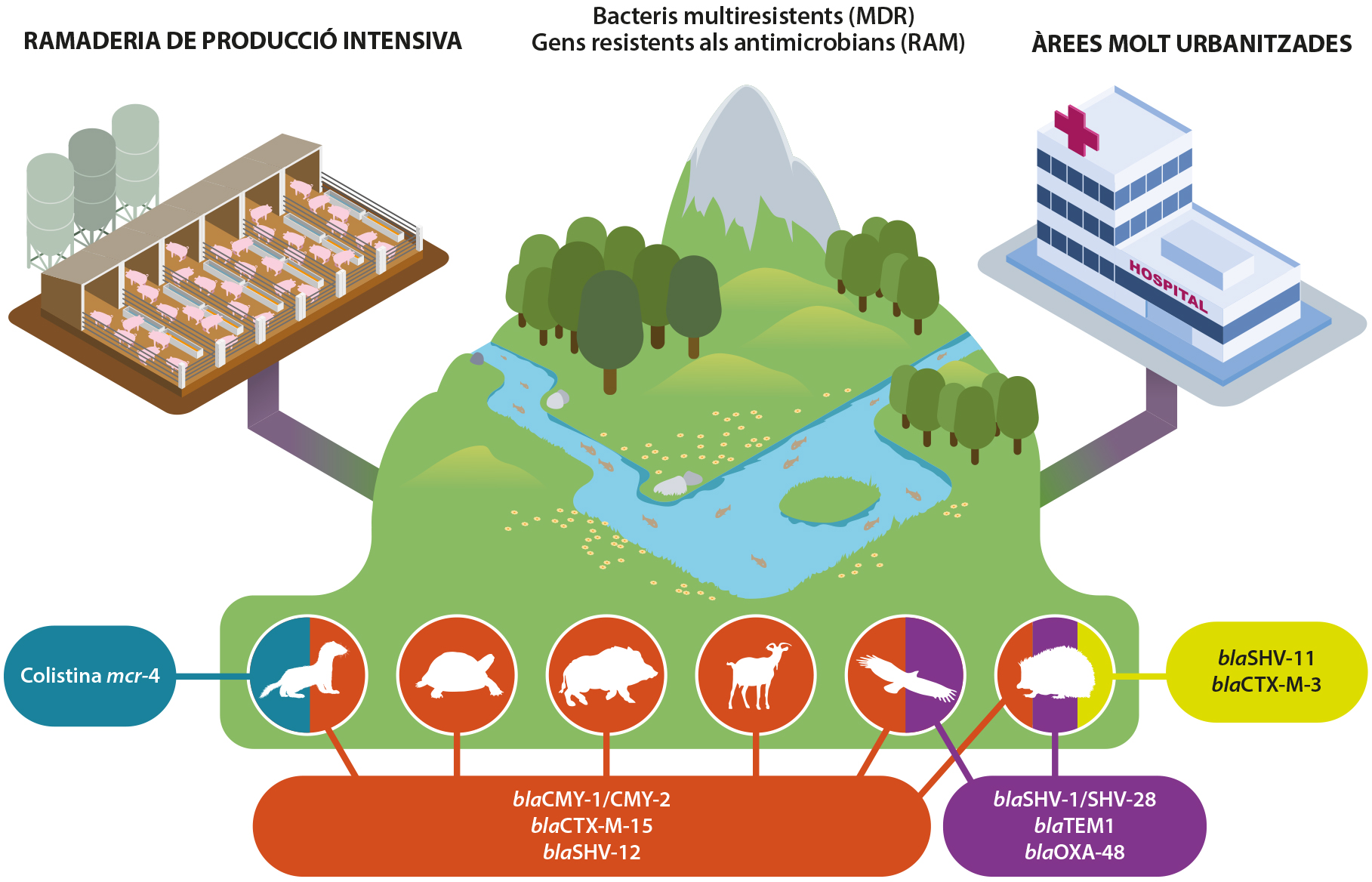
Es van recollir mostres d’espècies invasores com ara la tortuga de Florida (Trachemys scripta) i visó americà (Neovison vison) amb bastonets cloacals i rectals. En els resultats, el 55,2 % dels aïllats es van identificar com BRAM. E. coli i Pseudomonas fluorescens eren alguns dels bacteris més presents en els aïllats de totes les espècies, però altres agents nosocomials com ara K. pneumoniae, Salmonella spp. o C. freundii també eren comuns. Les proves de susceptibilitat fenotípica mostraren que la major resistència era davant els macròlids i els β-lactàmics. A més, els gens BLEA/Ampc eren presents en un 15,4 % de les tortugues i un 8,4 % dels visons americans. La freqüència genotípica va ser: tetM (20,6 %), blaCMY-2 (13 %), ermB (6,1 %), blaCMY-1 (4,6 %), blaCTX-M-15 (3,1 %) i mcr-4 (0,8 %). Les tortugues tenen una major prevalença de bacteris multiresistents (MDR) i gens resistents a antimicrobians que els mustèlids, encara que el gen de resistència a la colistina mcr-4 es va detectar en els visons. La distribució de gens de resistència als β-lactàmics, l’eritromicina, la tetraciclina i la colistina es concentrava en les àrees metropolitanes de les grans ciutats i en regions amb una gran producció porcina. Específicament, la major freqüència d’animals positius en gens BLEA/ampC es va trobar en àrees poblades de les grans ciutats (amb grans hospitals) i la major freqüència d’animals amb gens de resistència a la tetraciclina i l’eritromicina (tetM/emrB) o del gen mcr-4 de resistència a la colistina es va trobar en àrees amb una intensa producció ramadera (Mengistu et al., 2022).
En general, s’ha informat de la presència dels gens mcr, principalment mcr-1 a tot el món, en enterobacteris aïllats d’humans, bestiar, mascotes, aliments i fauna salvatge (Skov et al., 2016). Els gens de resistència a la colistina més freqüents trobats en enterobacteris porcins a Espanya són mcr-1 i mcr-4 (Aguirre et al., 2020; Vidal et al., 2020). Per tant, la presència de mcr-4 en la K. pneumoniae d’un visó americà que habite en una de les zones amb la major densitat de bestiar porcí és un resultat coherent. L’abús del sulfat de colistina en la producció porcina en el passat com a mètode preventiu per a controlar la diarrea després del deslletament podria ser la causa de la pressió selectiva de bacteris resistents a la colistina. De fet, entre 2013 i 2015, Espanya va ser el país europeu amb majors vendes de polimixines per als animals destinats a l’alimentació (EMA, 2016), amb una prevalença significativa dels gens de resistència a la colistina, principalment mcr-4 (Aguirre et al., 2020). L’Agència Espanyola de Medicaments i Productes Sanitaris va establir una reducció dràstica (97 %) de l’ús de colistina en porcs entre 2015 i 2018, amb un impacte positiu en la disminució de gens de resistència a aquesta (Aguirre et al., 2020). No obstant això, la presència d’aquests gens en aigües naturals suggereix que la reducció en l’ús d’aquest antimicrobià no és suficient per a evitar la selecció genètica en porcs vius o que la contaminació del riu prové de gens mcr estables en purins antics no tractats. Per tant, els animals semiaquàtics són bons sentinelles de la contaminació ambiental (de les aigües, en aquest cas) per gens i bacteris amb resistència als antimicrobians.
Un important motiu de preocupació
La majoria dels gens β-lactamases d’espectre ampli detectats en la fauna salvatge catalana també es poden trobar amb freqüència en entorns hospitalaris, la qual cosa suggereix que existeix una relació entre els bacteris dels animals salvatges i els centres sanitaris (Figura 1). A més, aquesta prevalença de bacteris nosocomials humans amb gens de resistència als β-lactàmics en les poblacions salvatges que viuen prop d’aquestes àrees urbanes és un gran motiu de preocupació, perquè aquests animals no han rebut mai tractament amb antibiòtics; és a dir, la presència de gens amb resistència antimicrobiana ha d’estar relacionada amb la seua exposició a aigües residuals o a sòls contaminats o amb residus antimicrobians. Les plantes de tractament d’aigües no són del tot eficients en l’eliminació de residus antibiòtics i bacteris resistents a antimicrobians (Karkman et al., 2018), i l’aigua contaminada arriba als rius i les mars. A més, el fem utilitzat en els sembrats també en conté (Han et al., 2021) i enriqueix el resistoma tant del sòl com de l’aigua (Zhou et al., 2020).
La relació entre nivells de resistència antimicrobiana en l’entorn i la seua presència en humans és complexa: hi ha múltiples combinacions d’antimicrobians, soques bacterianes, elements genètics mòbils (EGM) i espècies silvestres, i cada una té les seues pròpies dinàmiques. Un estudi recent (Wee et al., 2020) centrat en la relació entre bacteris resistents en humans i en el bestiar ha mostrat que la transferència horitzontal de gens amb resistència antibiòtica per mitjà d’EGM com els plasmidis estén la interconnexió entre l’humà i el bestiar més enllà de la transmissió clonal. És més, la investigació genòmica ha revelat gens amb resistència antimicrobiana i elements mòbils molt relacionats en llinatges bacterians humans i del bestiar.
Potencialment, la seqüenciació genòmica d’alta resolució pot ser una eina poderosa que ens ajude a comprendre millor les vies de propagació de bacteris resistents a antimicrobians, o com se’n transmet la resistència d’humans a animals salvatges i viceversa. Això serà clau per a desenvolupar polítiques efectives d’administració antimicrobiana i control de les infeccions per a millorar la salut humana-animal-ambiental.
La urgència de l’enfocament d’una sola salut
En conclusió, la fauna silvestre asimptomàtica sense cap registre de tractament antibiòtic pot ser portadora de bacteris resistents als medicaments humans o veterinaris i funcionar com a reservoris i sentinelles d’aquests bacteris resistents. La fauna silvestre també pot representar un risc zoonòtic per al personal dels centres de recuperació de fauna salvatge i per a la població general en contacte pròxim i continu amb aquests animals. En conseqüència, és crucial sensibilitzar la ciutadania sobre la forta interconnexió entre hàbitats i la seua relació per múltiples rutes d’intercanvi, raó per la qual els problemes relacionats amb la resistència antimicrobiana han d’afrontar-se des d’una sola salut. I a més, és urgent adoptar aquest enfocament en regions densament poblades i amb una producció ramadera intensiva.
Referències
Aguirre, L., Vidal, A., Seminati, C., Tello, M., Redondo, N., Darwich, L., & Martín, M. (2020). Antimicrobial resistance profile and prevalence of extended-spectrum beta-lactamases (ESBL), AmpC beta-lactamases and colistin resistance (mcr) genes in Escherichia coli from swine between 1999 and 2018. Porcine Health Management, 6, 4–9. https://doi.org/10.1186/s40813-020-00146-2
Darwich, L., Seminati, C., López-Olvera, J. R., Vidal, A., Aguirre, L., Cerdá, M., Garcias, B., Valldeperes. M., Castillo-Contreras, R., Migura-Garcia L., Conejero, C., & Mentaberre, G. (2021). Detection of beta-lactam-resistant Escherichia coli and toxigenic Clostridioides difficile strains in wild boars foraging in an anthropization gradient. Animals, 11, 1585. https://doi.org/10.3390/ani11061585
Darwich, L., Vidal, A., Seminati, C., Albamonte, A., Casado, A., Lopez, F., Molina-López, R. A., & Migura-Garcia, L. (2019). High prevalence and diversity of extended-spectrum β- lactamase and emergence of OXA-48 producing Enterobacterales in wildlife in Catalonia. PLOS One, 14(8), e0210686. https://doi.org/10.1371/journal.pone.0210686
EMA. (2016). Updated advice on the use of colistin products in animals within the European Union: Development of resistance and possible impact on human and animal health. http://www.ema.europa.eu/docs/en_GB/document_library/Press_release/2016/07/WC500211081.pdf
Garcias, B., Aguirre, L., Seminati, C., Reyes, N., Allepuz, A., Obón, E., Molina-Lopez, R. A., & Darwich, L. (2021). Extended-spectrum b-lactam resistant Klebsiella pneumoniae and Escherichia coli in wild European hedgehogs (Erinaceus europeus) living in populated areas. Animals, 11, 2837. https://doi.org/10.3390/ani11102837
Grundmann, H., Glasner, C., Albiger, B., Aanensen, D. M., Tomlinson, C. T., Andrasević, A. T., Cantón, R., Carmeli, Y., Friedrich, A. W., Giske, C. G., Glupczynski, Y., Gniadkowski, M., Livermore, D. M., Nordmann, P., Poirel, L., Rossolini, G. M., Seifert, H., Vatopoulos, A., Walsh, T., … EuSCAPE working group. (2017). Occurrence of carbapenemase-producing Klebsiella pneumoniae and Escherichia coli in the European survey of carbapenemase-producing Enterobacteriaceae (EuSCAPE): A prospective, multinational study. The Lancet Infectious Diseases, 17, 153–163. https://doi.org/10.1016/S1473-3099(16)30257-2
Han, B., Yang, F., Tian, X., Mu, M., & Zhang, K. (2021). Tracking antibiotic resistance gene transfer at all seasons from swine waste to receiving environments. Ecotoxicology and Environmental Safety, 219, 112335. https://doi.org/10.1016/j.ecoenv.2021.112335
Karkman, A., Do, T. T., Walsh, F., & Virta, M. P. J. (2018). Antibiotic-resistance genes in waste water. Trends in Microbiology, 26(3), 220–228. https://doi.org/10.1016/j.tim.2017.09.005
Mateu, E. M., Martin, M., Darwich, L., Mejia, W., Frias, N., & Garcia Peña, F. J. (2002). Antimicrobial susceptibility of Salmonella strains isolated from swine in Catalonia, Spain. The Veterinary Record, 150, 147–150. https://doi.org/10.1136/vr.150.5.147
Mejía, W., Casal, J., Zapata, D., Sánchez, G. J., Martín, M., & Mateu, E. (2006). Epidemiology of Salmonella infections in pig units and antimicrobial susceptibility profiles of the strains of Salmonella species isolated. The Veterinary Record, 159, 271–276. https://doi.org/10.1136/vr.159.9.271
Mengistu, T. S., Garcias, B., Castellanos, G., Seminati, C., Molina-Lopez, R. A., & Darwich, L. (2022). Occurrence of multidrug resistant Gram-negative bacteria and resistance genes in semi-aquatic wildlife–Trachemys scripta, Neovison vison and Lutra lutra–as sentinels of environmental health. Science of the Total Environment, 830, 154814. https://doi.org/10.1016/j.scitotenv.2022.154814
Molina-López, R. A., Valverdú, N., Martin, M., Mateu, E., Obon, E., Cerdà-Cuéllar, M., & Darwich, L. (2011). Wild raptors as carriers of antimicrobial-resistant Salmonella and Campylobacter strains. The Veterinary Record, 168(21), 565. https://doi.org/10.1136/vr.c7123
Molina-López, R. A., Vidal, A., Obón, E., Martín, M., & Darwich, L. (2015). Multidrug-resistant Salmonella enterica serovar Typhimurium monophasic variant 4,12:i:- isolated from asymptomatic wildlife in a Catalonian wildlife rehabilitation center, Spain. Journal of Wildlife Diseases, 51(3), 759–763. https://doi.org/10.7589/2015-01-019
Pitout, J. D., & Laupland, K. B. (2008). Extended-spectrum beta-lactamase-producing Enterobacteriaceae: An emerging public-health concern. The Lancet Infectious Diseases, 8(3), 159–166. https://doi.org/10.1016/S1473-3099(08)70041-0
Skov, R. L., & Monnet, D. L. (2016). Plasmid-mediated colistin resistance (mcr-1 gene): Three months later, the story unfolds. Eurosurveillance, 21, 30155. https://doi.org/10.2807/1560-7917.ES.2016.21.9.30155
Sun, J., Zeng, X., Li, X., Liao, X., Liu, Y., & Lin, J. (2018). Plasmid-mediated colistin resistance in animals: Current status and future directions. Animal Health Research Reviews, 18, 136–152. https://doi.org/10.1017/S1466252317000111
Tsiodras, S., Kelesidis, T., Kelesidis, I., Bauchinger, U., & Falagas, M. E. (2008). Human infections associated with wild birds. The Journal of Infection, 56, 83–98. https://doi.org/10.1016/j.jinf.2007.11.001
Tzouvelekis, L. S., Markogiannakis, A., Psichogiou, M., Tassios, P. T., & Daikos, G. L. (2012). Carbapenemases in Klebsiella pneumoniae and other Enterobacteriaceae: An evolving crisis of global dimensions. Clinical Microbiology Reviews, 25, 682–707. https://doi.org/10.1128/CMR.05035-11
Vidal, A., Aguirre, L., Seminati, C., Tello, M., Redondo, N., Martín, M., & Darwich, L. (2020). Antimicrobial resistance profiles and characterization of Escherichia coli strains from cases of neonatal diarrhea in Spanish pig farms. Veterinary Sciences, 7(2), 48. https://doi.org/10.3390/vetsci7020048
Wee, B. A., Muloi, D. M., & van Bunnik, B. (2020). Quantifying the transmission of antimicrobial resistance at the human and livestock interface with genomics. Clinical Microbiology and Infection, 26(12), 1612–1616. https://doi.org/10.1016/j.cmi.2020.09.019
Zhou, S., Zhu, D., Giles, M., Daniell, T., Neilson, R., & Yang, X. R. (2020). Does reduced usage of antibiotics in livestock production mitigate the spread of antibiotic resistance in soil, earthworm guts, and the phyllosphere? Environment International, 136, 105359. https://doi.org/10.1016/j.envint.2019.105359