Construint cervells capaços d’evolucionar
Reptes i perspectives de la neurobiologia evolutiva del desenvolupament
La biologia evolutiva del desenvolupament (també coneguda com evo-devo, de l’anglès evolutionary developmental biology) consisteix a comparar les trajectòries de desenvolupament completes de les espècies, i no sols les formes adultes. Aquest enfocament ha reeixit pel que fa a la morfologia general, però encara és bastant innovador aplicat a la neurobiologia. Fins avui, el camp on la neurobiologia evolutiva del desenvolupament ha obtingut més èxits ha estat en l’ús de dades comparatives referides al desenvolupament per a determinar les homologies adultes. La perspectiva més apassionant és l’ús d’aquestes dades per a comprendre com apareixen les diferències en les estructures i funcions adultes. En aquest sentit, un «sistema model» molt interessant és l’estudi de per què el neocòrtex es plega en algunes espècies però no en altres.
Paraules clau: cervell, evolució, desenvolupament, homologia, plegament cortical.
Segons em van ensenyar, el truc per a fer ciència de la bona és trobar un conjunt de preguntes que siguen alhora interessants i resolubles amb els mètodes actualment disponibles (Medawar, 1967). I també vaig aprendre que aquest conjunt de preguntes tendeix a canviar amb el temps, a mesura que les preguntes més antigues van trobant resposta o van perdent brillantor i nous mètodes donen peu a noves preguntes. Considerant aquestes lliçons, periòdicament faig balanç d’on ha transcorregut el meu camp d’investigació i cap a on es dirigeix. Aquest assaig reflecteix aquests pensaments, encara que estiga escrit amb una perspectiva més àmplia i examine la situació actual i les expectatives de la neurobiologia evolutiva del desenvolupament, un camp que compagina l’estudi de l’evolució del cervell amb el del desenvolupament d’aquest mateix òrgan.
La biologia evolutiva dels desenvolupament dens de la biologia general
Durant bona part del segle xx, la biologia evolutiva va estar sotmesa a un punt de vista que bàsicament oblidava el desenvolupament i que tractava el canvi evolutiu com si els adults ancestrals s’hagueren transformat directament en descendents adults. Per exemple, en els tan difosos gràfics de l’evolució del cavall es mostren els petits adults ancestrals com a versions de formes adultes molt més grans. El fet que cada cavall adult evolucionara des d’un embrió i deixara descendència que va haver de créixer abans d’assolir l’edat adulta es considerava en gran manera irrellevant per a la història evolutiva. A mesura que avançava el segle XX, els biòlegs evolucionistes es van anar interessant cada vegada més pel mecanisme que guia els canvis evolutius subjacents a la morfologia adulta, però se centraven quasi exclusivament en els canvis en les freqüències gèniques o al·lèliques i menystenien quasi sempre el paper dels gens en el desenvolupament orgànic. Com Theodosius Dobzhansky, un dels fundadors de la síntesi moderna de la biologia evolutiva, va assenyalar el 1951: «L’estudi dels mecanismes de l’evolució pertany a l’àmbit de la genètica de poblacions» (citat en Gilbert, Opitz i Raff, 1996). Així doncs, la síntesi moderna combinava la genètica de poblacions amb la morfologia comparada clàssica, però feia poc o cap ús de l’embriologia.
«La síntesi moderna combinava la genètica de poblacions amb la morfologia comparada clàssica, però feia poc o cap ús de l’embriologia»
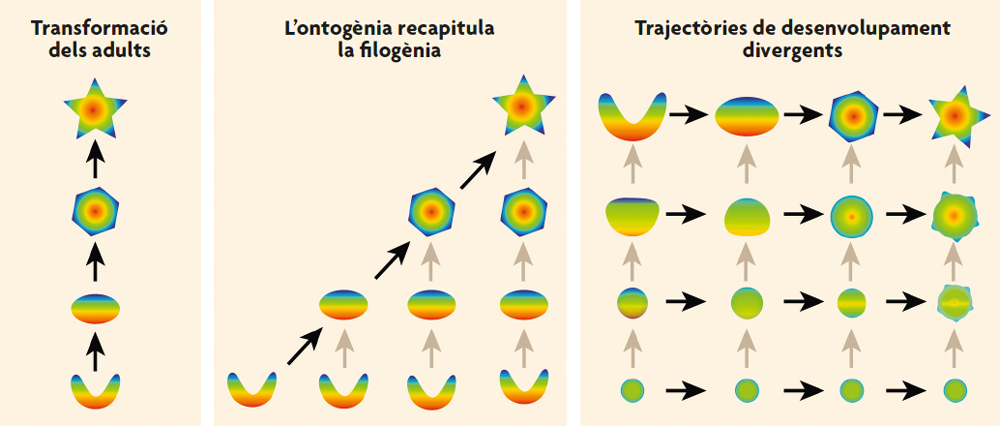
Probablement una raó d’aquesta omissió va ser que Ernst Haeckel i els seus deixebles a finals del segle xix van caure en l’error de simplificar excessivament la relació entre el desenvolupament (ontogènesi) i el canvi evolutiu (filogènesi). Argumentaven que, en l’evolució dels organismes individuals, aquests passaven pels estadis adults dels seus avantpassats o, per dir-ho en poques paraules, que «l’ontogènia recapitula la filogènia» (Gould, 1977). Des d’aquest punt de vista, el desenvolupament dels embrions de mamífers passa per etapes en què tenen brànquies, que es correspondrien amb les brànquies dels antics peixos i amfibis a partir dels quals van evolucionar els mamífers. Per a Haeckel, que els mamífers adults no conserven aquestes brànquies és simplement perquè continuen desenvolupant-se fins que es transformen en altres estructures, com la mandíbula i els ossos de l’orella mitjana. En essència, Haeckel i els seus seguidors pensaven que el canvi evolutiu només es devia a l’addició de noves etapes al final de l’ontogènesi d’un avantpassat. Si això fóra cert, llavors el desenvolupament embrionari de cada espècie passaria per les etapes adultes dels seus avantpassats seguint un ordre cronològic.
En tot cas, el plantejament de Haeckel era massa limitat. Una gran quantitat de dades embrionàries ens mostra ara que les transformacions evolutives a vegades impliquen la supressió d’etapes ancestrals adultes (de vegades aquest procés s’anomena pedomorfosi) o, més sovint, canvis en el desenvolupament que es donen a mitjan camí, abans que els avantpassats arriben a l’estadi adult. L’últim punt de vista, sobre el desenvolupament com a divergència entre espècies, es remunta a Karl Ernst von Baer a mitjan segle xix i per tant és anterior al principal treball de Haeckel, però va tenir una difusió lenta, tal vegada perquè Von Baer s’havia oposat tenaçment a la teoria de l’evolució de Darwin. En tot cas, sempre que la trajectòria de desenvolupament d’una espècie descendent acaba prematurament o divergeix de la del seu antecessor, el desenvolupament individual no pot recapitular la filogènia (figura 1). En compte de l’ontogènia que recapitula la filogènia, el patró més comú és que les diferents espècies s’assemblen bastant entre si durant algunes etapes primerenques del desenvolupament embrionari (el que se sol dir l’estadi filotípic) i que després divergesquen a mesura que van creixent. Així doncs, els estats embrionaris dels mamífers en realitat no presenten brànquies sinó que tenen fenedures faríngies que s’assemblen bastant a les d’altres embrions de vertebrats. Quan aquestes fenedures faríngies es desenvolupen (i les barres que hi ha entre elles), adopten diferents formes en distints llinatges de vertebrats.
Un segon problema amb la teoria de Haeckel era que considerava el desenvolupament com el mecanisme que dirigeix el canvi evolutiu. Aquest punt de vista és coherent amb la idea de Haeckel segons la qual tots els canvis en el desenvolupament d’un individu es poden transmetre a la seua descendència (és a dir, l’herència dels caràcters adquirits), però era difícil d’integrar en la síntesi moderna de la biologia evolucionista, ja que en aquesta síntesi les diferències en el desenvolupament es consideraven com el resultat de l’evolució, no com la causa. Com hem dit, els creadors de la síntesi moderna consideraven els canvis en les freqüències al·lèliques com el motor del canvi evolutiu; les relacions causals entre els gens i el desenvolupament van continuar en la foscor i van caure en l’oblit.
«La biologia evolutiva del desenvolupament es pot aplicar amb profit a l’evolució de becs, extremitats, aletes i ossos, així que per què no provar si funciona amb el cervell?»
Aquesta situació va canviar a final del segle XX, quan la biologia del desenvolupament es va orientar cada vegada més cap a l’àmbit molecular i es va dedicar a explorar i manipular l’expressió gènica en embrions. Una vegada que aquest treball es va basar en les comparacions i que aquestes es van estendre més enllà d’un selecte grup d’«espècies model», va ser possible estudiar els mecanismes moleculars subjacents a la divergència evolutiva en el desenvolupament. Aquest treball va permetre que la biologia del desenvolupament s’anara integrant en la biologia evolutiva, com a complement de la genètica de poblacions, i que nasquera la biologia evolutiva del desenvolupament (Gilbert et al., 1996). Aquest camp novell es va expandir ràpidament i continua florint avui dia, com mostren les revistes especialitzades i els panels d’avaluació de projectes de recerca.
També jo vaig caure fascinat per la biologia evolutiva del desenvolupament en els vuitanta. M’atreia la idea d’introduir-me en els mecanismes moleculars del canvi evolutiu i comparar l’ontogènia de diferents espècies, identificar els canvis evolutius específics en les trajectòries de desenvolupament, correlacionar tots aquests canvis morfològics amb els canvis en l’expressió gènica i, finalment, manipular experimentalment per a «recrear» aquells canvis evolutius en el laboratori. Em van impressionar, per exemple, els experiments que induïen el creixement de dents en embrions de pollastre (Kollar i Fisher, 1980), encara que fa milions d’anys que les aus van perdre les dents adultes. Més recentment, em va meravellar una investigació que comparava el desenvolupament del bec en diversos pinsans de les illes Galápagos i provava una hipòtesi sobre els mecanismes moleculars subjacents en aquesta variació mitjançant la manipulació del desenvolupament del bec en embrions de pollastre (Abzhanov, Protas, Grant, Grant i Tabin, 2004). Nombrosos treballs d’aquest tipus han provat ara que l’estudi de la biologia evolutiva del desenvolupament es pot aplicar amb profit a l’evolució de becs, extremitats, aletes i ossos. Però em preguntava si podria funcionar amb el cervell, si la tremenda complexitat del cervell faria arrere els neurobiòlegs evolutius del desenvolupament. En certa manera va ser així, almenys al començament. No obstant això, la neurobiologia evolutiva del desenvolupament ha avançat considerablement en els últims anys i promet progressar encara més en el futur.
La neurobiologia evolutiva del desenvolupament
Fins ara, la majoria dels neurobiòlegs especialitzats en evo-devo no s’han dedicat a explicar les diferències cerebrals entre espècies, sinó a buscar similituds inesperades i críptiques. En aquesta tasca han destacat Luis Puelles i els seus col·laboradors (per exemple en Puelles et al., 2000). Aquests autors van comparar els patrons d’expressió de nombrosos gens en cervells d’embrions de mamífers i aus, així com en algunes espècies d’altres grups de vertebrats, i van descobrir que aquests patrons són molt semblants entre aquestes espècies, a pesar de tenir un cervell adult molt diferent, especialment el prosencèfal. Aquests descobriments encaixen amb el patró general de divergència en el desenvolupament (millor que la recapitulació) que he exposat anteriorment. D’altra banda, les similituds en l’expressió gènica d’embrions han permès a Puelles et al. (2000) inferir nombroses homologies –caràcters equivalents que es poden remuntar a un origen evolutiu únic– que no han trobat explicació fins que les formes adultes han deixat de ser les úniques que es tenien en compte. El mateix enfocament general s’ha aplicat també per a establir homologies entre les principals regions cerebrals de vertebrats i invertebrats (Holland, Holland, Williams i Holland, 1992; Denes et al., 2007).
«La majoria dels neurobiòlegs especialitzats en evo-devo no s’han dedicat a explicar les diferències cerebrals entre espècies, sinó a buscar similituds inesperades i críptiques»
Encara que les similituds en l’expressió gènica embrionària han ajudat a aclarir unes poques homologies, moltes continuen essent controvertides. Una de les raons d’aquests debats aparentment interminables és que no tots els gens són igual de bons com a «indicadors d’homologia». Els més útils són els gens que s’expressen només en les estructures d’interès i que se sap que participen en el desenvolupament i el destí adult (Medina, Abellán i Desfilis, 2013). Quan no disposem d’aquests indicadors ideals, la millor opció és analitzar l’expressió de molts gens diferents –si pot ser, tot el transcriptoma– i posteriorment comparar les espècies estadísticament. Estadístiques diferents poden presentar resultats diferents, però l’enfocament estadístic és certament preferible a centrar-se només en els gens que abonen o contradiuen una hipòtesi en particular, la qual cosa seria com triar només el que ens dóna la raó. Aquestes comparacions de transcriptoma ja s’han aplicat a les regions cerebrals d’adults, però probablement es produiran avenços significatius quan aquestes anàlisis s’amplien a les regions cerebrals embrionàries. Al cap i a la fi, com dèiem abans, entre els embrions de distintes espècies el cervell és en general més semblant que en el cas dels adults. D’altra banda, els gens que s’expressen durant el desenvolupament embrionari tendeixen més a participar en les xarxes de regulació de gens que es creu que especifiquen la «identitat d’un caràcter».
Una vegada s’han identificat les homologies en les regions cerebrals, ja es poden correlacionar les diferències en el nivell i l’extensió espacial de l’expressió gènica embrionària amb les diferències entre espècies que presenta la morfologia cerebral adulta. Per exemple, en el meu laboratori hem vist que els lloros adults tenen un mesencèfal extraordinàriament petit, en comparació amb el d’altres aus, i que aquesta diferència en els individus adults es correlaciona amb diferències d’espècie en el patró d’expressió d’un gen que està implicat en el desenvolupament del mesencèfal (McGowan, Kuo, Martin, Monuki i Striedter, 2011). De la mateixa manera, altres científics han demostrat que, en un grup de peixos teleostis, les diferències que mostren els adults en la grandària d’algunes àrees del prosencèfal es correlacionen amb diferències entre espècies en l’expressió dels gens implicats a establir el patró del cervell anterior. De fet, la manipulació de l’expressió d’aquests gens pot recrear (fenocòpia) algunes de les diferències entre espècies que presenten els individus adults (Sylvester et al., 2010).
«La ciència és insaciable, vol respondre totes les preguntes, però, en cada moment donat, només pot reeixir a respondre alguns interrogants»
El que continuen sense explicar aquests estudis és la causa molecular de les diferències entre espècies en l’expressió gènica embrionària. Com va alterar l’evolució la regulació d’aquests gens? Es van afegir o eliminar alguns gens o seqüències reguladores d’ADN a les xarxes reguladores de gens ja existents? Respondre a aquestes preguntes és sovint difícil perquè els elements de regulació gènica poden estar localitzats bastant lluny dels gens regulats. D’altra banda, algunes diferències en l’expressió gènica poden ser degudes a canvis en l’ADN que no impliquen canvis en la seqüència d’ADN, és a dir, que es tractaria de modificacions epigenètiques, però que no obstant això es poden transmetre entre generacions.
Aquestes qüestions sense resoldre poden entrebancar el progrés de la neurobiologia evolutiva del desenvolupament, però seria un error argumentar que només la genòmica i l’epigenòmica poden donar una explicació mecanicista al canvi evolutiu en la morfologia cerebral. Al cap i a la fi, el desenvolupament cerebral es pot estudiar mitjançant diferents nivells d’anàlisi –des de la regulació gènica fins a la formació de teixits– i cada nivell es pot considerar un «mecanisme causal» per dret propi. Per exemple, el meu treball ha demostrat que l’expansió del telencèfal en lloros i ocells canors, comparada amb la d’altres aus, és deguda a un retard evolutiu en neurogènesi, la qual cosa incrementa el nombre de cèl·lules precursores del telencèfal (Charvet i Striedter, 2009). Desconeixem el mecanisme molecular que subjau en aquest canvi durant el procés de la neurogènesi, però el nostre descobriment és mecanicista. La biologia és una disciplina que s’organitza jeràrquicament, i cada especialista tendeix a estudiar un nivell diferent; per això el que per a un científic és un mecanisme, per a un altre és un fenomen que necessita explicació. A la llarga, la ciència és insaciable, vol respondre totes les preguntes, però, en cada moment donat, només pot reeixir a respondre alguns interrogants. Com resumim en la següent secció, un model excel·lent per a il·lustrar aquesta naturalesa multinivell de la neurobiologia evolutiva del desenvolupament és el plegament del neocórtex en el cervell d’una part dels mamífers.
El plegament cortical: un sistema model per a la neurobiologia evolutiva del desenvolupament
La major part del còrtex cerebral, el neocòrtex, mostra plecs o solcs complexos en els humans i en altres mamífers amb grans cervells. De fet, quasi tots els cervells de mamífers que superen els deu grams solen tenir un neocòrtex amb plecs, al contrari que els cervells més petits. D’altra banda, el grau de plecs corticals s’incrementa previsiblement amb l’àrea de la superfície cortical (especialment quan aquesta àrea es multiplica per l’arrel quadrada de la grossària cortical). En general, aquestes dades indiquen que hi ha una relació causal entre l’evolució del plegament cortical i el creixement evolutiu en l’àrea del neocòrtex. Dit d’una altra manera, el plegament neocortical va evolucionar a mesura que es va incrementar l’extensió del neocòrtex dels mamífers més enllà d’un cert llindar.
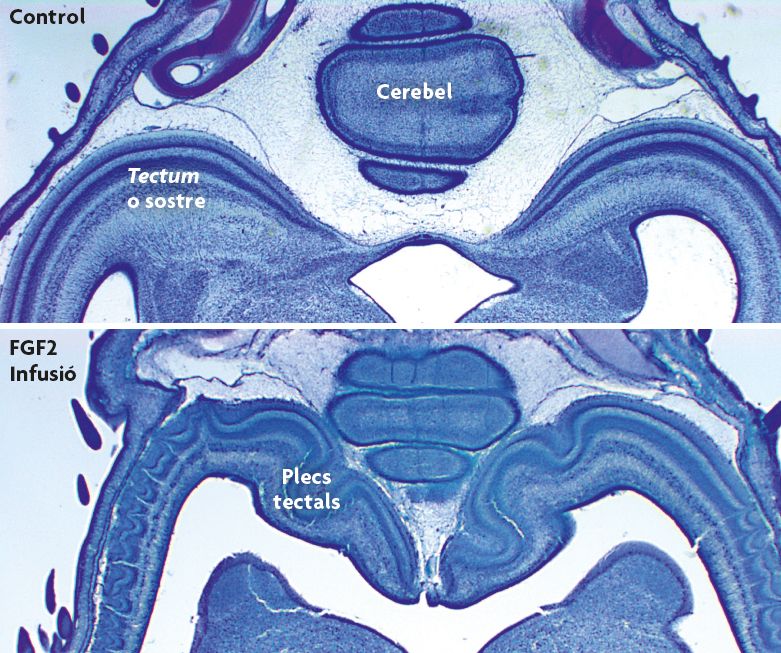
Figura 2. Plegament induït experimentalment en el sostre òptic (tectum) d’aus. La injecció del factor de transcripció FGF2 en els ventricles cerebrals d’embrions de pollastres retarda la neurogènesi tectal i, en conseqüència, es força el sostre òptic a créixer en volum i, especialment, en superfície (McGowan et al., 2011). Sorprenentment, un tectum més gran desenvolupa nombrosos plecs, la qual cosa no passa en el tectum normal. Hem suggerit que aquests plecs induïts són el resultat directe de l’increment en l’expansió tangencial del tectum, procés que genera forces mecàniques deformadores. / Georg F. Striedter
La importància de la funció del plegament cortical és objecte de debat. És clar, però, que sense els solcs, el neocórtex formaria un enorme globus ple de líquid i que això complicaria el part i dificultaria l’equilibri del cap sobre el coll. A més, el plec cortical permet que els àxons que connecten diferents regions del neocòrtex entre si i amb la resta del cervell siguen més curts que si el neocòrtex fóra llis i tinguera forma de globus. Reduir al mínim la longitud dels àxons, al seu torn, estalvia energia metabòlica i incrementa la velocitat a què les neurones de diferents àrees del cervell es poden comunicar. Aquests avantatges funcionals suggereixen que el plegament cortical té origen adaptatiu, és a dir, que la seua evolució hauria incrementat les probabilitats de supervivència i de reproducció dels individus. Aquesta explicació «adaptacionista» de l’evolució del plegament cortical no involucra el desenvolupament (no és evo-devo), però sí que és mecanicista; sense solcs els grans neocòrtex no haurien evolucionat (llevat que hagueren abandonat l’organització cortical en forma de làmina).
«Seria un error argumentar que només la genòmica i l’epigenòmica poden donar una explicació mecanicista al canvi evolutiu de la morfologia cerebral»
Des de la perspectiva evo-devo, el plec cortical és un fenomen del desenvolupament que requereix una explicació basada en el desenvolupament: Per què el neocòrtex, que és llis en les primeres etapes de desenvolupament, comença a plegar-se en aquelles espècies en què el neocòrtex adult presenta plecs? Quin tipus de forces generen els plecs? Començàrem a pensar seriosament sobre aquesta qüestió en el meu laboratori després de manipular embrions de pollastre perquè desenvoluparen un sostre òptic o tectum més ampli. Per a la nostra sorpresa, vam descobrir que, amb l’eixamplament d’aquest tectum es desenvolupaven diversos plecs (figura 2; McGowan et al., 2012). Encara que estàvem treballant amb aus i no amb mamífers, i estudiant el tectum i no el neocòrtex, vam començar a sospitar que devia existir algun principi general que podria explicar el plegament del teixit en diferents estructures i espècies.
Guiats per aquesta idea i basant-nos en l’extensa bibliografia sobre el plegament cortical, vam proposar que en els mamífers aquest és degut sobretot a forces que deformen el neocòrtex i que es generen quan l’estrat cel·lular del neocòrtex embrionari, denominat placa cortical, s’expandeix i augmenta en superfície, tangencialment, més ràpidament que el teixit situat per sota (Striedter, Srinivasan i Monuki, 2015). Com mostren els models que s’han estudiat, aquesta expansió diferencial produeix el plec una vegada que l’expansió ha superat el llindar de deformació, que depèn de la grossària i la rigidesa de les diferents capes. Mecanismes addicionals, com la tensió que crea el creixement dels àxons, poden influir en el lloc concret en què es formen els plecs. Vist aquest conjunt de causes, la raó per la qual el còrtex es plega més en unes espècies que en altres és que la placa cortical s’expandeix molt més (en àrea, no en espessor) en les espècies amb còrtex més plegat (figura 3). Com més creix, en relació amb el teixit de sota, major és la força de la deformació i més es plega el còrtex.
Així doncs, com s’expliquen les diferències entre espècies pel que fa al grau d’expansió del còrtex? Per a respondre això cal tenir en compte que la placa cortical es genera a partir de cèl·lules progenitores localitzades just davall d’aquesta làmina (la zona roja de la figura 3). En les espècies amb un còrtex petit i llis, les cèl·lules progenitores es divideixen inicialment per formar altres progenitores, però de seguida comencen a generar cèl·lules filles que no es tornaran a dividir; aquestes cèl·lules post-proliferatives després migren radialment cap a l’emergent placa cortical i es diferencien en neurones. Per contra, en les espècies amb còrtex gran i amb molts plecs, les cèl·lules progenitores corticals passen per unes quantes sèries de divisions cel·lulars addicionals abans de començar a generar cèl·lules post-proliferatives. A causa d’aquestes divisions cel·lulars addicionals, són moltes més les cèl·lules que acaben migrant a la placa cortical, on formen el neocòrtex. D’altra banda, a mesura que les neurones joves van migrant cap a la capa cortical, van empentant les cèl·lules veïnes a un costat de tal manera que la capa cortical es va estenent tangencialment, és a dir, que la superfície s’expandeix, encara que no guanye en espessor de manera apreciable. A causa d’aquesta «intercalació radial», l’increment evolutiu de neurones neocorticals està associat amb una gran expansió de la superfície del còrtex, que al seu torn augmenta molt menys en espessor. Aquesta expansió de la superfície, unida a una expansió molt menor del teixit subjacent, incrementa les forces deformants que generen els solcs cerebrals.
«Quins canvis evolutius en l’ADN provoquen que les cèl·lules progenitores corticals es dividesquen més en unes espècies que en altres? És difícil trobar una resposta senzilla»
Quins canvis evolutius en l’ADN provoquen que les cèl·lules progenitores corticals es dividesquen més en unes espècies que en altres? És difícil trobar una resposta senzilla, perquè tot de molècules molt diferents estan involucrades en el control del cicle cel·lular, i molt possiblement l’expansió evolutiva de les progenitores es basa en diferents mecanismes moleculars en les diferents espècies. No obstant això, aquest problema s’ha estudiat amb èxit en una espècie molt interessant: la nostra (Florio et al., 2015). Aquest treball ha mostrat que el gen ARHGAP11B va aparèixer en l’espècie humana poc després de la divergència amb el llinatge dels ximpanzés a causa d’una duplicació parcial d’un gen ancestral. Expressant artificialment aquest gen en cèl·lules progenitores del còrtex de ratolins es va forçar les dites progenitores a generar una quantitat inusualment gran de «cèl·lules progenitores basals», el que va incrementar la quantitat total de progenitores del còrtex. Encara més fascinant va ser que la meitat dels ratolins que expressaven ARHGAP11B en les seues progenitores corticals acabaren desenvolupant plecs corticals que s’assemblaven als humans. Així doncs, l’evolució de novo d’ARHGAP11B és probablement una de les causes moleculars principals de l’expansió i plegament del còrtex en el llinatge humà.
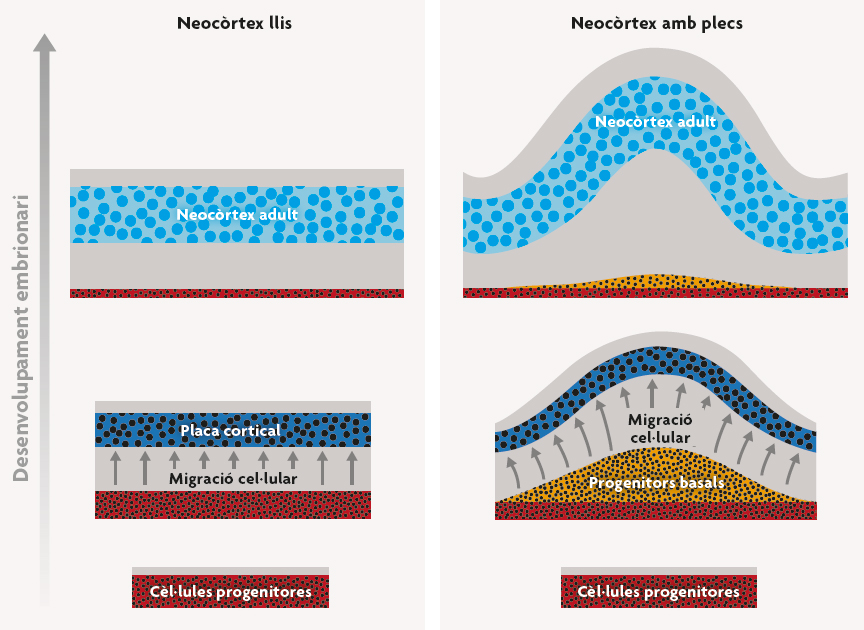
Figura 3. Mecanisme de desenvolupament per a l’evolució dels plecs del neocòrtex. Quan les cèl·lules progenitores del còrtex deixen de dividir-se, migren radialment fora de la zona progenitora (roig) per formar una placa cortical densa en cèl·lules (blau fosc). A mesura que avança el desenvolupament la placa cortical s’expandeix i, finalment, dóna lloc al neocòrtex adult (blau clar). En les espècies amb neocòrtex amb plecs (dreta), les cèl·lules progenitores es divideixen més sovint i formen una capa extra de «progenitores basals». Aquesta expansió del grup de progenitores genera més neurones que migren cap a la placa cortical. Aquestes neurones migrants s’insereixen en la placa cortical de tal manera que aquesta s’expandeix tangencialment molt més que no s’engrosseix. Com que el teixit subjacent no s’expandeix tangencialment tan de pressa, la capa cortical comença a deformar-se i a plegar-se. A mesura que la placa cortical va madurant i es transforma en un neocòrtex adult, els plecs més primerencs es van marcant de manera més prominent (Striedter et al., 2015). / Georg F. Striedter
A mesura que vaja progressant la investigació sobre el plegament cortical i sobre altres sistemes model de la biologia evolutiva del desenvolupament, probablement aniran coneixent-se més mecanismes subjacents de cada fenomen. Alguns d’aquests mecanismes ocuparan diferents nivells d’anàlisi, per això és important esbrinar com es relacionen entre si (Striedter, 1998). Fins i tot dins d’un nivell determinat, probablement es descobreixen múltiples mecanismes. Per exemple, l’evolució d’ARHGAP11B és probablement un dels molts mecanismes moleculars que guien l’expansió i el plegament del còrtex, fins i tot en el llinatge humà. A mesura que aquesta diversitat de mecanismes entra en joc, serà important distingir entre els principals factors causants –el que alguns han anomenat «mediadors»– i els menys importants –els que es podrien denominar «moduladors»–. No sempre serà una distinció fàcil, especialment si en cada llinatge predominen mecanismes diferents però generen morfologies semblants. Fins i tot en el cas que una manipulació experimental ben definida, com l’expressió d’ARHGAP11B en ratolins, genere un fenotip que semble una variant evolutiva, això no provaria que el mecanisme manipulat siga la principal causa del canvi filogenètic natural. No oblidem que en biologia sovint hi ha més d’una via per a resoldre un problema, més d’una via per a construir un determinat fenotip.
«Des de la perspectiva evo-devo, el plec cortical és un fenomen que requereix una explicació basada en el desenvolupament»
Tot i això, l’ús de manipulacions experimentals per a fenocopiar encara que només siguen alguns aspectes del canvi evolutiu pot ser molt útil. Particularment interessant seria explorar com la resta del sistema biològic respon a la manipulació específica. Per exemple, fa temps vaig proposar que l’increment evolutiu de grandària d’una regió cerebral, en comparació amb la resta del cervell, podia fer que l’àrea engrandida projectara cap a una major varietat de dianes i que rebera una major varietat d’aferències o inputs (Striedter, 2005). Abonen aquesta hipòtesi diverses dades basades en correlacions, però encara no s’ha provat experimentalment. Per a efectuar una prova d’aquest tipus es podria, per exemple, expressar ARHGAP11B en les cèl·lules corticals progenitores de ratolins i després examinar si les escorces adultes ampliades i plegades generen més connexions axonals de les naturals en ratolins normals. Provar aquesta hipòtesi seria interessant perquè implicaria l’existència de mecanismes de desenvolupament que ajudarien a integrar els canvis evolutius en una part del sistema nerviós amb la resta del sistema obviant la necessitat de canvis genòmics addicionals per a dur a terme la integració.
De manera més general, seria interessant descobrir el grau en què les manipulacions experimentals dirigides específicament a una regió del cervell o a un mecanisme tenen efectes posteriors en cascada en altres regions i mecanismes cerebrals, i fins a quin punt aquests efectes en cascada són adaptatius. Em fascina, per exemple, el descobriment que cabres que han nascut sense les potes anteriors puguen aprendre a caminar amb les dues posteriors (de forma bípeda) i després desenvolupar canvis adaptatius en altres parts del seu cos per a adequar-se a aquesta nova forma de locomoció (West-Eberhard, 2005). Sospite que el sistema nerviós també està dotat d’aquesta plasticitat tan útil; de fet, aquest tipus de plasticitat en el desenvolupament podria ser adaptativa en el sentit que promou l’evolucionabilitat (capacitat per a evolucionar).
«Seria interessant descobrir el grau en què les manipulacions experimentals dirigides específicament a una zona del cervell tenen efectes posteriors en cascada en altres regions»
Igual d’interessant és la idea que els sistemes nerviosos en desenvolupament podrien ser resistents davant de moltes pertorbacions, com les produïdes per les variacions genètiques o ambientals naturals dins d’una població. La idea d’aquests «mecanismes d’amortiment o tamponament» del desenvolupament es remunta almenys a Conrad Waddington (Striedter, 1998), però el fenomen és difícil d’estudiar perquè, al cap i a la fi, les manipulacions rellevants no produeixen un fenotip adult. Així i tot, els mecanismes que proporcionen aquesta resistència a la pertorbació es poden estudiar experimentalment, i cada vegada són més susceptibles de sotmetre’s a l’anàlisi matemàtica i a la modelització (per exemple, Lander, 2011). En general, crec que els sistemes nerviosos han evolucionat per a equilibrar la necessitat que el desenvolupament siga estable amb la necessitat que puga evolucionar. Entendre com s’aconsegueix i es gestiona aquest equilibri al llarg de l’evolució seria, al meu parer, un objectiu digne de la neurobiologia evolutiva del desenvolupament.
REFERÈNCIES
Abzhanov, A., Protas, M., Grant, B. G., Grant, P. R., & Tabin, C. J. (2004). BMP4 and morphological variation of beaks in Darwin’s finches. Science, 305, 1462–1465. doi: 10.1126/science.1098095
Charvet, C. J., & Striedter, G. F. (2009). Developmental origins of mosaic brain evolution: Morphometric analysis of the developing zebra finch brain. The Journal of Comparative Neurology, 514(2), 203–213. doi: 10.1002/ cne.22005
Denes, A. S., Jékely, G., Steinmetz, P. R. H., Raible, F., Snyman, H., Prud’homme, B., … Arendt, D. (2007). Molecular architecture of annelid nerve cord supports common origin of nervous system centralization in bilateria. Cell, 129(2), 277–288. doi: 10.1016/j.cell.2007.02.040
Florio, M., Albert, M., Taverna, E., Namba, T., Brandl, H., Lewitus, E., … Huttner, W. B. (2015). Human-specific gene ARHGAP11B promotes basal progenitor amplification and neocortex expansion. Science, 347, 1465–1470. doi: 10.1126/science.aaa1975
Gilbert, S. F., Opitz, J. M., & Raff, R. A. (1996). Resynthesizing evolutionary and developmental biology. Developmental Biology, 173(2), 357–372. doi: 10.1006/dbio.1996.0032
Gould, S. J. (1977). Ontogeny and phylogeny. Cambridge, MA: Harvard University Press.
Holland, P. W. H., Holland, L. Z., Williams, N. A., & Holland, N. D. (1992). An amphioxus homeobox gene: Sequence conservation, spatial expression during development and insights into vertebrate evolution. Development, 116, 653–661.
Kollar, E. J., & Fisher, C. (1980). Tooth induction in chick epithelium: Expression of quiescent genes for enamel synthesis. Science, 207, 993– 995. doi: 10.1126/science.7352302
Lander, A. D. (2011). Pattern, growth, and control. Cell, 144, 955–969. doi: 10.1016/j. cell.2011.03.009
McGowan, L., Kuo, E., Martin, A., Monuki, E. S., & Striedter, G. (2011). Species differences in early patterning of the avian brain. Evolution, 65, 907–911. doi: 10.1111/j.1558- 5646.2010.01126x
McGowan, L. D., Alaama, R. A., Freise, A. C., Huang, J. C., Charvet, C. J., & Striedter, G. F. (2012). Expansion, folding, and abnormal lamination of the chick optic tectum after intraventricular injections of FGF2. PNAS, 109(S1), 10640–10646. doi: 10.1073/pnas.1201875109
Medawar, P. B. (1967). The art of the soluble. Londres: Methuen.
Medina, L., Abellán, A., & Desfilis, E. (2013). A never-ending search for the evolutionary origin of the neocortex: Rethinking the homology concept. Brain, Behavior and Evolution, 81(3), 150–153. doi: 10.1159/000348282
Puelles, L., Kuwana, E., Puelles, E., Bulfone, A., Shimamura, K., Keleher, J., … Rubenstein, J. L. R. (2000). Pallial and subpallial derivatives in the embryonic chick and mouse telencephalon, traced by the expression of the genes Dlx- 2, Emx-1, Nkx-2.1, Pax-6, and Tbr-1. The Journal of Comparative Neurology, 424, 409–438. doi: 10.1002/1096-9861(20000828)424:3<409::AID-CNE3>3.0.CO;2-7
Striedter, G. F. (1998). Stepping into the same river twice: Homologues as recurring attractors in epigenetic landscapes. Brain, Behavior and Evolution, 52, 218–231. doi: 10.1159/000006565
Striedter, G. F. (2005). Principles of brain evolution. Sunderland, MA: Sinauer Associates.
Striedter, G. F., Srinivasan, S., & Monuki, E. S. (2015). Cortical folding: When, where, how, and why? Annuals Reviews of Neuroscience, 38, 291–307. doi: 10.1146/annurev-neuro-071714-034128
Sylvester, J. B., Rich, C. A., Loh, Y.-H. E., von Staaden, M. J., Fraser, G. J., & Streelman, J. T. (2010). Brain diversity evolves via differences in patterning. PNAS, 107, 9718–9723. doi: 10.1073/pnas.1000395107
West-Eberhard M. J. (2005). Phenotypic accommodation: Adaptive innovation due to developmental plasticity. Journal of Experimental Zoology Part B: Molecular and Developmental Evolution, 304, 610–618. doi: 10.1002/ jez.b.21071





