Vacunes i evolució
Per què és important entendre la diversitat genètica dels patògens?
Des del punt de vista de les intervencions en salut pública no hi ha millor arma que aquella que permet prevenir la transmissió o aparició de la malaltia. Dins del camp de les malalties infeccioses les vacunes s’han convertit en aquesta arma i han permès controlar-ne moltes. Avui dia hi ha un gran nombre de malalties infeccioses emergents per a les quals no hi ha vacunes o malalties oblidades que estan reemergint. Noves vacunes s’estan desenvolupant per atacar els patògens que s’hi relacionen. No obstant això, i a pesar de la importància del disseny d’una bona vacuna, la diversitat genètica dels patògens no s’ha tingut sempre en compte. L’estudi d’aquesta diversitat pot indicar-nos com el patogen s’adapta a la pressió del sistema immune i quina part de la resposta immune és beneficiosa per a l’hoste i quina part per al patogen. Entendre aquesta relació permetrà predir fins quin punt serà eficaç i universal una vacuna i ajudarà a dissenyar-les millor.
Paraules clau: variació antigènica, tuberculosi, grip, sistema immune, malalties infeccioses.
Una breu història de les vacunes
Les malalties infeccioses han estat una de les principals xacres de la humanitat. Vivint en el segle XXI és difícil adonar-se de l’impacte econòmic, polític i militar que han tingut en la història. Als casos coneguts de les epidèmies de verola al Nou Món que van portar a la mort un 25% de la població asteca en un sol any o la mort de vint-i-quatre milions d’europeus durant els anys de la pesta negra, cal afegir molts episodis més. El projecte per al canal de Panamà va ser inicialment escomès per França, que el va haver d’abandonar en part a causa de l’alta incidència de febre groga i malària. De fet, mentre els Estats Units d’Amèrica el construïen, el 85% dels treballadors del canal de Panamà van haver de ser hospitalitzats en algun moment a causa d’aquestes malalties. I la construcció del canal només va ser possible gràcies a les mesures de prevenció contra els respectius vectors que acabaven de ser identificats a Cuba en els anys posteriors a la guerra amb Espanya. La mal anomenada grip espanyola va matar el 3% de la població mundial entre 1918 i 1920, cinc vegades més morts que les causades per la Gran Guerra que tot just havia acabat. Molts historiadors culpen diferents plagues del deteriorament de moltes urbs de l’Imperi Romà i afirmen que això va contribuir a la caiguda d’aquest. De fet, l’anomenada plaga antonina (165-185 dC), l’agent causant de la qual es desconeix (s’especula que era la verola), es creu que va matar cinc milions d’habitants de l’imperi, mentre que l’anomenada plaga justiniana va assotar l’Imperi Bizantí (541-542 dC). El mateix Napoleó va fer vacunar tot el seu exèrcit contra la pigota i va lloar públicament Edward Jenner pel desenvolupament de la vacuna a pesar de ser ciutadà d’un país enemic.
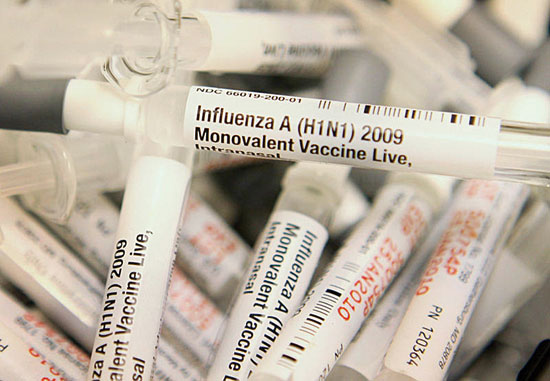
El virus de la grip estacional és del tipus H3N2. Això és així, però, només des de 1968, quan H3N2 va desplaçar el subtipus anterior (H2N2). A més, molts altres tipus en menor freqüència continuen circulant avui dia (H1N1, H1N2). / Agència SINC
Les causes de moltes malalties infeccioses només es van començar a aclarir quan el 1680 la Royal Society de Londres va reconèixer públicament les observacions d’un científic holandès, Antonie van Leeuwenhoek, sobre l’existència d’organismes microscòpics unicel·lulars. Que pogueren existir «entitats» que causaren les grans epidèmies ja havia estat proposat abans fins i tot que les observacions de Leeuwenhoek per personatges com Girolamo Fracastoro. Però va ser el treball de l’holandès i més tard de científics com Semmelweis (en el camp de la higiene) i de John Snow (en el camp de l’epidemiologia) els que van servir de suport a la formulació de l’anomenada teoria del germen. Aquesta teoria postulava que moltes de les malalties més comunes eren realment degudes a infeccions per microorganismes, teoria que va rebre un suport definitiu amb els treballs de Louis Pasteur i Robert Koch. Molts dels agents causants de les majors epidèmies van ser descrits en el segle XIX o començament del XX i identificar-los va portar a una època d’innovació en la prevenció, diagnòstic i tractament de les malalties infeccioses (De Kruif, 1926). Com a conseqüència de tot això, la segona meitat del segle XX es va caracteritzar si no per l’eradicació, sí pel desplaçament de les malalties infeccioses com la principal causa de morbidesa almenys als països desenvolupats. En aquest sentit hi ha un consens general: el desenvolupament de vacunes i les campanyes de vacunació massiva, moltes de les quals promogudes a escala mundial, han salvat milions de vides i virtualment eradicat moltes malalties (Nabel, 2013). Un paper central en la història de la investigació en vacunes l’ocupa una malaltia a la qual se li imputa la mort de centenars de milions de persones al llarg de la història, la verola.
Al contrari del que es pensa, el procés d’inocular patògens en les persones per generar una resposta immune protectora a futures exposicions no va començar amb Edward Jenner, el metge britànic al qual s’atribueix correctament el desenvolupament de la primera vacuna. Els primers casos d’inoculació antivariòlica són atribuïts a una monja budista al voltant de l’any 1020 dC. Segons ha quedat recollit, la monja mostrejava restes de les ferides de pacients de verola i les introduïa en les fosses nasals de persones no malaltes, procediment que proporcionava un cert grau de protecció contra noves infeccions. En l’Anglaterra del segle XVIII la versió bovina de la malaltia era tan important econòmicament com mortal ho era la versió humana. El treball amb totes dues malalties va portar Edward Jenner a desenvolupar i provar amb èxit la primera vacuna contra la verola –de fet, la primera vacuna de la història–, a partir de la versió bovina de la malaltia. La vacuna no sols representà una fita científica que va obrir el camí cap a moltes més sinó que a més va representar l’inici d’actuacions de salut pública a gran escala, la qual cosa converteix la verola en el major exemple d’eradicació d’una malaltia a partir de plans coordinats de vacunació massiva. Ali Maow Maalin, el 1977, a l’edat de 23 anys, resident a Merca (Somàlia), es va convertir en el darrer cas oficial de verola al món i el primer gran èxit de l’Organització Mundial de la Salut (OMS) en l’erradicació de les malalties infeccioses. L’èxit amb la vacunació de la verola i en major o menor mesura de malalties com la poliomielitis, rubèola, parotiditis o la diftèria no ha impedit, però, que encara avui moltes malalties infeccioses continuen essent comunes o hagen ressorgit i noves aproximacions al desenvolupament de vacunes es facen necessàries.
«La descipció d’agents va obrir una època d’innovació en la prevenció, diagnòstic i tractament de les malalties infeccioses»
El punt de vista del patogen
Una possible causa del fracàs en el disseny de vacunes és que en molts casos no s’ha tingut en compte la diversitat genètica del patogen i la seua capacitat d’adaptar-se a noves pressions de selecció com són les vacunacions o l’ús d’antibiòtics. Des del punt de vista genètic, els patògens, igual com les poblacions humanes, no són homogenis, han acumulat canvis al llarg de la seua història evolutiva. Hi ha patògens amb una alta diversitat genètica, que fins i tot presenten tipus patògens i no-patògens, com és el cas d’Escherichia coli, i patògens molt especialitzats amb molt baixa diversitat, com és el cas dels bacils de la lepra i la tuberculosi o el bacteri de la pesta. Alguns presenten un alt nivell de recombinació, per exemple Neisseria meningitidis i alguns virus, mentre que altres són genèticament monomòrfics. En el context de les vacunes aquesta variació preexistent ha de ser tinguda en compte, així com la capacitat del patogen de mutar i trobar variacions de fuga a l’acció del sistema immune o de la protecció conferida per les vacunes. Tots aquests aspectes relacionats amb l’evolució del patogen poden afectar el desenvolupament i la universalitat de noves vacunes. Per a il·lustrar l’impacte de l’evolució en el disseny de vacunes, veurem dos exemples molt diferents: el cas de la vacuna de la grip i el de la vacuna de la tuberculosi.
L’èxit amb la vacunació de la verola i altres malalties no ha impedit que encara avui moltes malalties infeccioses continuen sent immunes o hagen ressorgit i noves aproximacions al desenvolupament de vacunes es facen necessàries. / Aki Hänninen
La grip: evadint la resposta immune
Els virus en general i els basats en ARN en particular són els típics exemples d’organismes que evolucionen a tal velocitat que són capaços de trobar solucions a molts dels reptes que els posem per a prevenir-los i tractar-los. No obstant això no són només les altes taxes de mutació o de recombinació el secret del seu èxit, sinó també les grans dimensions poblacionals, que els permeten trobar les solucions evolutives més òptimes amb major rapidesa. Aquesta alta variabilitat té conseqüències directes en el disseny de fàrmacs i vacunes per a tractar o prevenir la infecció. Un cas paradigmàtic, potser el més estudiat, és el de la vacuna usada cada any per a la grip estacional.
El reservori natural per a tots els virus de la grip, ja siga aquesta estacional o epidèmica, són les aus. Els virus de la grip que afecten humans són coneguts com a tipus A i generalment són diferenciats basant-se en la combinació de dues de les seues proteïnes, HA (hemaglutinina) i NA (neuramidasa). Aquestes proteïnes són reconegudes pel sistema immune, en altres paraules, són antigens. Cada esdeveniment important de recombinació que ha generat noves combinacions d’aquestes dues proteïnes ha comportat un canvi radical en la seua antigenicitat, cosa que ha donat lloc a episodis pandèmics més o menys rellevants. Això és el que va ocórrer amb el virus de 1918, que s’estima que va matar 50 milions de persones globalment i que comunament és conegut com el virus de la grip espanyola. Així, per exemple, el virus de la grip que ens afecta tots els anys (també coneguda com a grip estacional) és del tipus H3N2. Això, però, és així només des de 1968, quan H3N2 va desplaçar el subtipus anterior (H2N2). A més molts altres tipus amb menor freqüència continuen circulant avui dia (H1N1, H1N2).
«La vacuna contra la verola va significar l’inici d’actuacions de salut pública a gran escala»
De tot el que s’ha exposat anteriorment queda clara la gran capacitat del virus de la grip per a generar diversitat antigènica. De fet, atenent al mecanisme involucrat i sobretot a les conseqüències de l’acumulació d’aquesta variació, se sol diferenciar entre episodis de «deriva antigènica» i episodis de «desplaçament antigènic» (Rambaut et al., 2008). Als últims m’he referit ja i són els que generalment comporten un canvi radical en la composició antigènica del virus. Com que la població general no ha estat exposada anteriorment a aquesta nova combinació, el resultat són pandèmies de major o menor gravetat. Històricament se’n distingeixen cinc, de grans pandèmies, incloent-hi la més recent, coneguda com a grip A, produïda per un virus tipus H1N1.
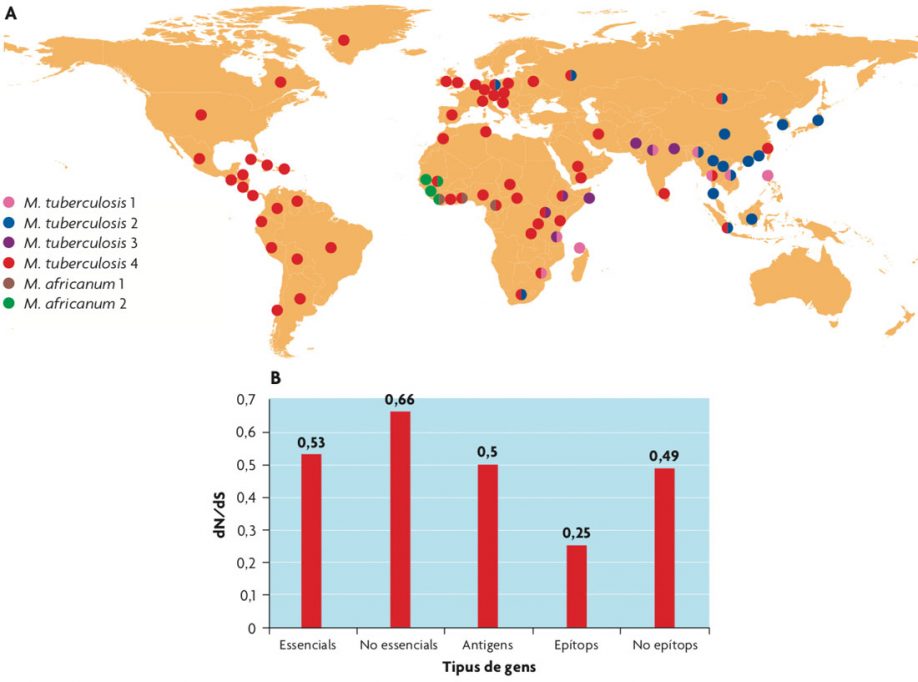
A) Distribució global dels principals llinatges dins del complex de la tuberculosi. Els colors indiquen el llinatge dominant en les diferents zones geogràfiques. / Extreta de Comas i Gagneux, 2009. B) Els epítops coneguts de M. tuberculosis són la part més conservada del genoma del patogen i suggereixen que la tuberculosi no segueix una estratègia d’evasió del sistema immune sinó que s’aprofita d’aquest per a transmetre’s. / Adaptat de Comas et al., 2010.
Al contrari del que ocorre quan el virus canvia totalment de composició antigènica, la grip estacional ha d’enfrontar-se al fet que la infecció a una persona genera un cert grau d’immunitat protectora que limita el nombre de persones susceptibles al mateix tipus de virus cada any. La manera en què el virus evadeix poblacions amb una alta immunitat adquirida és fent valdre l’alta taxa de mutació i les grandàries poblacionals que presenta, i que li permeten trobar variacions aminoacídiques que evadesquen la immunitat adquirida per infeccions prèvies. El resultat d’això és que el virus de la grip estacional és lleugerament diferent cada any com a resultat d’acumular variacions de fuga al sistema immune (figura 1). És aquest canvi continu el que fa que la vacuna recomanada contra la grip no puga ser la mateixa cada any. Un comitè d’experts decideix anualment quina és la millor combinació d’antigens per a generar immunitat general, basada en les dades dels tipus de grip circulant en els anys anteriors. Per posar un exemple, per a l’any 2013 l’OMS va recomanar que la vacuna estiguera composta per una mescla d’antigens d’una soca detectada el 2009 de H1N1, una altra del 2011 de H3N2 i una altra per a la menys comuna però present en molts països de grip tipus B, del 2010.
«El virus de la grip estacional és lleugerament diferent cada any com a resultat d’acumular variacions de fuga al sistema immune»
La tuberculosi: manipulant la resposta immune
Un cas especial quant a l’impacte de la diversitat del patogen en la resposta immune el constitueix el bacil de la tuberculosi. Entre 1908 i 1921 dos microbiòlegs de l’Institut Pasteur, Calmette i Guérin, van aïllar i van cultivar mitjançant passes seriats el bacil de la tuberculosi bovina per crear una soca atenuada que es poguera usar per a immunitzar contra la infecció tuberculosa en humans. Aquesta soca atenuada és coneguda com el bacil de Calmette i Guérin (BCG) i és la vacuna més usada en la història. La versió bovina de la tuberculosi és causada per Mycobacterium bovis, que forma part del conegut com a complex de la tuberculosi junt amb altres bacils que provoquen tuberculosi en animals però rarament en humans i els bacils que pràcticament només provoquen tuberculosi en humans (Mycobacterium tuberculosis i Mycobacterium africanum). Per bé que tots ells posseeixen diferents noms específics, les diferències a escala genòmica són tan petites (al voltant de 2.000 canvis nucleotídics com a màxim) que avui dia serien considerats una sola espècie. Quan Calmette i Guérin van desenvolupar la vacuna a partir d’una soca virulenta de la tuberculosi bovina no sabien que durant el procés de passes al laboratori (a rodanxes de creïlla suplementades amb glicerol) es van produir una sèrie de canvis a escala genòmica que es van incrementar quan la soca de la vacuna es va distribuir per laboratoris d’arreu el món. Com que en aquella època no existien mètodes per a mantenir les mostres congelades, els laboratoris van realitzar passes seriades per mantenir-les. El resultat és que diferents soques de la vacuna van acumular diferents mutacions en el seu genoma, el que va donar lloc a una genealogia que permet seguir l’evolució de la vacuna durant els darrers noranta anys. D’aquesta manera la vacuna contra la tuberculosi es va convertir involuntàriament en un experiment d’evolució que va durar dècades. No obstant això la vacuna de la tuberculosi no és efectiva contra la forma més contagiosa i comuna de la malaltia, la tuberculosi pulmonar en adults. Sí que ho és, i d’ací que es facen campanyes de vacunació massiva amb BCG als països amb alta incidència de tuberculosi, contra les formes extrapulmonars de la malaltia en nens.
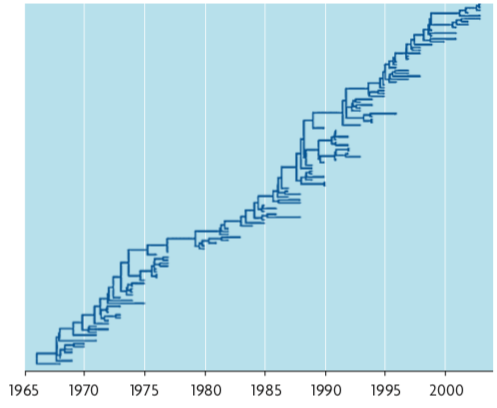
Figura 1. Arbre filogenètic d’una regió del gen HA de la grip A (H3N2) a partir de mostres de virus obtingudes entre 1968 i 2002. L’arbre reflecteix un llinatge predominant del qual es deriven branques secundàries que duren uns pocs anys. El llinatge central reflecteix l’adaptació de l’antigen del virus al llarg del temps com a resposta a l’acció del sistema immune. / Font: PLoS Comput Biol
Com hem vist en el cas de la grip, la majoria de patògens d’una manera o una altra acumula canvis en aquelles zones o proteïnes del genoma que són reconegudes pel sistema immune durant la infecció. Aquestes proteïnes són conegudes com a antigens i els canvis que s’hi acumulen s’associen a la variació antigènica, que permet al patogen evadir les defenses humanes. No obstant això, el cas de la tuberculosi és especial. Un estudi que aplicava tecnologies de seqüenciació massiva sobre un conjunt de soques representatives de la diversitat coneguda del bacil ha revelat que els antigens, i concretament els fragments peptídics reconeguts pel sistema immune coneguts com epítops, estan hiperconservats en Mycobacterium tuberculosis (Comas et al., 2010). De fet si es compara amb els gens essencials, gens que no es poden eliminar en el patogen perquè són necessaris per a sobreviure, els epítops estan igual o millor conservats i acumulen menys canvis aminoacídics que els gens no-essencials o altres zones no reconegudes pel sistema immune. No obstant això, per experiments amb ratolins sabem que la resposta immune adaptativa i sobretot la referida a cèl·lules T CD4+ és essencial per a contenir la infecció. Per què el bacil de la tuberculosi no tracta d’evadir aquesta resposta aprofitant canvis en la seqüència dels seus epítops? La resposta més senzilla és perquè en el cas de la tuberculosi el patogen necessita de la resposta immune per a transmetre’s. La resposta immune permet al bacil completar el seu cicle d’infecció, primer induint un estat de latència i més tard sobrereaccionant en el 5-10% dels casos en què el bacteri es reactiva. És, de fet, la reacció inflamatòria part de la causa del dany en els teixits del pulmó que són expulsats, junt amb el patogen, en esternudar, la qual cosa els permet transmetre’s. Aquest cicle vital indica que, si bé la resposta immune en part beneficia l’hoste, també sembla que part d’aquesta reacció beneficia el patogen. De fet els pacients VIH positius amb baixos nivells de CD4+ presenten amb més freqüència formes extrapulmonars, no transmissibles de la malaltia, com també una menor càrrega bacil·lar en l’esput. Açò indica que una correcta resposta immune és necessària per a contenir la infecció en el pulmó en primer lloc i per a la posterior transmissió en els casos en què el bacteri es reactiva de la infecció latent.
«La vacuna contra la tuberculosi es va convertir involuntàriament en un experiment d’evolució que va durar dècades»
Aconseguir una vacuna eficaç contra la tuberculosi pulmonar s’ha convertit en un dels principals objectius de l’OMS en els darrers trenta anys. Encara que la tuberculosi es pot curar si se segueix el tractament, s’estima que un terç de la població mundial està infectada de manera latent i que al voltant d’un 10% presentarà símptomes de tuberculosi activa en algun moment de la seua vida. Això indica que, si bé els casos actius poden ser tractats amb antibiòtics, en termes de cost-benefici seria molt més efectiva una vacuna que en primer lloc evitara la infecció o que almenys impedira la reactivació de la infecció latent. Més de deu candidats són actualment en diferents fases de desenvolupament, alguns dels quals ja s’estan provant en assajos clínics amb humans. No obstant això, la tuberculosi és una malaltia complexa. Del seu agent causant, a pesar d’haver estat descobert fa més de cent anys, sabem encara poc, així com de la interacció entre el bacteri i el sistema immune durant la infecció. L’arribada de la seqüenciació genòmica, i més recentment de les tecnologies de seqüenciació massiva, està permetent entendre en tota la seua extensió la diversitat d’aquest patogen, la qual cosa ha portat a nous coneixements sobre la manera com es transmet, evoluciona i, per al tema que ens ocupa, com respon al sistema immune.
La vacuna de la tuberculosi no és efectiva contra la forma més contagiosa i comuna de la malaltia, la tuberculosi pulmonar en adults. Sí que ho és, i d’ací que es facen campanyes de vacunació massiva amb BCG als països amb alta incidència de tuberculosi, contra les formes extrapulmonars de la malaltia en nens. En la imatge, una campanya d’immunització a Delhi (l’Índia). / OMS/P. Virot
Aquests resultats permeten també entendre per què l’eficàcia de la vacuna BCG és tan desigual, ja que la forma bovina del bacil a nivell genòmic no és essencialment molt diferent del bacil de la tuberculosi humana. De fet és una bandera roja en el disseny de vacunes que intenten usar alguns d’aquests epítops hiperconservats, perquè en part poden afavorir el patogen, no l’hoste. Per tant, al contrari que altres aproximacions per al disseny de vacunes que busquen identificar les regions més conservades del genoma (coneguda com vacunologia reversa), potser, en el cas de la tuberculosi i d’altres infeccions semblants, s’hagen de cercar nous antigens, basats en regions hipervariables del genoma, que reflectesquen una vertadera acumulació de variació de fuga en resposta al sistema immune. Estratègies semblants a les usades per Mycobacterium tuberculosis per aprofitar part de la resposta immune per completar el seu cicle vital han estat recentment descrites per a altres patògens com el VIH o Streptococcus pneumoniae.
Els dos casos analitzats, així com molts més, porten a una consideració essencial. En un patogen la variació existeix i quan es dissenyen noves vacunes cal preguntar-se diverses coses: Quina és la naturalesa de la variació preexistent? Està aquesta variació unida a pressions selectives immunes o de vacunacions? Quina és la capacitat del patogen d’adaptar-se davant de noves pressions de selecció? Responent aquestes preguntes es podran dissenyar millors vacunes mercès a un millor coneixement de la interacció del sistema immune i el patogen, la qual cosa ens permetrà distingir entre aquells elements que formen part de la resposta immune protectora enfront d’aquelles interaccions que poden beneficiar el patogen.
REFERÈNCIES
Comas, I. i S. Gagneux, 2009. «The Past and Future of Tuberculosis Research». PLoS Pathogens, 5(10): e1000600. doi: 10.1371/journal.ppat.1000600.
Comas, I. et al., 2010. «Human T Cell Epitopes of Mycobacterium tuberculosis Are Evolutionarily Hyperconserved». Nature Genetics, 42(6): 498-503. doi: 10.1038/ng.590.
De Kruif, P., 1926. Microbe Hunters. Harcourt, Brace and Co. Nova York.
Nabel, G. J., 2013. «Designing Tomorrow’s Vaccines». The New England Journal of Medicine, 368(6): 551-560. doi: 10.1056/NEJMra1204186.
Rambaut, A. et al., 2008. «The Genomic and Epidemiological Dynamics of Human Influenza A Virus». Nature, 453(7195): 615-619. doi: 10.1038/nature06945.