Els virus dels bacteris
L'ús de fags contra la resistència bacteriana a antibiòtics
Introducció als fags
Els microorganismes i la humanitat han conviscut des que es va originar la nostra espècie, fet que ha donat lloc a tot d’interaccions, tant de bones com de dolentes. Molts microorganismes són beneficiosos per a l’ésser humà, mentre que d’altres poden generar malalties. Entre els microorganismes més coneguts, trobem els bacteris i els virus. A diferència dels bacteris, organismes unicel·lulars procariotes, els virus són paràsits intracel·lulars obligats, cosa que significa que necessiten un hoste per a completar el seu cicle vital. Estan constituïts per àcids nucleics que formen el seu genoma i proteïnes que el recobreixen. Inerts en el medi extracelul·lar, són capaços de reconèixer de manera molt específica els seus hostes. Una vegada es produeix el reconeixement, injecten el seu material genètic (és a dir, el seu genoma) en l’hoste, i segresten la seua maquinària cel·lular per a poder replicar-se i produir progènie viral. En general, hi ha virus capaços d’infectar organismes dels tres dominis de la vida –bacteris, arqueobacteris i eucariotes– i, de fet, són altament específics: cada virus està especialitzat a reconèixer un petit rang d’hostes. Per exemple, els virus que infecten bacteris, denominats bacteriòfags, solament reconeixen alguns bacteris, i no podran reconèixer ni infectar mai cèl·lules eucariotes. Dins dels virus d’eucariotes, els virus de plantes són molt diferents dels virus d’animals, i dins dels animals, hi ha virus que infecten un tipus cel·lular o un altre.
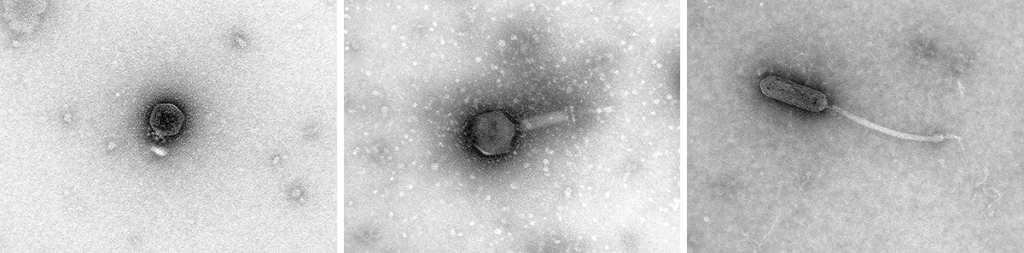
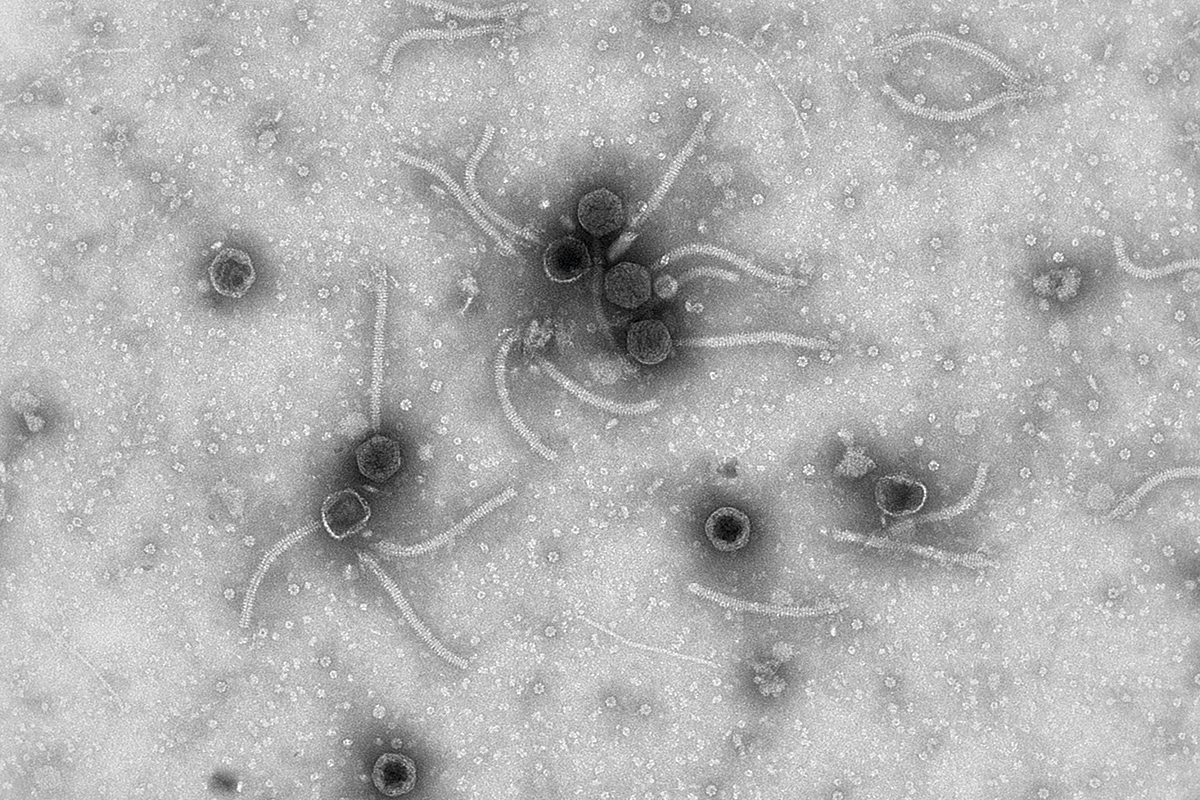
Figura 1. Exemples de micrografies de fags, virus de bacteris, en què podem observar la seua diversitat morfològica. Aquestes micrografies s’han obtingut en el Laboratori de Virologia Ambiental i Biomèdica de l’Institut de Biologia Integrativa de Sistemes (UV-CSIC)./ Pilar Domingo-Calap
Els bacteriòfags, comunament anomenats fags, són els virus més abundants de la biosfera. S’estima que hi ha 1031 partícules virals, és a dir, deu vegades més de virus que de bacteris, i que, per a cada bacteri, hi ha almenys un fag capaç d’infectar-lo. Aquests nombres reflecteixen la importància dels fags en els ecosistemes, així com l’enorme diversitat que presenten, encara desconeguda. Els fags contenen genomes que poden ser d’ARN o ADN, de cadena senzilla o doble, circulars o lineals, segmentades o no segmentades. A més, s’ha observat un gran nombre de morfologies, que va creixent a mesura que es van descobrint nous fags (Figura 1).
Segons el seu cicle biològic, els fags poden dividir-se en fags lítics i temperats, encara que s’han descrit cicles alternatius. Els primers destrueixen el bacteri hoste en un procés conegut com lisi, que representa la ruptura de la membrana cel·lular i l’alliberament del virus al medi extracelul·lar. Els fags temperats incorporen el seu genoma en el de l’hoste, es mantenen latents en forma de profags i representen un paper fonamental en la transferència horitzontal de gens, és a dir, la transmissió d’informació genètica entre organismes que no es produeix a través de la transmissió vertical.
El descobriment dels fags i les seues primeres aplicacions
Els fags van ser descoberts fa ja més d’un segle de manera independent pel bacteriòleg Frederick Twort (1915) i el microbiòleg Félix d’Hérelle (1917). Tots dos buscaven una explicació de l’halo que a vegades observaven quan feien cultius bacterians en plaques d’agar (Figura 2). No obstant això, va ser D’Hérelle qui va proposar que l’halo observat era el resultat de la lisi bacteriana deguda a un altre microorganisme, que va denominar bacteriòfag. D’Hérelle va ser també pioner a aplicar els fags com a tractament en xiquets amb disenteria a França i còlera a l’Índia, fet que marca l’inici, per tant, de la teràpia de fags. Poc després, a causa del descobriment de la penicil·lina en 1928 per Alexander Fleming i després de la II Guerra Mundial, l’ús d’antibiòtics d’ampli espectre es va estendre als països d’Occident i la teràpia de fags va quedar oblidada. Mentrestant, als països de l’Est, on l’accés als antibiòtics era pràcticament nul, els fags van continuar usant-se com a tractament contra infeccions bacterianes, la qual cosa ha afavorit que avui dia s’hi troben centres de referència mundial que continuen utilitzant aquestes teràpies de manera rutinària.
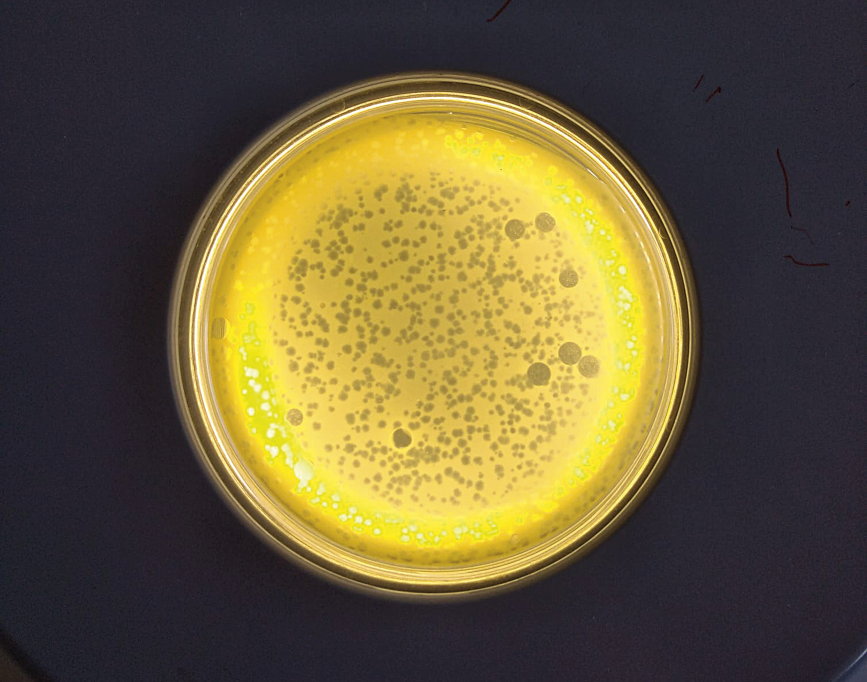
Figura 2. Exemple de placade Petri amb cultius bacterians en agar semisòlid, on s’observa la presència d’halos o plaques de lisi transparents, que reflecteixen l’acció dels fags lisant els bacteris que hi creixen. Hi ha dos fags distints, un que produeix plaques de lisi grans i un altre que en fa de menudes. La lisi suposa la ruptura de la membrana cel·lular del bacteri i l’alliberament del virus al medi extracelul·lar. Imatges preses al Laboratori de Virologia Ambiental i Biomèdica de l’Institut de Biologia Integrativa de Sistemes (UV-CSIC)./ Amanda Martínez
Avui dia, els països occidentals manquen de legislació específica i d’assajos clínics reconeguts i validats per les agències reguladores per a l’ús de fags en pacients. Aquest tan sols està permès en casos excepcionals com a tractament compassiu. No obstant això, científics i metges de tot el món estem sol·licitant a les agències reguladores la necessitat d’incloure la teràpia de fags com a tractament reconegut. Al nostre país, des de la Xarxa Espanyola de Bacteriòfags i Elements Transductors (FAGOMA), estem iniciant la tramitació a través de l’Agència Espanyola de Medicaments i Productes Sanitaris (AEMPS) per a facilitar-ne el reconeixement com a tractament efectiu contra bacteris multiresistents.
Els fags en investigació bàsica
Els fags han sigut àmpliament utilitzats per a comprendre processos biològics fonamentals com la replicació, la transcripció i la traducció dels àcids nucleics. Cal destacar que una gran quantitat de productes derivats de fags s’utilitzen habitualment com a reactius en la investigació, com és el cas de les ligases i les polimerases. A Espanya, la patent del mètode d’amplificació d’àcids nucleics basat en l’ADN polimerasa obtinguda a partir del fag phi29 –descoberta per Margarita Salas– continua sent la més rendible que ha presentat el CSIC. De fet, aquesta tecnologia es considera una de les grans fites de la història de la ciència al nostre país. Així mateix, premis Nobel de Química recents han sigut atribuïts a investigacions basades en fags. En 2018, Frances Arnold, George P. Smith i Gregory Winter van ser guardonats per desenvolupar un mètode basat en fags com a vectors per a la clonació o expressió de gens, conegut com phage display, que permet l’evolució dirigida d’enzims i anticossos. Mitjançant aquesta tècnica poden combinar-se proteïnes d’interès en la part externa d’un fag per crear biblioteques de proteïnes que podran ser útils en diversos camps com el desenvolupament d’anticossos, l’estudi d’interaccions proteïna-proteïna, o la producció d’antivirals o antitumorals, entre moltes aplicacions més. Recentment, en 2020, Emmanuelle Charpentier i Jennifer Doudna van ser premiades per la translació del sistema immunitari dels bacteris davant dels fags al seu ús com a «tisores genètiques», conegut com CRISPR-Cas9. Aquesta eina permet fer canvis en l’ADN de qualsevol organisme amb una elevada precisió. Aquests són només alguns exemples de l’ús de fags com a model experimental en ciència bàsica i les aplicacions potencials que tenen en l’actualitat.
Els fags en biomedicina
Els fags es consideren eines molt prometedores en el camp de la biomedicina per la seua utilitat en la prevenció, diagnòstic i tractament de malalties bacterianes. Encara que el seu ús més conegut és la teràpia de fags, hi ha altres aplicacions que susciten gran interès com ara els biosensors, les teràpies antitumorals, les vacunes basades en fags o els vehicles dirigits contra dianes específiques en el camp de la nanomedicina. Així, el potencial dels fags com a eines biomèdiques és cada vegada major, gràcies a la fàcil manipulació, alta especificitat i baix cost de producció. No obstant això, encara hi ha punts febles, com la necessitat de revisar els aspectes ètics i els protocols de regulació del seu ús en biomedicina. Ací detallarem algunes de les aplicacions dels fags en biomedicina, amb l’objectiu de donar a conèixer el seu potencial des de diferents aproximacions.
Els fags en prevenció
La pell, les superfícies mucoses o el tracte digestiu són exemples de compartiments en què viuen bacteris, virus i altres microorganismes que formen el microbioma. Fags i bacteris coevolucionen constantment i el mantenen en equilibri. En aquest sentit, els fags poden utilitzar-se com a «probiòtics» per controlar les comunitats bacterianes i prevenir malalties associades a un creixement bacterià inadequat. De nou, cal destacar que els fags són altament específics dels bacteris que són capaços de reconèixer –gràcies a receptors concrets que posseeixen–, i aquesta característica és clau per a controlar soques bacterianes d’interès, ja que els bacteris no diana romanen inalterats i mantenen l’homeòstasi (Figura 3). Els fags, per tant, poden ser considerats moduladors de la microbiota i eines segures, ja que formen part de l’entorn natural del microbioma.
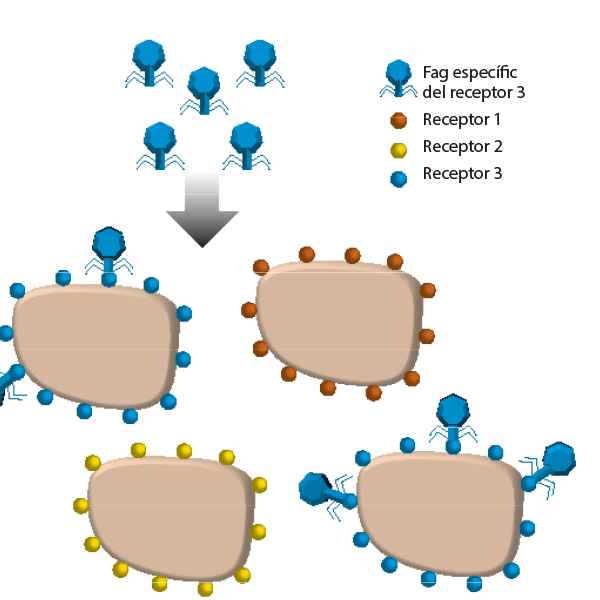
Figura 3. A causa de la seua alta especificitat, els fags només poden reconèixer les cèl·lules que expressen receptors específics. En la figura, podem observar aquest procés de reconeixement i unió d’un determinat fag a un bacteri diana. D’aquesta manera, es prevé la infecció de la resta de bacteris i possibles efectes secundaris en la microbiota./ Redibuixat a partir de Pilar Domingo-Calap
Un altre ús dels fags en la prevenció de malalties són les vacunes derivades de fags. L’enginyeria de fags basada en el phage display pot utilitzar-se per a produir vacunes específiques contra altres patògens com els fongs o fins i tot altres virus (Smith, 2019). Una altra aplicació és generar biblioteques de fags per a la producció d’anticossos recombinants. En aquest cas, els anticossos obtinguts poden utilitzar-se com a agents profilàctics, però també com a eines de diagnòstic, de tipificació bacteriana o terapèutiques.
Els fags també poden combatre biopel·lícules bacterianes. En entorns hospitalaris, aquestes biopel·lícules es formen en dispositius mèdics, catèters, pròtesis, o fins i tot en superfícies, i solen estar compostes per bacteris nosocomials resistents a antibiòtics. Els fags, gràcies a la seua capacitat de replicació in situ i a enzims codificats en els seus genomes, poden destruir activament aquestes biopel·lícules, ja que poden penetrar-les i eliminar-les de manera molt eficient. Per aquesta raó, els fags podrien utilitzar-se per a tractar dispositius mèdics o les superfícies abans d’usar-les. Cal destacar que alguns enzims derivats de fags, com és el cas de les lisines o les holines, també tenen un gran potencial per a combatre bacteris (Ferriol-González i Domingo-Calap, 2020).
Els fags en diagnòstic
Com hem esmentat, els fags també poden ser utilitzats per a la detecció i tipificació de bacteris, una solució ràpida i econòmica per a una tasca que a vegades resulta laboriosa i difícil. Si disposem d’una llibreria de fags capaços de reconèixer una bateria de bacteris d’interès, podem determinar de manera senzilla quin bacteri està causant una infecció. En aquest sentit, la bioimatge i la biodetecció basada en fags es considera d’especial rellevància en biotecnologia. A més, és possible vincular marcadors específics en els genomes dels fags per a detectar per mitjà d’imatges o sensors per on s’estenen els fags i fer un marcatge in situ, la qual cosa pot ajudar a diagnosticar malalties bacterianes i a fer-ne la localització concreta en el pacient, ja que els fags són molt sensibles i poden detectar bacteris en quantitats molt baixes (Van der Merwe et al., 2014).
Els fags com a tractament
L’ús indiscriminat d’antibiòtics ha provocat l’emergència de bacteris multiresistents o superbacteris. Per desgràcia, avui dia hi ha soques bacterianes que no poden ser tractades amb cap dels antibiòtics disponibles. Aquest problema s’ha convertit en una amenaça mundial i requereix el desenvolupament de tractaments alternatius. De fet, es preveu que l’any 2050 hi haja uns deu milions de morts a l’any relacionades amb superbacteris resistents, més morts que per càncer (Kraker et al., 2016).
En els últims anys, a Europa s’estan realitzant els primers assajos clínics en teràpia de fags, i recentment, a causa de la pandèmia ocasionada pel SARS-CoV-2, els EUA han permès l’ús de fags en pacients de COVID-19 en vigilància intensiva. La raó principal és que la meitat de les defuncions en unitats de vigilància intensiva es devien a infeccions secundàries ocasionades per superbacteris nosocomials causants de pneumònies i sèpsies. En concret, Acinetobacter baumannii, Staphylococcus aureus i Pseudomonas aeruginosa han sigut tractades amb èxit amb fags en aquesta mena de pacients. Així, encara que la falta de legislació en dificulta l’ús en la pràctica clínica, a poc a poc va augmentant el nombre de persones tractades amb fags. Més enllà de la COVID-19, a hores d’ara són els mateixos pacients (a vegades, el personal mèdic) els qui es posen directament en contacte amb investigadors experts en fags per intentar aconseguir virus específics capaços de controlar les infeccions bacterianes diana. De fet, pacients amb infeccions provocades per superbacteris sense tractament han realitzat crides de socors a través de xarxes socials per trobar fags com a alternativa terapèutica. Afortunadament, alguns han estat tractats amb èxit, la qual cosa obre les portes a la teràpia de fags com a tractament contra bacteris patògens (Kortright et al., 2019). Aquest procés és encara lent i complex, però cada vegada hi ha més laboratoris implicats que estem generant biblioteques de fags que permeten agilitar-lo.
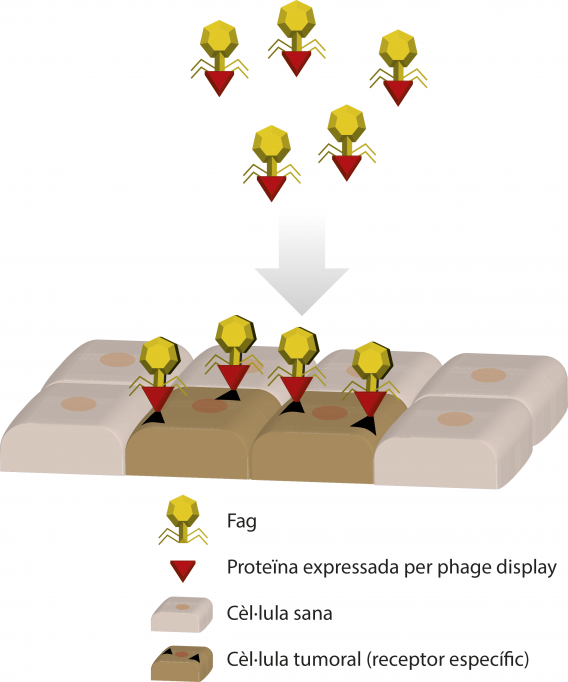
Figura 4. Fags modificats genèticament per a expressar proteïnes exògenes i poder reconèixer cèl·lules eucariotes d’interès com, per exemple, cèl·lules tumorals. Aquestes cèl·lules expressen receptors específics que poden ser reconeguts gràcies a les noves proteïnes expressades en els fags per mitjà de modificació genètica o phage display. Una vegada reconeguda la cèl·lula tumoral, el fag pot actuar com a vehicle de molècules antitumorals o induir la mort cel·lular./ Redibuixat a partir de Pilar Domingo-Calap
En contrast amb l’ampli espectre d’acció dels antibiòtics, com hem comentat prèviament, els fags són altament específics, la qual cosa resulta d’especial interès per a reduir efectes secundaris, ja que el microbioma romandrà en equilibri i solament es destruiran els bacteris diana. En el cas de la teràpia amb fags, és important utilitzar fags lítics capaços de lisar ràpidament els bacteris de manera eficient. Cal destacar que s’ha proposat també l’ús de teràpies combinades de fags amb antibiòtics, ja que s’ha vist que podria haver-hi un efecte sinèrgic combinant els dos tractaments.
Una altra aplicació terapèutica dels fags és, de nou, a través del phage display. És possible modificar genèticament els fags per a dirigir-los a cèl·lules d’interès, incloent-hi cèl·lules eucariotes. Així, els fags poden utilitzar-se com a vehicles per a fer arribar gens o fàrmacs a les cèl·lules desitjades, tècnica d’especial interès en oncologia, ja que es poden dissenyar fags contra cèl·lules tumorals (Figura 4).
Conclusions
L’ús dels fags en biomedicina és molt ampli i permet abordar la problemàtica dels bacteris resistents des de molts punts de vista (Domingo-Calap i Delgado-Martínez, 2018). Aquestes prometedores eines presenten a més uns certs avantatges davant dels antibiòtics, com és el seu baix cost de producció, que permetria usar-los a tot el món, incloent-hi països poc desenvolupats. D’altra banda, igual com han emergit resistències a antibiòtics, els bacteris poden desenvolupar resistència als fags. No obstant això, al contrari dels antibiòtics, que són molècules químiques estables, els fags evolucionen i s’adapten, i poden contrarestar les resistències. A més, és possible reduir l’emergència de resistències per mitjà de l’evolució dirigida dels fags en el laboratori. Una altra solució és l’ús de còctels de fags, en què es pot reduir l’aparició de resistències de manera significativa.
No obstant això, malgrat la gran versatilitat dels fags i de resultats molt prometedors, encara hi ha punts febles per a implantar-los en la pràctica clínica. Els principals problemes són la falta de legislació i la seua acceptació per part del públic general. Els fags són virus i el seu ús es pot veure blocat per preocupacions ètiques. Per aquestes raons, es necessiten protocols de regulació per a donar seguretat i confiança a la població. Assajos i proves clíniques seguint una normativa (encara inexistent) són necessaris per a demostrar la seguretat dels fags en els éssers humans. En aquest sentit, és important destacar que els fags no són capaços d’infectar cèl·lules eucariotes (llevat que els modifiquem genèticament com hem comentat), la qual cosa fa que siguen biològicament i ecològicament segurs. Cal destacar també que les investigacions realitzades fins ara no apunten a un reconeixement dels fags per part del sistema immunitari, de manera que no hi hauria resposta específica contra els fags, la qual cosa facilita administrar-los, fins i tot per via intravenosa.
L’enorme diversitat de fags és també d’especial interès des del punt de vista ecològic, ja que s’estan descobrint noves espècies i observant una biodiversitat inexplorada fins ara que pot portar a noves aplicacions. A més, noves tecnologies vinculades als fags ajudaran a crear millors eines en la pràctica clínica. Un exemple interessant és la nanotecnologia, que pot millorar l’estabilitat dels fags, ajudar a vehicular-los o a crear biosensors. Les aproximacions multidisciplinàries en el camp de la biomedicina ens ajuden a explorar noves vies i a proposar nous tractaments personalitzats de ràpida resposta i menors efectes secundaris.
Per a acabar, ha de destacar-se que l’ús de fags no està relegat al seu ús en clínica, sinó que pot tenir aplicacions en molts camps més, com l’agricultura o la ramaderia. Els mateixos principis que hem estat comentant es poden aplicar a bacteris fitopatògens o que causen malalties en animals. Aquest tipus d’aproximacions també s’està començant a implantar en la indústria agroalimentària, per exemple, als Estats Units i en alguns països de la Unió Europea, on l’ús de fags està permès per al control de bacteris patògens tant en cadena de producció d’aliments com en el producte final (Moye et al., 2018). Concretament, hi ha preparats de fags comercials contra bacteris com ara Escherichia coli, Salmonella sp., i Listeria monocytogenes. La seua comercialització com a eines de biocontrol en seguretat alimentària està donant molt bons resultats, tant en la desinfecció de superfícies industrials com en la descontaminació d’aliments.
Els fags es postulen com a eines molt prometedores en la lluita contra bacteris resistents i, per tant, és necessari invertir en aquest camp d’estudi per a aportar noves dades que afavorisquen la regulació i l’ús rutinari. Fer tasques de divulgació i conscienciació ciutadana és també de gran importància per a poder arribar al públic general, per a donar a conèixer noves teràpies de control de bacteris patògens i abordar la problemàtica amb un tractament ecològicament segur i sostenible. I és que no tots els virus són dolents. N’hi ha de bons que ens poden ajudar a controlar la que podria ser la següent pandèmia: els superbacteris.
Referències
Domingo-Calap, P., & Delgado-Martínez, J. (2018). Bacteriophages: Protagonists of a post-antibiotic era. Antibiotics, 7(3), 66. https://doi.org/10.3390/antibiotics7030066
Ferriol-González, C., & Domingo-Calap, P. (2020). Phages for biofilm removal. Antibiotics, 9(5), 268. https://doi.org/10.3390/antibiotics9050268K
Kortright, K. E., Chan, B. K., Koff, J. L., & Turner, P. E. (2019). Phage therapy: A renewed approach to combat antibiotic-resistant bacteria. Cell Host & Microbe, 25(2), 219–232. https://doi.org/10.1016/j.chom.2019.01.014
Kraker, M. E. A. de, Stewardson, A. J., & Harbarth, S. (2016). Will 10 million people die a year due to antimicrobial resistance by 2050? PLOS Medicine, 13(11), e1002184. https://doi.org/10.1371/journal.pmed.1002184
Moye, Z. D., Woolston, J., & Sulakvelidze, A. (2018). Bacteriophage applications for food production and processing. Viruses, 10(4), 205. https://doi.org/10.3390/v10040205
Smith, G. P. (2019). Phage display: Simple evolution in a petri dish (Nobel lecture). Angewandte Chemie International Edition, 58(41), 14428–14437. https://doi.org/10.1002/anie.201908308
Van der Merwe, R. G., van Helden, P. D., Warren, R. M., Sampson, S. L., & van Pittius, N. C. G. (2014). Phage-based detection of bacterial pathogens. Analyst, 139(11), 2617–2626. https://doi.org/10.1039/C4AN00208C





