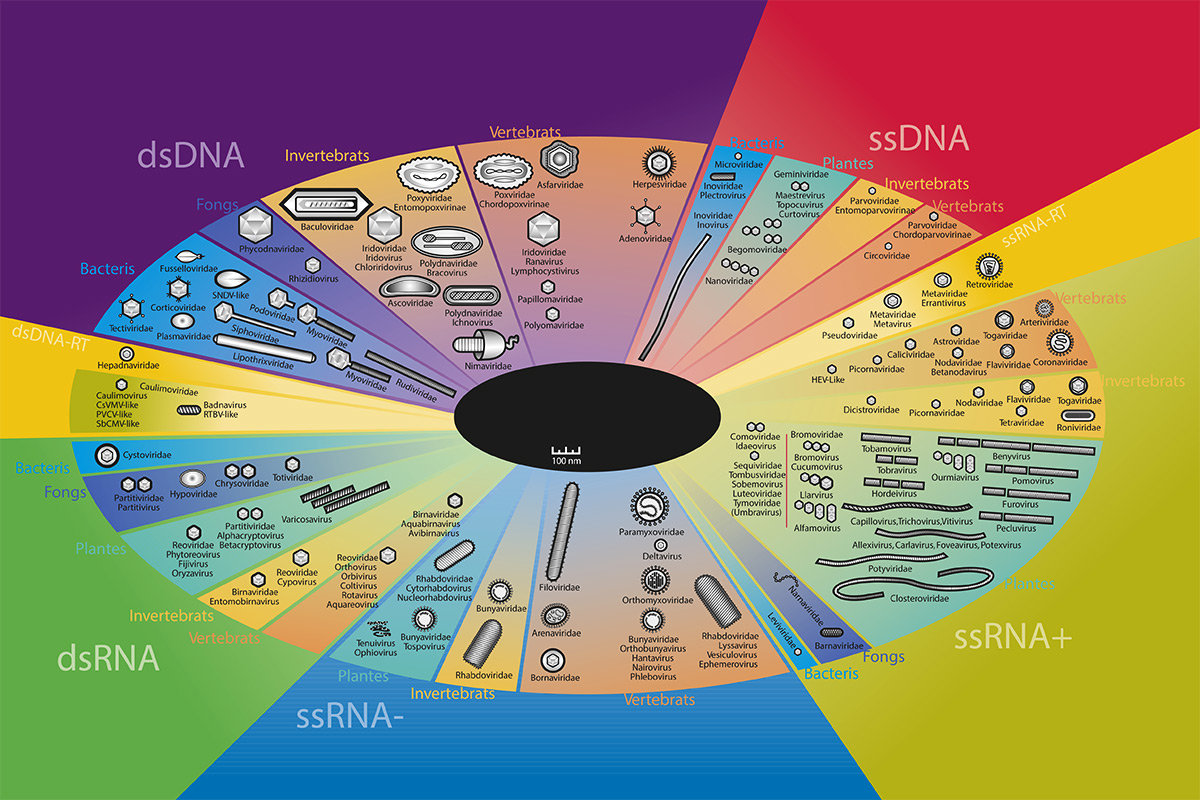
Origin and evolution of virus. The word evolution conjures images of fossils in dusty rocks, organisms stored in jars of formalin and phylogenetic trees spanning geological eras uncovering the history of evolution of life on earth. Modern virology challenges this image and reminds us that evolution is not just contemporary (we can see it happening in real time) but that it also has huge implications on our future: in as much as the human population, and with it all our pets and house plants, increase, the same happens to the viruses affecting us. The general public is beginning to become familiar with viral evolution and diversity, often alarmed by articles in the press about new and terrible viral illnesses, the pandemic of the aids virus and periodic outbreaks of ‘flu’ and other respiratory or gastric viruses. Scientists constantly confront them, with the need to design new pharmaceuticals, vaccines, diagnostic methods and campaigns to control the ever increasing “new emerging diseases” of viral etiology. In fact, we are starting to understand the forces that control viral evolution and the implications this has on our own survival.
Sobre l’origen dels virus
Com que no sabem res sobre l’origen primordial dels virus, qualsevol afirmació sobre la matèria se situa en el terreny de la pura conjectura. No obstant això, el debat entorn de l’origen gira al voltant de tres idees no necessàriament excloents. Per una banda, la teoria regressiva de l’origen dels virus defensa que els virus deriven de paràsits intracel·lulars que van perdre tots els gens no necessaris per a la seua pròpia replicació i transmissió. Aquesta teoria és semblant a la teoria regressiva proposada per a explicar l’origen dels orgànuls d’origen endosimbiòtic com la mitocòndria o el cloroplast. Mentre la teoria de l’origen cel·lular postula que els virus van aparèixer a partir de components cel·lulars que van adquirir la capacitat de replicar autònomament però dins d’una altra cèl·lula. La teoria de l’origen en el brou primitiu o de l’origen coevolutiu suggereix en canvi que els virus van aparèixer com a molècules de RNA autoreplicatives que existien en un ancestral i hipotètic món del RNA, anterior al món cel·lular, i que amb l’aparició de les primeres cèl·lules van començar a parasitar-les i a evolucionar d’una manera concertada amb elles.
«La principal font de variació genètica és la mutació, és a dir, el canvi en la seqüència de nucleòtids que constitueix el genoma del virus»
Pel que fa als virus de DNA (figura 1), la comparació i anàlisi filogenètica de seqüències de polimerases de DNA virals i els seus homòlegs cel·lulars posa d’evidència la coevolució entre moltes d’aquestes famílies de virus (per exemple Herpesviridae, Parvoviridae i Papoviridae) i els seus hostes, amb arbres filogenètics en què perfectament solapen les divergències entre gèneres virals i els seus respectius hostes. A més, hi ha una associació molt estreta entre certes variants de seqüència d’un mateix virus i el genotip de l’hoste. Així, per exemple, distintes variants dels tipus 16 i 18 de papil·lomavirus humans es distribueixen en les poblacions humanes segons un patró geogràfic i racial ben definit.
Quant als virus de RNA o ribovirus (figura 1), les inferències es fan molt més difícils a causa de la major velocitat d’acumulació de mutacions dels genomes de RNA. A més, els genomes de RNA són molt més compactes i comparteixen poca informació amb els seus hostes. No obstant això, l’estudi de la seqüència nucleotídica d’aquest tipus de virus revela l’existència de superfamílies definides per ordenacions gèniques idèntiques i estratègies comunes de codificació dels seus productes i replicació, la qual cosa suggereix, o bé un ancestre comú, o bé que distints virus van adoptar una mateixa solució evolutiva. Com que aquests virus infecten tant animals com plantes, aquesta conservació apunta a la possible existència d’un ancestre comú viral anterior a la separació dels dos regnes.
Basant-se en les propietats de la transcriptasa inversa, H. Temin (1989) va adoptar la hipòtesi del protovirus per a explicar l’origen dels retrovirus (figura 1). Segons aquesta hipòtesi, un enzim semblant a una transcriptasa inversa s’encarregava de copiar segments de RNA en DNA que era integrat en el genoma de l’hoste en forma de retroelements. A la llarga, aquests van adquirir major complexitat, i inclogueren dominis funcionals amb funció d’integrasa o helicasa, regions reguladores i gens estructurals que codificaven per a les proteïnes de l’embolcall. Aquesta hipòtesi prediu que fins i tot haurien de trobar-se empremtes d’aquest procés en el genoma dels mamífers. De fet, molts dels intermediaris esmentats són abundants en els genomes eucariotes en forma de pseudogens, retroposons, retrotransposons i tota una varietat de retrovirus endògens.
Per evolució entenem el canvi en la composició genètica de les poblacions. La teoria quantitativa de la genètica de poblacions ens ensenya que la condició prèvia perquè actue la selecció natural és l’existència de variació genètica. Si hi ha variació genètica, i aquesta té un efecte sobre l’eficàcia dels organismes, llavors aquells genotips més eficaços deixaran més descendents i, per tant, la seua freqüència en la població augmentarà en les següents generacions. Malgrat tot, la teoria també prediu que hi ha condicions en què la selecció natural no actua eficientment i, per tant, el grau d’adaptació pot disminuir i pot portar les poblacions fins l’extinció. Aquests principis bàsics de la teoria evolutiva també regeixen el comportament temporal de les poblacions virals.
«A mesura que la població viral s’aproxima a l’òptim adaptatiu, són necessàries mutacions cada vegada més específiques i, òbviament, aquestes mutacions són més infreqüents»
La gènesi de variabilitat genètica en poblacions virals
La principal font de variació genètica és la mutació, és a dir, el canvi en la seqüència de nucleòtids que constitueix el genoma del virus. Aquests canvis poden ser substitucions d’un nucleòtid per un altre distint, o la inserció o deleció (eliminació) de seqüències de grandària variable. La principal causa de mutació són els errors introduïts per les polimerases virals, els enzims responsables d’obtenir còpies del genoma parental. Aquí cal distingir entre virus de DNA i virus de RNA. La taxa de mutació dels primers està al voltant de 0,004 errors per genoma i replicació; un valor que està en el mateix ordre de magnitud que el mesurat per als seus hostes cel·lulars. Per contra, per als ribovirus les estimacions de la taxa de mutació genòmica disponibles per a distints virus són unes 1.000 vegades majors, en el rang d’un error per genoma i replicació.
La següent causa de variació genètica és la recombinació o generació de genomes híbrids que contenen parts procedents de dos virus parentals distints. La recombinació en virus de DNA, i probablement en retrovirus, segurament la realitzen enzims cel·lulars. Per la seua banda, alguns ribovirus (p.e. Coronaviridae i Picornaviridae) poden recombinar mitjançant un mecanisme conegut com “salt de motlle” en què una polimerasa que copia un genoma salta a una altra i continua la còpia.
Una última font de variació, particularment important en virus amb genomes segmentats com el de la grip, és la reordenació de segments, que consisteix en l’encapsidament de segments genòmics procedents de variants diferents d’un mateix virus que coincideixen en el mateix hoste en cas de coinfecció.
No obstant això aquesta enorme variabilitat és una arma de doble tall, depenent de l’efecte que sobre l’eficàcia d’un virus tinga cada possible mutació. Per a un determinat ambient constant, considerarem beneficioses aquelles mutacions que facen més eficaços els genomes que les porten, direm neutrals d’aquelles que no tinguen efecte aparent sobre l’eficàcia i deletèries d’aquelles que tinguen un impacte negatiu sobre l’eficàcia viral. És intuïtiu, i així es pot comprovar que la immensa majoria de les mutacions tindran un efecte deleteri sobre la viabilitat viral i que només una petita fracció contribuirà a augmentar l’adaptació viral.
«El poliovirus produeix al voltant de 10.000 noves partícules per cèl·lula infectada en tan sols quatre hores. Els nombres fins i tot són més aclaparadors quan es considera la productivitat per organisme infectat»
En pensar en variació genètica en poblacions virals no hem de perdre de vista un altre factor clau: l’enorme productivitat viral. La infecció d’una única cèl·lula per un virus resulta en la producció d’un enorme nombre de nous virus. Per exemple, el poliovirus produeix al voltant de 10.000 noves partícules per cèl·lula infectada en tan sols quatre hores. Els nombres fins i tot són més aclaparadors quan es considera la productivitat per organisme infectat: entre les 109 partícules per dia en el cas del virus de tipus 1 de la immunodeficiència humana (VIH-1) i les 10¹¹ partícules per dia per al virus de l’hepatitis B. Si combinem les estimacions de taxa de mutació anteriors amb aquests valors de productivitat se’ns fa evident la imatge d’immenses poblacions extremadament heterogènies. Aquestes són les condicions necessàries perquè actue la selecció natural d’una manera molt eficient.
Adaptació per acció de la selecció natural
A pesar del caràcter aleatori de la mutació, un patró comú d’evolució ha estat observat en distints virus. Aquest patró es caracteritza per augments exponencials de l’eficàcia en períodes relativament curts de temps seguits per una deceleració en la taxa d’adaptació per a, finalment, arribar a una situació d’equilibri dinàmic en què ja no s’observaven més augments en l’eficàcia (figura 2A) i es pot considerar que el virus està adaptat a la nova situació. La raó per a aquesta deceleració en la velocitat d’adaptació té a veure amb la disponibilitat de mutacions beneficioses i la magnitud de l’efecte beneficiós associat amb cada possible mutació. Al principi del procés, quan la població viral es troba lluny de l’òptim adaptatiu propi del seu ambient, hi ha moltes característiques fenotípiques que millorar i pràcticament qualsevol canvi beneficiós que ocórrega provocarà un augment en l’eficàcia biològica que conduirà la població cap a un òptim d’eficàcia. A mesura que la població s’aproxima a l’òptim adaptatiu, són necessàries mutacions cada vegada més específiques i, òbviament, aquestes mutacions són més infreqüents. En aquest sentit, un nou ambient pot significar des d’una nova espècie hoste, un nou tipus cel·lular o, fins i tot, l’existència de resposta immune o la presència de fàrmacs antivirals
.
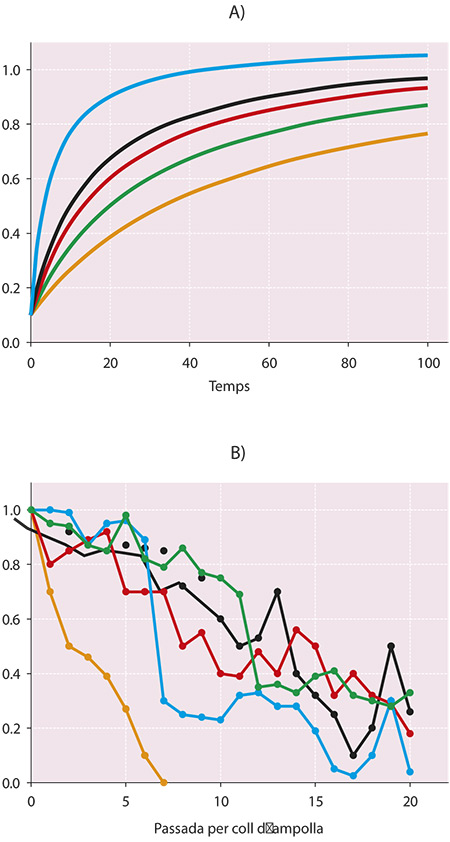
Figura 2. Efecte de la grandària poblacional sobre la dinàmica evolutiva viral. Si la selecció natural és la força evolutiva principal, les poblacions virals s’adapten al seu entorn (A). Després de contínues transmissions a través de colls d’ampolla poblacionals l’eficàcia de les poblacions virals es redueix dràsticament (B). En tots els casos, distintes línies representen distintes trajectòries evolutives independents.
Mutacions deletèries, colls d’ampolla i deriva genètica
La genètica de poblacions prediu que si la taxa de mutació és gran i la població petita o està sotmesa a continus colls d’ampolla poblacionals (reducció dràstica de la grandària poblacional) de molt pocs individus, els genomes lliures de mutacions són escassos i poden no passar a la següent generació simplement per atzar (o deriva genètica). Com que després de cada coll d’ampolla la quantitat de variació genètica es redueix pràcticament a zero, la selecció natural deixa de ser el mecanisme fonamental que regeix el procés evolutiu i pren el relleu la deriva genètica. En poblacions asexuals –clonals– aquesta pèrdua serà irreversible i el nombre mitjà de mutacions per genoma augmentarà amb les successives pèrdues dels individus portadors dels genomes menys mutats. Aquest fenomen es coneix com a cadell de Muller.
La grandària de les poblacions virals canvia tremendament com a conseqüència de la transmissió entre hostes i fins i tot, entre distints teixits dins d’un mateix individu infectat. Una nova infecció pot ser iniciada amb molt poques partícules virals que, posteriorment, s’expandiran fins assolir la càrrega viral pròpia de la infecció. Les partícules que inicien la infecció han estat preses a l’atzar del conjunt de genotips que constituïen la població original i, per tant, no tenen per què ser representatives de la constitució genètica de la població original. Pensem, per exemple, en la transmissió aèria del virus de la grip. De l’enorme quantitat de partícules virals que es troben en un individu malalt, únicament unes poques unitats, potser desenes, passaran, contingudes en les minúscules gotes de saliva expel·lides en esternudar, fins a l’incaut que estava just enfront del malalt en aquell moment. I d’aquestes, no totes passaran al torrent sanguini i iniciaran una nova infecció. En aquestes condicions, es pot esperar que el cadell de Muller represente algun paper durant l’evolució viral. En efecte, ja ha estat comprovat en virus com ara el bacteriòfag f6, el de l’estomatitis vesicular, el de la febre aftosa, el VIH-1 o el del mosaic del cogombre. El perfil de pèrdua d’eficàcia és semblant en tots, després de múltiples transmissions a través de colls d’ampolla poblacionals l’eficàcia biològica pateix dramàtiques pèrdues seguint un patró de fluctuacions aleatòries (figura 2B).
I si el cadell de Muller actua, per què els virus no s’extingeixen? Simplement per que després del coll d’ampolla inicial es regenera la immensa variabilitat que esmentàvem adés (incloent-hi la reversió al genotip ancestral) i de nou la selecció natural afavoreix la recuperació de l’eficàcia poblacional. En altres paraules, tot procés d’infecció viral alterna dues fases, una primera, breu, on és la deriva genètica la força evolutiva que domina i que té com a conseqüència que la infecció s’inicie amb genotips no optimitzats; i una segona, llarga, en què és la selecció natural la força evolutiva dominant i que té com a conseqüència la reoptimització de la població viral. El resultat final dependrà de l’equilibri entre aquests dos processos.
Virus emergents
Definim un virus com emergent si apareix per primera vegada en una població donada o, més comunament, si apareix per primera vegada en una espècie induint una simptomatologia molt més severa que la produïda en l’espècie hoste original.
Direm que un virus és reemergent quan és descrit en una espècie hoste després d’un llarg temps sense haver-hi estat detectat. Mentre que durant els anys noranta el terme va començar a formar part del lèxic popular, generalment amb connotacions catastrofistes, els virus emergents ja feia temps que eren considerats com la més clara manifestació de l’evolució viral. La taula 1 mostra alguns exemples de virus emergents. El denominador comú de tots els exemples recollits és el canvi d’hoste, és a dir, el salt d’un virus des del seu hoste natural a una nova espècie. Tots aquests exemples també es caracteritzen per un augment dramàtic de la virulència en la nova espècie hoste.
| Virus | Família | Possibles causes per a l’emergència |
| Virus de Junin, Guanarito, Lassa, Machupo i Sabia | Arenaviridae | Pràctiques agrícoles que afavoreixen el contacte entre humans i rosegadors |
| Virus Sin Nombre | Bunyaviridae | Creixement descontrolat de poblacions de ratolins i el seu contacte amb humans |
| Virus de la febre de la vall del Rift | Bunyaviridae | Noves preses i irrigació extensiva de territoris abans de secà |
| Hantavirus | Bunyaviridae | Pràctiques agrícoles que afavoreixen el contacte entre humans i rosegadors |
| Virus de Norwalk, Sapporo i altres virus gastroentèrics | Caliciviridae i altres | Nous mètodes de detecció |
| Virus de la síndrome respiratòria aguda severa (SARS) | Coronaviridae | Alta densitat poblacional, que facilita el contacte entre persones |
| Virus d’Ebola | Filoviridae | Desforestació de selves verges i contacte amb l’hoste natural (desconegut)/importació de micos infectats a Europa i EUA |
| Virus de Marburg | Filoviridae | Importació de micos infectats a Europa |
| Virus del dengue | Flaviviridae | Alta densitat poblacional; reserves d’aigües a l’aire lliure en climes càlids que afavoreixen el creixement del mosquit vector; canvi climàtic |
| Virus de la febre groga | Flaviviridae | Colonització de zones humides abans deshabitades i contacte amb el mosquit vector; canvi climàtic |
| Virus de l’hepatitis C | Flaviviridae | Transfusió amb hemoderivats contaminats; ús de xeringues i altres materials clínics contaminats |
| Virus de l’encefalitis del Nil Occidental | Flaviviridae | Migració d’aus infectades a zones densament poblades on els mosquits transmeten el virus des de les aus als humans; canvi climàtic |
| Virus de la pesta porcina clàssica | Flaviviridae | Importació de ramat infectat; contagi des d’animals salvatges |
| Virus de la grip | Orthomyxoviridae | Mescla de porcs i aus en granges; enorme mobilitat de les poblacions humanes i de ramat |
| Parvovirus caní | Parvoviridae | Mutació espontània del virus de la panleucopènia felina que va resultar en nous tropisme d’hoste i patogènesi |
| Virus de la febre aftosa | Picornaviridae | Importació de ramat infectat |
| Virus de la immunodeficiència humana (tipus 1) | Retroviridae | Transfusió amb hemoderivats contaminats ; transmissió sexual; ús de xeringues contaminades, alta mobilitat de les poblacions humanes |
| Virus de la leucèmia dels limfòcits T en humans | Retroviridae | Transfusió amb hemoderivats contaminats, ús de xeringues contaminades; factors socials |
Taula 1. Exemples de virus emergents i reemergents [actualitzat a partir de les dades recopilades per Morse (1993)].
La (re-)aparició d’un virus emergent sempre és equivalent a la gènesi de noves variants virals. Molt sovint aquestes variants emergents són el resultat de grans reordenacions genòmiques, com per exemple en el cas de noves estirps del virus de la grip, on partícules virals que contenen segments genòmics procedents de virus que infecten aus o porcs són les responsables de brots epidèmics en humans. En altres ocasions basta amb petits canvis aïllats per a produir el bot interespecífic, com en el cas del parvovirus caní, on canvis en uns pocs llocs aminoacídicos de la proteïna de la càpside del virus de la panleucopènia felina basten perquè el virus infecte cèl·lules canines eficientment (Parker i Parrish, 1997).
A més de les propietats intrínseques del virus, quins altres factors afavoreixen l’emergència de malalties virals? Normalment no es pot atribuir a un únic factor l’emergència d’una malaltia, sinó que cal cercar la conjunció d’uns quants. Lázaro i Escarmís (2002) recullen tres factors. En primer lloc, el canvi climàtic global. L’augment en la temperatura mitjana del planeta afavoreix que els insectes que actuen com a vector de transmissió colonitzen latituds més altes on abans les baixes temperatures els impedien reproduir-se adequadament. D’exemples, en tenim els virus del dengue, de les febres groga i de la vall del Rift, el de l’encefalitis equina oriental, australiana i del Nil occidental i la síndrome pulmonar causada per hantavirus.
«Mentre que durant els anys noranta el terme va començar a formar part del lèxic popular, els virus emergents ja feia temps que eren considerats com la més clara manifestació de l’evolució viral»
Un segon factor són els canvis ecològics. La desforestació i posterior transformació de zones de selva verge en terrenys d’ús agrícola i ramader ha permès el contacte per primera vegada de l’home així com dels seus animals i plantes domèstics amb patògens amb què mai abans havien tingut relació. A més, la substitució d’extenses zones de flora autòctona per monocultius agrícoles ha facilitat l’aparició de plagues de gran impacte econòmic, com la causada a Austràlia i el Sud-est Asiàtic pel virus de l’enduriment del fruit de la passió o la provocada al Carib i Amèrica Central pel virus del mosaic daurat de la tomaca. Encara que els virus emergents més populars producte de la invasió i destrucció de selves verges són el de l’Ebola i el VIH-1.
Per últim, la demografia i el comportament social afavoreixen també l’aparició de noves enfermetats virals. Les migracions humanes han estat la major font d’epidèmies al llarg de la història, i ben conegut és que les malalties virals introduïdes pels conquistadors espanyols a Amèrica Central i el Carib (grip, galteres, xarampió i pigota) van contribuir en gran manera a l’extermini de la població autòctona. Més recentment, els moviments migratoris forçats per conflictes bèl·lics, l’escassetat de menjar, i en menor grau el turisme, permeten que virus exòtics es traslladen ràpidament a zones del planeta densament poblades. Aquest problema s’agreuja quan coincideix amb condicions sanitàries deficients. També, el comerç incontrolat d’animals i plantes permet la disseminació de virus potencialment letals per a l’home, com va ser el cas del virus hemorràgic de Marburg, introduït en aquesta ciutat alemanya en mones procedents d’Uganda i destinades a la investigació mèdica.
Bibliografia
Bernard, H. U., 1994. “Coevolution of papillomaviruses with human populations”, Trends Microbiol., 2: 140-143.
Drake, J. W., Charlesworth, B., Charlesworth, D. i J. F. Crow, 1998. “Rates of spontaneous mutation”, Genetics, 148: 1667-1686.
Koonin, E. V. i V. V. Dolja, 1993. “Evolution and taxonomy of positive-strand RNA viruses: implications of comparative analysis of amine acid sequences”, Crit. Rev. Biochem. Mol. Biol., 28: 375-430.
Lázaro, E. i C. Escarmís, 2002. Virus emergentes: la amenaza oculta, Equipo Sirius SA.
Morse, S., 1993. Emerging Viruses, Oxford Univ. Press.
Novella, I. S., Duarte, E. A., Elena, S. F., Moya, A., Domingo, E., i J. J. Holland, 1995. “Exponential increases of RNA virus fitness during large population transmissions”, Proc. Natl. Acad. Sci. USA, 92: 5841-5844.
Parker, J. S. L. i C. R. Parrish, 1997. “Canine parvovirus host range is determined by the specific conformation of an additional región of the capsid”, J. Virol., 71: 9214-9222.
Temin, H. M., 1989. “Retrovirus variation and evolution”, Genome, 31: 17-22.
Webster, R. G., 1998. “Influenza: an emerging disease”, Emerg. Infect. Dis., 4: 436-441.





